Яды и противоядия [Гдаль Иосифович Оксенгендлер] (fb2) читать онлайн
[Настройки текста] [Cбросить фильтры]
[Оглавление]
Г. И. Оксенгендлер ЯДЫ И ПРОТИВОЯДИЯ
Введение
В настоящее время невозможно представить ни один вид человеческой деятельности, прямо или косвенно не связанный с влиянием на организм химических веществ, количество которых составляет десятки тысяч и продолжает непрерывно расти. В их числе — ядохимикаты (инсектициды, пестициды, гербициды), препараты бытового назначения (краски, лаки, растворители, синтетические моющие средства), лекарственные вещества, химические добавки к пищевым продуктам, косметические средства. Немаловажное значение в этой связи имеют биологически активные соединения растительного происхождения: алкалоиды, гликозиды, органические кислоты, многие из которых не разрушаются при высушивании, длительном хранении, термической обработке самих растений или мяса отравленных ими животных. Еще одна группа ядов образуется в результате жизнедеятельности микроорганизмов. Микробные яды (например, ботулинический токсин) подчас в сотни раз превосходят высокотоксичные синтетические вещества по силе биологического действия. Надо иметь также в виду, что в природе есть много ядовитых существ: членистоногих, моллюсков, рыб, змей, которые могут стать опасными для человека. Ведущие токсикологи с обоснованным беспокойством и тревогой отмечают, что бурное развитие химической промышленности, внедрение химической технологии во многие отрасли народного хозяйства и в сферу быта создают химическое загрязнение среды обитания и серьезную угрозу здоровью населения, приводят к значительным экономическим потерям (заболевания и гибель животных, экологически связанных с человеком, например рыб, ухудшение пищевых свойств сельскохозяйственных растений и многое другое).[1] Промышленные источники вредных для человека веществ, которые могут быть как активными (различные функционирующие механизмы, приборы, агрегаты, а также сам человек), так и пассивными (материалы, покрытия и другие объекты), способны выделять в воздух десятки токсичных агентов. Например, в производстве витаминов в воздухе рабочей зоны обнаружено более 30, а в производстве шин (при вулканизации) более 100 вредных для организма химических соединении.[2] Однако, несмотря на большое количество и разнообразие ядовитых соединений, образующихся при многих производственных процессах, удельный вес профессиональных интоксикаций в последние годы снижается благодаря успехам промышленной гигиены и медицинским предупредительным мероприятиям. Это в первую очередь можно видеть на примере СССР и социалистических стран. Следует отметить, что поступление различных ядовитых веществ из заводских труб и городского транспорта в воздушные бассейны многих больших городов подчас достигает опасного уровня. Так, только за одни сутки крупный нефтеперерабатывающий завод может выбросить в атмосферу до 520 т углеводородов, 1,8 т сероводорода, 600 т окиси углерода, 310 т сернистого газа, а выхлопные газы автомобилей, этих по сути дела химических фабрик на колесах, содержат на 1 т сжигаемого горючего от 12 до 24 кг окислов азота, от 0,3 до 5 кг аммиака и углеводородов, до 4–5% окиси углерода.[3] С увеличением удельного веса воздушного транспорта возрастает опасность авиационных выхлопных газов: один реактивный самолет оставляет после взлета и при посадке ядовитый шлейф, равный по объему выхлопным газам 7 тыс. автомашин.[4] Надо иметь также в виду, что в реки, озера, моря постоянно проникают ядовитые вещества из воздуха и почвы. К примеру, половина пестицидов, находящихся в океане, попала в него из воздуха. Они способны сохраняться в воде в течение многих лет и создавать опасность вредного воздействия на людей. В связи с изложенным приобретает все возрастающий практический интерес выдвинутая академиком АМН СССР А. А. Покровским[5] концепция охраны внутренней среды человека от многочисленных вредных для организма химических агентов. При этом в широком плане ставится задача создания барьера не только в отношении веществ, обладающих острой или хронической токсичностью, но и для любых не свойственных организму химических соединений, способных проникать в ткани и органы, накапливаться в них и сохраняться длительное время. Международная статистика показывает, что «токсическая ситуация», сложившаяся в экономически развитых странах, сопровождается неуклонным увеличением общего числа острых отравлений. Среди них, по данным большинства авторов, бытовые (случайные) отравления занимают по частоте первое место, преднамеренные (суицидальные) — второе и профессиональные — третье. Не следует забывать, что в военных кругах империалистических государств в качестве перспективного средства ведения войны рассматривается химическое оружие, основу которого, как известно, составляют отравляющие вещества — химические соединения, способные поражать людей при их применении в ничтожно малых дозах.[6] Многие примеры применения империалистами отравляющих и ядовитых веществ в разных точках земного шара в последние десятилетия свидетельствуют о реальной опасности этого оружия. В некоторых западных странах как в специальных изданиях, так и в литературе, предназначенной для широких масс, пропагандируется идея «гуманности» отравляющих веществ по сравнению с другими средствами ведения войны. При этом США и другие государства — члены НАТО — всячески препятствуют запрещению химического оружия. Из изложенного следует, что разработка действенных мер борьбы с отрицательным влиянием вредных химических факторов на организм человека становится одной из первоочередных задач науки и практики. Отсюда становится понятным и главное назначение токсикологии[7] как науки — раскрытие сущности влияния ядов на организм и создание на этой основе эффективных средств предупреждения и лечения отравлений. Точная и краткая формулировка одного из основных способов решения этой проблемы — «создание полезных веществ, активно действующих против опасных веществ».[8] В настоящей книге на примерах распространенных интоксикаций рассматриваются сущность и особенности влияния на организм ядовитых веществ, освещаются пути и характер научного поиска токсикологов, химиков, биохимиков, фармакологов в раскрытии молекулярных механизмов токсических процессов и разработке эффективных противоядий. При этом автор далек от стремления сколько-нибудь полно осветить такую большую проблему, а лишь предпринимает попытку привлечь внимание читателя к важнейшим разделам современной токсикологии и к достижениям этой развивающейся науки. Автор выражает глубокую благодарность академику Е. Н. Мишустину, а также своему товарищу по многолетней совместной работе Ю. Н. Лейкину за просмотр рукописи и ценные советы по ее улучшению.ГЛАВА 1 Яды и организм
Биологическая активность химических соединений определяется их структурой, физическими и химическими свойствами, особенностями механизма действия, путей поступления в организм и превращения в нем, а также дозой (концентрацией) и длительностью влияния на организм. В зависимости от того, в каком количестве действует то или иное вещество, оно может являться или индифферентным для организма, или лекарством, или ядом. При значительных превышениях доз многие лекарственные вещества становятся ядами. Так, например, увеличение лечебной дозы сердечного гликозида строфантина в 2,5–3 раза уже приводит к отравлению. В то же время такой яд, как мышьяк, в малых дозах является лекарственным препаратом. Лечебным действием обладает и известное отравляющее вещество иприт: разбавленный в 20000 раз вазелином, этот яд военной химии применяется под названием псориазин в качестве средства против чешуйчатого лишая. С другой стороны, постоянно поступающие в организм с пищей или вдыхаемым воздухом вещества становятся вредными для человека, когда они вводятся в непривычно больших количествах или при измененных условиях внешней среды. Это можно видеть на примере поваренной соли, если увеличить ее концентрацию в организме по сравнению с обычной в 10 раз, или — кислорода, если вдыхать его при давлении, превышающем нормальное в несколько раз. В этом смысле понятно и происхождение известного изречения одного из корифеев средневековой медицины Парацельса (1493–1541 гг.): «Все есть яд, и ничто не лишено ядовитости; одна лишь доза делает яд незаметным». С ним перекликаются слова великого поэта древности Рудаки (умер в 941 г.):Доза. Концентрация. Токсичность
Как уже отмечалось, воздействуя на организм в различных количествах, одно и то же вещество вызывает неодинаковый эффект. Минимальная действующая, или пороговая, доза (концентрация) ядовитого вещества — это такое его наименьшее количество, которое вызывает явные, но обратимые изменения жизнедеятельности. Минимальная токсическая доза — это уже гораздо большее количество яда, вызывающее выраженное отравление с комплексом характерных патологических сдвигов в организме, но без смертельного исхода. Чем сильнее яд, тем ближе величины минимально действующей и минимально токсической доз.[18] Помимо названных, в токсикологии принято еще рассматривать смертельные (летальные) дозы и концентрации ядов, т. е. те их количества, которые приводят человека (или животное) к гибели при отсутствии лечения. Летальные дозы определяются в результате опытов на животных. В экспериментальной токсикологии чаще всего пользуются средней летальной дозой (DL50) или концентрацией (CL50) яда, при которых погибает 50% подопытных животных. Если же наблюдается 100%-ная их гибель, то такая доза или концентрация обозначается как абсолютная летальная (DL100 и CL100). Понятие токсичности (ядовитости) означает меру несовместимости вещества с жизнью и определяется величиной, обратной DL50(CL50), т. е. ).
В зависимости от путей поступления яда в организм определяют следующие токсикометрические параметры: мг/кг массы тела — при воздействии яда, попавшего с отравленной пищей и водой внутрь организма, а также на кожу и слизистые оболочки; мг/л или г/м3 воздуха — при ингаляционном (т. е. через органы дыхания) проникновении яда в организм в виде газа, пара или аэрозоля; мг/см2 поверхности — при попадании яда на кожу. Имеются способы и более углубленной количественной оценки ядовитости химических соединений. Так, при воздействии через дыхательные пути степень токсичности яда (Т) характеризует модифицированная формула Габера:
).
В зависимости от путей поступления яда в организм определяют следующие токсикометрические параметры: мг/кг массы тела — при воздействии яда, попавшего с отравленной пищей и водой внутрь организма, а также на кожу и слизистые оболочки; мг/л или г/м3 воздуха — при ингаляционном (т. е. через органы дыхания) проникновении яда в организм в виде газа, пара или аэрозоля; мг/см2 поверхности — при попадании яда на кожу. Имеются способы и более углубленной количественной оценки ядовитости химических соединений. Так, при воздействии через дыхательные пути степень токсичности яда (Т) характеризует модифицированная формула Габера:
 где с — концентрация яда в воздухе (мг/л); t — время воздействия (мин); υ — объем вентиляции легких (л/мин); g — масса тела (кг).
При разных способах введения ядов в организм требуются неодинаковые их количества для того, чтобы вызвать один и тот же токсический эффект. Например, DL50 диизопропилфторфосфата, установленные на кроликах при различных способах введения, следующие (в мг/кг):[19]
где с — концентрация яда в воздухе (мг/л); t — время воздействия (мин); υ — объем вентиляции легких (л/мин); g — масса тела (кг).
При разных способах введения ядов в организм требуются неодинаковые их количества для того, чтобы вызвать один и тот же токсический эффект. Например, DL50 диизопропилфторфосфата, установленные на кроликах при различных способах введения, следующие (в мг/кг):[19]
 Значительное превышение пероральной дозы над парентеральными (т. е. введенными в организм, минуя желудочно-кишечный тракт) свидетельствует прежде всего о разрушении большей части яда в пищеварительной системе.
C учетом величины среднесмертельных доз (концентраций) при различных путях поступления в организм яды подразделяются на группы. Одна из таких классификаций, разработанных в нашей стране, приводится в таблице.
Классификация вредных веществ по степени токсичности (рекомендована Всесоюзной проблемной комиссией по научным основам гигиены труда и профессиональной патологии в 1970 г.)
Значительное превышение пероральной дозы над парентеральными (т. е. введенными в организм, минуя желудочно-кишечный тракт) свидетельствует прежде всего о разрушении большей части яда в пищеварительной системе.
C учетом величины среднесмертельных доз (концентраций) при различных путях поступления в организм яды подразделяются на группы. Одна из таких классификаций, разработанных в нашей стране, приводится в таблице.
Классификация вредных веществ по степени токсичности (рекомендована Всесоюзной проблемной комиссией по научным основам гигиены труда и профессиональной патологии в 1970 г.)
 При повторном воздействии одного и того же яда на организм может изменяться течение отравления из-за развития явлений кумуляции, сенсибилизации и привыкания. Под кумуляцией понимается накопление в организме токсичного вещества (материальная кумуляция) или вызываемых им эффектов (функциональная кумуляция). Понятно, что накапливается то вещество, которое медленно выводится или медленно обезвреживается, при этом суммарно действующая доза очень быстро возрастает. Что касается функциональной кумуляции, то она может проявляться тяжелыми расстройствами тогда, когда сам яд не задерживается в организме. Такое явление может наблюдаться, например, при отравлении алкоголем. Степень выраженности кумулятивных свойств ядовитых веществ принято оценивать коэффициентом кумуляции (K), который определяется в эксперименте на животных:
При повторном воздействии одного и того же яда на организм может изменяться течение отравления из-за развития явлений кумуляции, сенсибилизации и привыкания. Под кумуляцией понимается накопление в организме токсичного вещества (материальная кумуляция) или вызываемых им эффектов (функциональная кумуляция). Понятно, что накапливается то вещество, которое медленно выводится или медленно обезвреживается, при этом суммарно действующая доза очень быстро возрастает. Что касается функциональной кумуляции, то она может проявляться тяжелыми расстройствами тогда, когда сам яд не задерживается в организме. Такое явление может наблюдаться, например, при отравлении алкоголем. Степень выраженности кумулятивных свойств ядовитых веществ принято оценивать коэффициентом кумуляции (K), который определяется в эксперименте на животных:
 где а — повторно вводимое животному количество яда, составляющее 0,1–0,05 DL50; b — количество введенных доз (а); с — однократно введенная доза.
В зависимости от величины коэффициента кумуляции токсичные вещества делят на 4 группы:[20]
1) с резко выраженной кумуляцией (К<1);
2) с выраженной кумуляцией (К от 1 до 3);
3) с умеренной кумуляцией (К от 3 до 5);
4) со слабо выраженной кумуляцией (К>5).
Сенсибилизация — состояние организма, при котором повторное воздействие вещества вызывает больший эффект, чем предыдущее. В настоящее время нет единого взгляда на биологическую сущность этого явления. На основании экспериментальных данных можно полагать, что эффект сенсибилизации связан с образованием под влиянием токсичного вещества в крови и других внутренних средах измененных и ставших чужеродными для организма белковых молекул. Последние индуцируют формирование антител — особых структур белковой природы, осуществляющих защитную функцию организма. По-видимому, повторное даже значительно более слабое токсическое воздействие с последующей реакцией яда с антителами (или измененными рецепторными белковыми структурами) вызывает извращенный ответ организма в виде явлений сенсибилизации.
При повторяющемся воздействии ядов на организм можно наблюдать и обратное явление — ослабление их эффектов вследствие привыкания, или толерантности. Механизмы развития толерантности неоднозначны. Так, например, было показано, что привыкание к мышьяковистому ангидриду обусловлено возникновением под его влиянием воспалительных процессов на слизистой оболочке желудочно-кишечного тракта и уменьшением вследствие этого всасывания яда.[21] В то же время, если препараты мышьяка вводить парентерально, толерантности не наблюдается. Однако наиболее частой причиной толерантности является стимуляция, или индукция, ядами активности ферментов, обезвреживающих их в организме. Об этом явлении пойдет еще речь впереди. А сейчас отметим, что привыкание к некоторым ядам, например ФОС, может быть еще обусловлено снижением чувствительности к ним соответствующих биоструктур или перегрузкой последних из-за массированного воздействия на них избыточного количества молекул токсичного вещества.
В связи с изложенным особое значение приобретает законодательная регламентация предельно допустимых концентраций(ПДК) вредных веществ в воздухе рабочей зоны промышленных и сельскохозяйственных предприятий, научно-исследовательских и испытательных учреждений, конструкторских бюро. Считается, что ПДК этих веществ при ежедневной восьмичасовой работе в течение всего рабочего стажа не могут вызывать у работающих заболеваний или отклонений в состоянии здоровья, обнаруживаемых современными методами исследования непосредственно в процессе работы или в отдаленные сроки. По сравнению с другими индустриальными странами в СССР существует более строгий подход к установлению ПДК многих химических агентов. В первую очередь это относится к веществам, обладающим первоначально незаметным, но постепенно нарастающим действием. Например, в Советском Союзе приняты более низкие уровни ПДК, чем в США, для окиси углерода (20 мг/м3 против 100 мг/м3), паров ртути и свинца (0,01 мг/м3 против 0,1 мг/м3), бензола (5 мг/м3 против 80 мг/м3), дихлорэтана (10 мг/м3 против 400 мг/м3) и других токсичных веществ.[22] В нашей стране на предприятиях и учреждениях функционируют специальные токсикологические и санитарные лаборатории, которые осуществляют строгий контроль за содержанием вредных веществ в рабочих помещениях, за внедрением новых экологически безвредных технологических процессов, за работой газопылеулавливающих установок, за сточными водами и т. д. Любой химический продукт, выпускаемый промышленностью СССР, проходит проверку на токсичность и получает токсикологическую характеристику.
где а — повторно вводимое животному количество яда, составляющее 0,1–0,05 DL50; b — количество введенных доз (а); с — однократно введенная доза.
В зависимости от величины коэффициента кумуляции токсичные вещества делят на 4 группы:[20]
1) с резко выраженной кумуляцией (К<1);
2) с выраженной кумуляцией (К от 1 до 3);
3) с умеренной кумуляцией (К от 3 до 5);
4) со слабо выраженной кумуляцией (К>5).
Сенсибилизация — состояние организма, при котором повторное воздействие вещества вызывает больший эффект, чем предыдущее. В настоящее время нет единого взгляда на биологическую сущность этого явления. На основании экспериментальных данных можно полагать, что эффект сенсибилизации связан с образованием под влиянием токсичного вещества в крови и других внутренних средах измененных и ставших чужеродными для организма белковых молекул. Последние индуцируют формирование антител — особых структур белковой природы, осуществляющих защитную функцию организма. По-видимому, повторное даже значительно более слабое токсическое воздействие с последующей реакцией яда с антителами (или измененными рецепторными белковыми структурами) вызывает извращенный ответ организма в виде явлений сенсибилизации.
При повторяющемся воздействии ядов на организм можно наблюдать и обратное явление — ослабление их эффектов вследствие привыкания, или толерантности. Механизмы развития толерантности неоднозначны. Так, например, было показано, что привыкание к мышьяковистому ангидриду обусловлено возникновением под его влиянием воспалительных процессов на слизистой оболочке желудочно-кишечного тракта и уменьшением вследствие этого всасывания яда.[21] В то же время, если препараты мышьяка вводить парентерально, толерантности не наблюдается. Однако наиболее частой причиной толерантности является стимуляция, или индукция, ядами активности ферментов, обезвреживающих их в организме. Об этом явлении пойдет еще речь впереди. А сейчас отметим, что привыкание к некоторым ядам, например ФОС, может быть еще обусловлено снижением чувствительности к ним соответствующих биоструктур или перегрузкой последних из-за массированного воздействия на них избыточного количества молекул токсичного вещества.
В связи с изложенным особое значение приобретает законодательная регламентация предельно допустимых концентраций(ПДК) вредных веществ в воздухе рабочей зоны промышленных и сельскохозяйственных предприятий, научно-исследовательских и испытательных учреждений, конструкторских бюро. Считается, что ПДК этих веществ при ежедневной восьмичасовой работе в течение всего рабочего стажа не могут вызывать у работающих заболеваний или отклонений в состоянии здоровья, обнаруживаемых современными методами исследования непосредственно в процессе работы или в отдаленные сроки. По сравнению с другими индустриальными странами в СССР существует более строгий подход к установлению ПДК многих химических агентов. В первую очередь это относится к веществам, обладающим первоначально незаметным, но постепенно нарастающим действием. Например, в Советском Союзе приняты более низкие уровни ПДК, чем в США, для окиси углерода (20 мг/м3 против 100 мг/м3), паров ртути и свинца (0,01 мг/м3 против 0,1 мг/м3), бензола (5 мг/м3 против 80 мг/м3), дихлорэтана (10 мг/м3 против 400 мг/м3) и других токсичных веществ.[22] В нашей стране на предприятиях и учреждениях функционируют специальные токсикологические и санитарные лаборатории, которые осуществляют строгий контроль за содержанием вредных веществ в рабочих помещениях, за внедрением новых экологически безвредных технологических процессов, за работой газопылеулавливающих установок, за сточными водами и т. д. Любой химический продукт, выпускаемый промышленностью СССР, проходит проверку на токсичность и получает токсикологическую характеристику.
Пути поступления ядов в организм
Поступление ядов в организм человека может происходить через органы дыхания, пищеварительный тракт и кожу. Огромная поверхность легочных альвеол (около 80–90 м2) обеспечивает интенсивное всасывание и быстрый эффект действия ядовитых паров и газов, присутствующих во вдыхаемом воздухе. При этом в первую очередь легкие становятся «входными воротами» для тех из них, которые хорошо растворимы в жирах. Диффундируя через альвеолярно-капиллярную мембрану толщиною около 0,8 мкм, отделяющую воздушную сроду от кровяного русла, молекулы ядов наикратчайшим путем проникают в малый круг кровообращения и затем, минуя печень, через сердце достигают кровеносных сосудов большого круга. С отравленной пищей, водой, а также в «чистом» виде токсичные вещества всасываются в кровь через слизистые оболочки полости рта, желудка и кишечника. Большинство из них всасывается в эпителиальные клетки пищеварительного тракта и далее в кровь по механизму простой диффузии. При этом ведущим, фактором проникновения ядов во внутренние среды организма является их растворимость в липидах (жирах), точнее — характер распределения между липидной и водной фазами в месте всасывания. Существенную роль играет также степень диссоциации ядов. Что касается жиронерастворимых чужеродных веществ, то многие из них проникают через клеточные мембраны слизистых оболочек желудка и кишечника по порам или пространствам между мембранами. Хотя площадь пор составляет только около 0,2% всей поверхности мембраны, тем не менее это обеспечивает всасывание многих водорастворимых и гидрофильных веществ.[23] Током крови из желудочно-кишечного тракта токсичные вещества доставляются в печень — орган, выполняющий барьерную функцию по отношению к подавляющему большинству чужеродных соединений. Как показывают многие исследования, скорость проникновения ядов через неповрежденную кожу прямо пропорциональна их растворимости в липидах, а дальнейший их переход в кровь зависит от способности растворяться в воде. Это относится не только к жидкостям и твердым веществам, но и к газам. Последние могут диффундировать через кожу как через инертную мембрану. Таким способом, например, кожный барьер преодолевают HCN, СО2, СО, H2S и другие газы. Небезынтересно отметить, что прохождению через кожу тяжелых металлов способствует образование ими солей с жирными кислотами жирового слоя кожи. Прежде чем оказаться в том или ином органе (ткани), находящиеся в крови яды преодолевают ряд внутренних клеточных и мембранных барьеров. Важнейшими из них являются гематоэнцефалический и плацентарный — биологические структуры, которые находятся на границе кровеносного русла, с одной стороны, и центральной нервной системой и материнским плодом — с другой. Поэтому результат действия ядов и лекарств часто зависит от того, насколько выражена их способность проникать через барьерные структуры. Так, вещества, растворимые в липидах и быстро диффундирующие через липопротеидные мембраны, например спирты, наркотические средства, многие сульфаниламидные препараты, хорошо проникают в головной и спинной мозг. Они сравнительно легко попадают в кровь плода через плаценту. В этой связи нельзя не упомянуть случаи рождения детей с признаками привыкания к наркотикам, если их матери являлись наркоманками. Пока младенец находится в утробе матери, он адаптируется к определенной дозе наркотика. В то же время отдельные чужеродные вещества плохо проникают через барьерные структуры. Особенно это относится к препаратам, образующим в организме четвертичные аммониевые основания, к сильным электролитам, некоторым антибиотикам, а также коллоидным растворам.Превращение токсичных веществ в организме
Проникающие в организм яды, как и другие чужеродные соединения, могут подвергаться разнообразным биохимическим превращениям (биотрансформации), в результате которых чаще всего образуются менее токсичные вещества (обезвреживание, или детоксикация). Но известно немало случаев усиления токсичности ядов при изменении их структуры в организме. Есть и такие соединения, характерные свойства которых начинают проявляться только вследствие биотрансформации. В то же время определенная часть молекул яда выделяется из организма без каких-либо изменений или вообще остается в нем на более или менее длительный период, фиксируясь белками плазмы крови и тканей. В зависимости от прочности образующегося комплекса «яд-белок» действие яда при этом замедляется или же утрачивается совсем. Кроме того, белковая структура может быть лишь переносчиком ядовитого вещества, доставляющим его к соответствующим рецепторам.[24]
Рис.1. Общая схема поступления, биотрансформации и выведения чужеродных веществ из организма
Изучение процессов биотрансформации позволяет решить ряд практических вопросов токсикологии. Во-первых, познание молекулярной сущности детоксикации ядов дает возможность оцепить защитные механизмы организма и на этой основе наметить пути направленного воздействия на токсический процесс. Во-вторых, о величине поступившей в организм дозы яда (лекарства) можно судить по количеству выделяющихся через почки, кишечник и легкие продуктов их превращения — метаболитов,[25] что дает возможность контролировать состояние здоровья людей, занятых производством и применением токсичных веществ; к тому же при различных заболеваниях образование и выделение из организма многих продуктов биотрансформации чужеродных веществ существенно нарушается. В-третьих, появление ядов в организме часто сопровождается индукцией ферментов, катализирующих (ускоряющих) их превращения. Поэтому, влияя с помощью определенных веществ на активность индуцированных ферментов, можно ускорить или затормозить биохимические процессы превращений чужеродных соединений. В настоящее время установлено, что процессы биотрансформации чужеродных веществ протекают в печени, желудочно-кишечном тракте, легких, почках (рис. 1). Кроме того, согласно результатам исследований профессора И. Д. Гадаскиной,[26] немалое число токсичных соединений подвергается необратимым превращениям и в жировой ткани. Однако главное значение здесь имеет печень, точнее — микросомальная фракция ее клеток. Именно в клетках печени, в их эндоплазматическом ретикулуме, локализуется большинство ферментов, катализирующих превращения чужеродных веществ. Сам ретикулум представляет собой сплетение линопротеидных канальцев, пронизывающих цитоплазму (рис. 2). Наивысшая ферментативная активность связывается с так называемым гладким ретикулумом, который в отличие от шероховатого не имеет на своей поверхности рибосом.[27] Неудивительно поэтому, что при заболеваниях печени резко повышается чувствительность организма ко многим чужеродным веществам. Надо отметить, что, хотя число микросомальных ферментов невелико, они обладают очень важным свойством — высоким сродством к различным чужеродным веществам при относительной химической неспецифичности. Это создает им возможность вступать в реакции обезвреживания практически с любым химическим соединением, попавшим во внутренние среды организма. В последнее время доказано присутствие ряда таких ферментов в других органоидах клетки (например, в митохондриях), а также в плазме крови и в микроорганизмах кишечника.
Рис. 2. Схематическое изображение клетка печени (Парк, 1373). 1 — ядро; 2 — лизосомы; 3 — эндоплазматический ретикулум; 4 — поры в ядерной оболочке; 5 — митохондрии; 6 — шероховатый зндоплазматический ретикулум; 7 — инвагинации плазматической мембраны; 8 — вакуоли; 9 — верна гликогена; 10 — гладкий эндонлазматический ретикулум
Считается, что главным принципом превращения в организме чужеродных соединений является обеспечение наибольшей скорости их выведения путем перевода из жирорастворимых в более водорастворимые химические структуры. В последние 10–15 лет при изучении сущности биохимических превращений чужеродных соединений из жирорастворимых в водорастворимые все большее значение придается так называемой монооксигеназной ферментной системе со смешанной функцией, которая содержит особый белок — цитохром Р-450. Он близок по строению к гемоглобину (в частности, содержит атомы железа с переменной валентностью) и является конечным звеном в группе окисляющих микросомальных ферментов — биотрансформаторов, сосредоточенных преимущественно в клетках печени.[28] В организме цитохром Р-450 может находиться в 2 формах: окисленной и восстановленной. В окисленном состоянии он вначале образует с чужеродным веществом комплексное соединение, которое после этого восстанавливается специальным ферментом — цитохромредуктазой. Затем это, уже восстановленное, соединение реагирует с активированным кислородом, в результате чего образуется окисленное и, как правило, нетоксичное вещество. В основе биотрансформации токсичных веществ лежит несколько типов химических реакций, в результате которых происходит присоединение или же отщепление метальных (-СН3), ацетильных (СН3СОО-), карбоксильных (-СООН), гидроксильных (-ОН) радикалов (групп), а также атомов серы и серосодержащих группировок. Немалое значение имеют процессы распада молекул ядов вплоть до необратимой трансформации их циклических радикалов. Но особую роль среди механизмов обезвреживания ядов играют реакции синтеза, или конъюгации, в результате которых образуются нетоксичные комплексы — конъюгаты. При этом биохимическими компонентами внутренней среды организма, вступающими в необратимое взаимодействие с ядами, являются: глюкуроновая кислота (С5Н9О5СООН), цистеин( ), глицин (NH2-CH2-CОOH),серная кислота и др. Молекулы ядов, содержащие несколько функциональных групп, могут трансформироваться посредством 2 и более метаболических реакций. Попутно отметим одно существенное обстоятельство: поскольку превращение и детоксикация ядовитых веществ за счет реакций конъюгации связаны с расходованием важных для жизнедеятельности веществ, то эти процессы могут вызвать дефицит последних в организме. Таким образом, появляется опасность другого рода — возможность развития вторичных болезненных состояний из-за нехватки необходимых метаболитов. Так, детоксикация многих чужеродных веществ находится в зависимости от запасов гликогена в печени, поскольку из него образуется глюкуроновая кислота. Поэтому при поступлении в организм больших доз веществ, обезвреживание которых осуществляется посредством образования эфиров глюкуроновой кислоты (например, бензольных производных), снижается содержание гликогена — основного легко мобилизуемого резерва углеводов. С другой стороны, есть вещества, которые под воздействием ферментов способны отщеплять молекулы глюкуроновой кислоты и тем самым способствовать обезвреживанию ядов. Одним из таких веществ оказался глицирризин, входящий в состав солодкового корня. Глицирризин содержит 2 молекулы глюкуроновой кислоты в связанном состоянии, которые освобождаются в организме, и это, по-видимому, определяет защитные свойства солодкового корня при многих отравлениях, известные издавна медицине Китая, Тибета, Японии.[29]
Что касается выведения из организма токсичных веществ и продуктов их превращения, то в этом процессе определенную роль играют легкие, органы пищеварения, кожа, различные железы. Но наибольшее значение здесь имеют ночки. Вот почему при многих отравлениях с помощью специальных средств, усиливающих отделение мочи, добиваются быстрейшего удаления ядовитых соединений из организма. Вместе с тем приходится считаться и с повреждающим воздействием на почки некоторых выводимых с мочой ядов (например, ртути). Кроме того, в почках могут задерживаться продукты превращения токсичных веществ, как это имеет место при тяжелых отравлениях этиленгликолем.[30] При его окислении в организме образуется щавелевая кислота и в почечных канальцах выпадают кристаллы оксалата кальция, препятствующие мочеотделению. Вообще подобные явления наблюдаются тогда, когда концентрация выводимых через почки веществ высока.
Чтобы понять биохимическую сущность процессов превращения в организме ядовитых веществ, рассмотрим несколько примеров, касающихся распространенных компонентов химического окружения современного человека.
), глицин (NH2-CH2-CОOH),серная кислота и др. Молекулы ядов, содержащие несколько функциональных групп, могут трансформироваться посредством 2 и более метаболических реакций. Попутно отметим одно существенное обстоятельство: поскольку превращение и детоксикация ядовитых веществ за счет реакций конъюгации связаны с расходованием важных для жизнедеятельности веществ, то эти процессы могут вызвать дефицит последних в организме. Таким образом, появляется опасность другого рода — возможность развития вторичных болезненных состояний из-за нехватки необходимых метаболитов. Так, детоксикация многих чужеродных веществ находится в зависимости от запасов гликогена в печени, поскольку из него образуется глюкуроновая кислота. Поэтому при поступлении в организм больших доз веществ, обезвреживание которых осуществляется посредством образования эфиров глюкуроновой кислоты (например, бензольных производных), снижается содержание гликогена — основного легко мобилизуемого резерва углеводов. С другой стороны, есть вещества, которые под воздействием ферментов способны отщеплять молекулы глюкуроновой кислоты и тем самым способствовать обезвреживанию ядов. Одним из таких веществ оказался глицирризин, входящий в состав солодкового корня. Глицирризин содержит 2 молекулы глюкуроновой кислоты в связанном состоянии, которые освобождаются в организме, и это, по-видимому, определяет защитные свойства солодкового корня при многих отравлениях, известные издавна медицине Китая, Тибета, Японии.[29]
Что касается выведения из организма токсичных веществ и продуктов их превращения, то в этом процессе определенную роль играют легкие, органы пищеварения, кожа, различные железы. Но наибольшее значение здесь имеют ночки. Вот почему при многих отравлениях с помощью специальных средств, усиливающих отделение мочи, добиваются быстрейшего удаления ядовитых соединений из организма. Вместе с тем приходится считаться и с повреждающим воздействием на почки некоторых выводимых с мочой ядов (например, ртути). Кроме того, в почках могут задерживаться продукты превращения токсичных веществ, как это имеет место при тяжелых отравлениях этиленгликолем.[30] При его окислении в организме образуется щавелевая кислота и в почечных канальцах выпадают кристаллы оксалата кальция, препятствующие мочеотделению. Вообще подобные явления наблюдаются тогда, когда концентрация выводимых через почки веществ высока.
Чтобы понять биохимическую сущность процессов превращения в организме ядовитых веществ, рассмотрим несколько примеров, касающихся распространенных компонентов химического окружения современного человека.

Рис. 3. Окисление (гидроксилирование) бензола в ароматические спирты, образование конъюгатов и полное разрушения его молекулы (разрыв ароматического кольца)
Так, бензол, который, подобно другим ароматическим углеводородам, широко используется в качестве растворителя различных веществ и как промежуточный продукт при синтезе красителей, пластических масс, лекарств и других соединений, трансформируется в организме по 3 направлениям с образованием токсичных метаболитов (рис. 3). Последние выделяются через почки. Бензол может очень долго (по некоторым данным, до 10 лет) задерживаться в организме, в особенности в жировой ткани. Определенный интерес представляет изучение процессов превращения в организме токсичных металлов, оказывающих все более широкое влияние на человека в связи с развитием науки и техники и освоением природных богатств. Прежде всего надо отметить, что в результате взаимодействия с окислительно-восстановительными буферными системами клетки, при котором осуществляется перенос электронов, валентность металлов меняется. При этом переход в состояние низшей валентности обычно связывается с уменьшением токсичности металлов. Например, ионы шестивалентного хрома переходят в организме в малотоксичную трехвалентную форму, а трехвалентный хром удается достаточно быстро удалить из организма с помощью некоторых веществ (пиросульфата натрия, виннокаменной кислоты и др.). Ряд металлов (ртуть, кадмий, медь, никель) активно связывается с биокомплексами, в первую очередь — с функциональными группировками ферментов (-SH, -NH2, -СООН и др.), что подчас определяет избирательность их биологического действия. В числе ядохимикатов — веществ, предназначенных для уничтожения вредных живых существ и растений, имеются представители различных классов химических соединений, в тойили иной мере токсичных для человека: хлорорганических, фосфорорганических, металлоорганических, нитрофенольных, цианистых и др. Согласно имеющимся данным,[31] около 10% всех смертельных отравлений в настоящее время вызывается ядохимикатами. Наиболее значимыми из них, как известно, являются ФОС. Гидролизуясь, они, как правило, утрачивают токсичность. В противоположность гидролизу окисление ФОС почти всегда сопровождается усилением их токсичности. Это можно видеть, если сопоставить биотрансформацию 2 инсектицидов — диизопропилфторфосфата, который теряет токсические свойства, отщепляя при гидролизе атом фтора, и тиофоса (производное тиофосфорной кислоты), который окисляется в значительно более токсичный фосфакол (производное ортофосфорной кислоты). Среди широко используемых лекарственных веществ снотворные препараты являются наиболее частыми источниками отравлений. Процессы их превращений в организме изучены достаточно хорошо. В частности, показано, что биотрансформация одного из распространенных производных барбитуровой кислоты — люминала (рис. 4) — протекает медленно, и это лежит в основе его достаточно длительного снотворного действия, так как оно зависит от количества неизмененных молекул люминала, контактирующих с нервными клетками. Распад барбитурового кольца приводит к прекращению действия люминала (как, впрочем, и других барбитуратов), который в лечебных дозах вызывает сон длительностью до 6 ч. В этой связи небезынтересна судьба в организме другого представителя барбитуратов — гексобарбитала. Его снотворное действие намного короче даже при применении значительно больших, чем люминала, доз. Полагают, что это зависит от большей скорости и от большего числа путей инактивации гексобарбитала в организме (образование спиртов, кетонов, деметилированных и других производных). С другой стороны, те барбитураты, которые сохраняются в организме почти в неизмененном виде, как например барбитал, оказывают более длительное снотворное действие, чем люминал. Из этого следует, что вещества, которые в неизмененном виде выводятся с мочой, могут вызвать интоксикацию, если почки не справляются с их удалением из организма.
Важно также отметить, что для понимания непредвиденного токсического эффекта при одновременном применении нескольких лекарств должное значение надо придавать ферментам, влияющим на активность комбинирующихся веществ. Так, например, лекарственный препарат физостигмин при совместном применении с новокаином делает последний весьма токсичным веществом, так как блокирует фермент (эстеразу), гидролизирующий новокаин в организме. Подобным же образом проявляет себя и эфедрин, связывая оксидазу, инактивирующую адреналин и тем самым удлиняя и усиливая действие последнего.
Среди широко используемых лекарственных веществ снотворные препараты являются наиболее частыми источниками отравлений. Процессы их превращений в организме изучены достаточно хорошо. В частности, показано, что биотрансформация одного из распространенных производных барбитуровой кислоты — люминала (рис. 4) — протекает медленно, и это лежит в основе его достаточно длительного снотворного действия, так как оно зависит от количества неизмененных молекул люминала, контактирующих с нервными клетками. Распад барбитурового кольца приводит к прекращению действия люминала (как, впрочем, и других барбитуратов), который в лечебных дозах вызывает сон длительностью до 6 ч. В этой связи небезынтересна судьба в организме другого представителя барбитуратов — гексобарбитала. Его снотворное действие намного короче даже при применении значительно больших, чем люминала, доз. Полагают, что это зависит от большей скорости и от большего числа путей инактивации гексобарбитала в организме (образование спиртов, кетонов, деметилированных и других производных). С другой стороны, те барбитураты, которые сохраняются в организме почти в неизмененном виде, как например барбитал, оказывают более длительное снотворное действие, чем люминал. Из этого следует, что вещества, которые в неизмененном виде выводятся с мочой, могут вызвать интоксикацию, если почки не справляются с их удалением из организма.
Важно также отметить, что для понимания непредвиденного токсического эффекта при одновременном применении нескольких лекарств должное значение надо придавать ферментам, влияющим на активность комбинирующихся веществ. Так, например, лекарственный препарат физостигмин при совместном применении с новокаином делает последний весьма токсичным веществом, так как блокирует фермент (эстеразу), гидролизирующий новокаин в организме. Подобным же образом проявляет себя и эфедрин, связывая оксидазу, инактивирующую адреналин и тем самым удлиняя и усиливая действие последнего.

Рис. 4. Видоизменение люминала в организме по двум направлениям: посредством окисления и за счет распада барбитурового кольца с последующим превращением продукта окисления в конъюгат
Большую роль в биотрансформации лекарств играют процессы индукции (активации) и торможения активности микросомалыных ферментов различными чужеродными веществами. Так, этиловый алкоголь, некоторые инсектициды, никотин ускоряют инактивацию многих лекарственных препаратов. Поэтому фармакологи обращают внимание на нежелательные последствия контакта с названными веществами на фоне лекарственной терапии, при котором лечебный эффект ряда лекарств снижается. B то же время надо учитывать, что если контакт с индуктором микросомальных ферментов внезапно прекращается, то это может привести к токсическому действию лекарств и потребует уменьшения их доз. Надо также иметь в виду, что, по данным Всемирной организации здравоохранения (ВОЗ), у 2,5% населения значительно повышен риск проявления токсичности лекарств, так как генетически обусловленный период их полураспада в плазме крови у данной группы людей в 3 раза больше среднего. При этом около трети всех описанных у человека ферментов во многих этнических группах представлены различными по своей активности вариантами. Отсюда — индивидуальные различия в реакциях па тот или иной фармакологический агент, зависящие от взаимодействия многих генетических факторов. Так, установлено, что примерно у одного на 1–2 тыс. человек резко снижена активность сывороточной холинэстеразы, которая гидролизует дитилин — средство, применяемое для расслабления скелетной мускулатуры на несколько минут при некоторых хирургических вмешательствах. У таких людей действие дитилина резко удлиняется (до 2 ч и более) и может стать источником тяжелого состояния. Среди людей, живущих в странах Средиземноморья, в Африке и Юго-Восточной Азии, имеется генетически обусловленная недостаточность активности фермента глюкозо-6-фосфат-дегидрогеназы эритроцитов (снижение до 20% от нормы). Эта особенность делает эритроциты малоустойчивыми к ряду медикаментов: сульфаниламидам, некоторым антибиотикам, фенацетину. Вследствие распада эритроцитов у таких лиц на фоне лекарственного лечения возникают гемолитическая анемия и желтуха. Совершенно очевидно, что профилактика этих осложнений должна заключаться в предварительном определении активности соответствующих ферментов у больных. Хотя приведенный материал лишь в общих чертах дает представление о проблеме биотрансформации токсичных веществ, он показывает, что организм человека обладает многими защитными биохимическими механизмами, которые в определенной степени предохраняют его от нежелательного воздействия этих веществ, по крайней мере — от небольших их доз. Функционирование такой сложной барьерной системы обеспечивается многочисленными ферментными cруктурами, активное влияние на которые дает возможность изменять течение процессов превращения и обезвреживания ядов. Но это уже — одна из следующих наших тем. При дальнейшем изложении мы будем еще возвращаться к рассмотрению отдельных аспектов превращения в организме некоторых токсичных веществ в той мере, в какой это необходимо для понимания молекулярных механизмов их биологического действия.Биологические особенности организма, влияющие на токсический процесс
Какие же внутренние факторы, т. е. относящиеся к организму человека и животных как к объекту токсического воздействия, определяют возникновение, течение и последствия отравлений? Прежде всего надо назвать видовые различия чувствительности к ядам, которые в конечном счете оказывают влияние на возможности переноса на человека экспериментальных данных, полученных в опытах на животных. Например, собаки и кролики могут переносить атропин в дозе, превосходящей в 100 раз дозу, смертельную для человека. С другой стороны, есть яды, обладающие более сильным действием на отдельные виды животных, чем на человека. К ним относится синильная кислота, окись углерода и др. Животные, занимающие более высокое положение в эволюционном ряду, как правило, чувствительнее к большинству нейротропных, т. е. действующих преимущественно на нервную систему, химических соединений. Так, результаты опытов, приведенные К. С. Шадурским,[32] свидетельствуют, что большие одинаковые дозы некоторых ФОС на морских свинок действуют в 4 раза сильнее, чем на мышей, и в сотни раз сильнее, чем на лягушек. В то же время к малым дозам тетраэтилсвинца — яда, также поражающего центральную нервную систему, более чувствительны крысы, чем кролики, а последние более чувствительны к эфиру, чем собаки.[33] Можно полагать, что эти различия определяются прежде всего биологическими особенностями, присущими животным каждого вида: степенью развития отдельных систем, их компенсаторными механизмами и возможностями, а также интенсивностью и характером обменных процессов, в том числе биотрансформации чужеродных веществ. Такой подход, к примеру, позволяет биохимически оценить факт устойчивости кроликов и других животных к большим дозам атропина. Оказалось, что их кровь содержит эстеразу, которая гидролизует атропин и отсутствует у человека. В отношении человека в практическом плане принято считать, что в целом он более чувствителен к химическим веществам, нежели теплокровные животные. В этой связи несомненный интерес представляют результаты опытов на добровольцах (врачах одного из московских медицинских институтов). Эти опыты показали, что человек в 5 раз чувствительнее морских свинок и кроликов и в 25 раз чувствительнее крыс к токсическому действию соединений серебра. К таким веществам, как мускарин, героин, атропин, морфин, человек оказался в десятки раз чувствительнее лабораторных животных. Действие же некоторых ФОС на человека и животных различалось мало.[34] При детальном изучении картины отравления было выявлено, что и многие признаки воздействия одного и того же вещества на особей разных видов подчас существенно разнятся. На собак, к примеру, морфий оказывает наркотическое действие, как и на человека, а у кошек это вещество вызывает сильное возбуждение и судороги. С другой стороны, бензол, вызывая у кроликов, как и у человека, угнетение кроветворной системы, у собак не приводит к таким сдвигам. Здесь надо отметить, что даже ближайшие к человеку представители животного мира — обезьяны — значительно отличаются от него по реакции на яды и лекарственные препараты. Вот почему эксперименты на животных (в том числе — высших) по изучению действия лекарств и других чужеродных веществ не всегда дают основания для определенных суждений о возможном их влиянии на организм человека. Иной вид различий течения интоксикаций определяется особенностями пола. Изучению этого вопроса было посвящено большое количество экспериментальных и клинических наблюдений. И хотя в настоящее время не складывается впечатления, что половая чувствительность к ядам имеет какие-то общие закономерности, в общебиологическом плане принято считать, что женский организм более устойчив к действию различных вредоносных факторов внешней среды. Согласно экспериментальным данным,[35] к воздействию окиси углерода, ртутя, свинца, наркотическим и снотворным веществам более устойчивы самки животных, в то время как самцы устойчивое самок к ФОС, никотину, стрихнину, некоторым мышьяковистым соединениям. При объяснении такого рода явлений надо учитывать по крайней мере 2 фактора. Первый — это существенные различия особей разного пола в скорости биотрансформации ядовитых веществ в клетках печени. Не следует забывать, что в итоге этих процессов в организме могут образовываться еще более токсичные соединения и именно они могут в конечном счете определять быстроту наступления, силу и последствия токсического эффекта. Вторым фактором, определяющим неодинаковое реагирование животных разного пола на одни и те же яды, надо считать биологическую специфику мужских и женских половых гормонов. Их роль в формировании устойчивости организма к вредным химическим агентам внешней среды подтверждается, например, таким фактом: у неполовозрелых особей различия в чувствительности к ядам между самцами и самками практически отсутствуют и начинают проявляться лишь при достижении ими половой зрелости. Об этом же свидетельствует и следующий пример: если самкам крыс вводить мужской половой гормон тестостерон, а самцам — женский половой гормон эстрадиол, то самки начинают реагировать на некоторые яды (например, наркотики) как самцы, и наоборот. Клинико-гигиенические и экспериментальные данные свидетельствуют о более высокой чувствительности к ядам детей, чем взрослых, что принято объяснять своеобразием нервной и эндокринной систем детского организма, особенностями вентиляции легких, процессов всасываемости в желудочно-кишечном тракте, проницаемости барьерных структур и др. Но все же, как и для понимания причин половых различий в чувствительности к ядам, надо прежде всего иметь в виду низкую активность биотрансформационных печеночных ферментов организма ребенка, из-за чего он хуже переносит такие яды, как никотин, алкоголь, свинец, сероуглерод, а также сильнодействующие лекарства (например, стрихнин, алкалоиды опия) и многие другие вещества, которые обезвреживаются главным образом в печени. Но к некоторым токсичным химическим агентам дети (равно как и животные раннего возраста) оказываются даже более устойчивыми, чем взрослые. К примеру, в силу меньшей чувствительности к кислородному голоданию дети до 1 года более резистентны к действию окиси углерода — яду, блокирующему кислород — передающую функцию крови. К этому надо добавить, что и у разных возрастных групп животных также определяются существенные различия чувствительности по отношению ко многим токсичным веществам. Так, Г. Н. Красовский и Г. Г. Авилова в упомянутой выше работе отмечают, что молодые и новорожденные особи более чувствительны к сероуглероду и нитриту натрия, в то время как взрослые и старые — к дихлорэтану, фтору, гранозану.Последствия воздействия ядов на организм
Уже накоплено много данных, свидетельствующих о развитии различных болезненных состояний спустя длительные сроки после воздействия на организм тех или иных ядовитых веществ. Так, в последние годы все большее значение в возникновении заболеваний сердечнососудистой системы, в частности атеросклероза, придается сероуглероду, свинцу, окиси углерода, фторидам. Особо опасным следует считать бластомогенный, т. е. вызывающий развитие опухолей, эффект некоторых веществ. Эти вещества, получившие название канцерогенов,[36] встречаются как в воздухе промышленных предприятий, так и населенных пунктов и жилых помещений, в водоемах, почве, продуктах питания, растениях. Распространенными среди них являются полициклические ароматические углеводороды, азосоединения, ароматические амины, нитрозоамины, некоторые металлы, соединения мышьяка. Так, в недавно вышедшей в русском переводе книге американского исследователя Экхольма[37] приводятся случаи канцерогенного действия ряда веществ на промышленных предприятиях США. Например, у людей, работающих с мышьяком на медных, свинцовых и цинковых плавильных заводах без достаточной техники безопасности, наблюдается особенно высокий процент рака легких. Жители близлежащих мест также чаще обычного болеют раком легких, по-видимому, от того, что они вдыхают рассеянный в воздухе мышьяк и другие вредные вещества, которые содержатся в выбросах этих заводов. Однако, как отмечает автор, за последние 40 лет владельцами предприятий не были введены какие-либо меры предосторожности при контакте рабочих с канцерогенными ядами. Все это в еще большей степени относится к горнякам на урановых рудниках и рабочим красильного производства. Естественно, что для профилактики профессиональных злокачественных новообразований прежде всего необходимо изъятие канцерогенов из производства и замена их веществами, не обладающими бластомогенной активностью. Там же, где это невозможно, наиболее правильным решением, способным гарантировать безопасность их применения, является установление их ПДК. Одновременно в нашей стране ставится задача резкого ограничения содержания таких веществ в биосфере до количеств, значительно меньших ПДК. Делаются также попытки воздействия на канцерогены и токсичные продукты их превращений в организме с помощью специальных фармакологических средств. Одним из опасных отдаленных последствий некоторых интоксикаций являются различные пороки развития и уродства, наследственные болезни и т. п., что зависит как от непосредственного влияния яда на половые железы (мутагенное действие), так и от расстройства внутриутробного развития плода. К веществам, действующим в этом направлении, токсикологи относят бензол и его производные, этиленимин, сероуглерод, свинец, марганец и другие промышленные яды, а также отдельные ядохимикаты. В этой связи должен быть назван и печально известный лекарственный препарат талидомид, который в качестве успокаивающего средства применяли в ряде западных стран беременные женщины и который стал причиной уродств для нескольких тысяч новорожденных. Еще одним примером такого рода является скандал, разыгравшийся в 1964 г. в США вокруг препарата под названием «Мер-29», который усиленно рекламировался как средство профилактики атеросклероза и сердечно-сосудистых заболеваний и которым воспользовались свыше 300 тыс. пациентов. В последующем обнаружилось, что «Мер-29» при длительном приеме приводил у многих людей к тяжелым заболеваниям кожи, облысению, снижению остроты зрения и даже слепоте. Концерн «У. Меррел и Ко», производитель этого лекарства, был оштрафован на 80 тыс. долларов, в то время как за 2 года препарат «Мер-29» был продан на сумму в 12 млн. долларов.[38] И вот спустя 16 лет, в начале 1980 г. этот концерн снова на скамье подсудимых. Ему предъявлен иск на 10 млн. долларов в качестве компенсации за многочисленные случаи уродств у новорожденных в США и Англии, матери которых принимали против тошноты на ранней стадии беременности лекарство под названием бендектин. Вопрос об опасности этого препарата впервые был поднят в медицинских кругах в начале 1978 г., однако фармацевтические предприятия продолжают производить бендектин, приносящий их хозяевам большие прибыли.ГЛАВА 2 Антидоты — специфические средства борьбы с отравлениями
В литературе подчас встречаются противоречивые толкования понятия «антидот».[39] Однако современное его значение, по мнению большинства авторов, должно включать: а) вещества, инактивирующие яды посредством прямого химического (или физико-химического) взаимодействия с ними в организме; б) вещества, устраняющие последствия воздействия ядов на биологические структуры. Но являясь однозначным, этот ответ на вопрос, что такое антидот, основывается на следующем, известном в токсикологии в течение многих лет определении: «Противоядием (оно называется по традиции также антидотом, т. е. даваемым против) называется лекарство, применяемое при лечении отравлений, т. е. нарушений здоровья, вызываемых вредным воздействием какого-либо химического агента (яда), и способствующее либо обезвреживанию последнего, либо предупреждению и устранению токсического эффекта».[40] Итак, применяя антидоты, стремятся, с одной стороны, при помощи специальных химических препаратов воспрепятствовать действию ядов на организм, а с другой — нормализовать или по крайней мере затормозить развивающиеся при этом неблагоприятные функциональные сдвиги в различных органах и системах. Понятно, что чем большее распространение будут иметь сведения о сущности действия и способах применения противоядий, тем более успешными станут мероприятия по предотвращению отравлений и ликвидации их последствий. Справедливость этих слов можно проиллюстрировать хотя бы такими примерами. Известно, что глюкоза инактивирует проникшую в организм синильную кислоту и ее соли. В определенных условиях такое широко распространенное вещество, как питьевая сода, может также стать противоядием, поскольку обезвреживает некоторые кислоты. Не зная этого, трудно рассчитывать на успех в оказании помощи при отравлениях названными ядами, даже если под рукой окажутся сахар и сода.Из истории антидотов
Появлению эффективных противоядий предшествовал долгий путь исканий многих поколений человечества. Естественно, что начало этого пути связано с тем временем, когда людям стали известны яды. В Древней Греции существовало убеждение, что против любого яда должно применяться свое противоядие. Этот принцип, одним из авторов которого был Гиппократ, поддерживался и другими выдающимися представителями медицины в течение многих веков, хотя, конечно, в химическом смысле тогда не существовало каких-либо оснований для таких утверждений. Тем не менее признание представителями древней медицины за противоядиями особо специфических целебных свойств само по себе является примечательным, ибо в дальнейшем отдельные антидоты стали наделять многими свойствами. Так, в книге Никандра из Колофана (185–135 гг. до н. э.) под названием «Алексифармака» можно уже встретить упоминание о подобных антидотах. Примерно к этому времени надо отнести и знаменитый антидот понтийского царя Митридата VI Эвпатора (120–63 гг. до н. э.), состоявший из 54 частей. Он включал опий, различные растения, высушенные и растертые в порошок части тела змеи. Имеются свидетельства, что Митридат принимал свой антидот ежедневно малыми дозами чтобы выработать невосприимчивость к отравлениям любыми ядами.[41] Впоследствии на его основе было создано другое универсальное противоядие под названием «терьяк», которое в течение многих веков применялось в разных странах для лечения отравленных, хотя обладало только успокаивающим и болеутоляющим действием. Описание универсального противоядия есть и у Плиния Второго (23–73 гг. н. э.). Таким противоядием он считал молоко. Во II–I веках до н. э. при дворах некоторых царей специально изучали действие ядов на организм, причем сами монархи не только проявляли интерес к этим исследованиям, но иногда даже принимали в них личное участие. Объясняется это тем, что в те времена яды нередко применялись для убийств прежде всего с политическими целями. В частности, для этого использовали змей, укус которых рассматривался как кара богов. Так, например, царь Митридат и его придворный врач ставили опыты над приговоренными к смерти людьми, которых они подвергали укусам ядовитых змей и на которых испытывали различные способы лечения. Впоследствии она составили «Тайные мемуары» о ядах и противоядиях, которые тщательно охранялись. В 66 г. до н. э. эти мемуары были захвачены римским полководцем Помпеем и по его приказу переведены на латинский язык.[42] Но, пожалуй, наиболее интересные сведения о противоядиях содержатся в произведении выдающегося врача античной эпохи Клавдия Галена (129–199 гг. н. э.), которое так и называлось — «Антидоты». В нем Гален приводит список важнейших из существовавших тогда противоядий, которые затем в течение почти двух веков находили практическое применение. Гален считал, что применение лекарств, в том числе противоядий, должно в основном соответствовать принципу «противоположное противоположным». Так, он различал охлаждающие, согревающие и вызывающие гниение яды, а в качестве противоядия рекомендовал вещества, восстанавливающие нарушенное в организме равновесие. Например, при отравлении опием, считавшимся охлаждающим ядом, рекомендовались согревающие процедуры. Надо отметить, что в первом тысячелетии н. э. наука о ядах и противоядиях мало продвинулась вперед. В сочинениях этой эпохи можно найти взгляды и предписания античных авторов, например Галена, Никандра из Колофана, множество рекомендаций, основанных на религиозных представлениях и схоластических умозаключениях. В частности, в те времена и вплоть до Средних веков и эпохи Возрождения упорно поддерживалась вера в единый механизм (принцип) действия ядов, а значит и в то, что побеждены они могут быть только универсальными антидотами. Одним из веществ такого рода длительно считался безоар — измельченный желчный камень, извлекавшийся у жвачных животных и нашедший широкое применение в качестве противоядия наружного и внутреннего использования при различных отравлениях и заболеваниях. Увлечение идеей создания противоядия многостороннего действия продолжалось и в более позднюю эпоху, что видно на примере антидота Маттиомуса (1618 г.), включавшего около 250 компонентов. В медицинских книгах XVII и XVIII вв. все еще можно было найти упоминания о безоаре и других подобных антидотах как о чудесных и верных средствах против всех ядов и заразных болезней. Еще в древности широко было распространено требование к противоядиям (как, впрочем, и к лекарствам вообще) как к средствам, способствующим изгнанию яда из организма или притягивающим его к себе. Считалось также, что эти вещества должны возбуждать соответствующие функции организма с целью скорейшего освобождения его от токсичного агента. Поэтому с давних времен высоко ценились лекарства, вызывавшие рвоту, понос, усиленное мочеотделение, потоотделение, слюноотделение.[43] Надо сказать, что и до настоящего времени рвотные, слабительные и мочегонные средства играют немалую роль в лечебных мероприятиях по удалению ядовитых веществ из организма. Для раннего средневековья наиболее ценным с точки зрения практических рекомендаций по борьбе с отравлениями следует признать знаменитый «Канон врачебной науки» Абу-Али Ибн-Сины (Авиценны) (980–1037 гг.), созданный в период с 1012 по 1023 г. В нем описано 812 лекарств растительного, животного и минерального происхождения и среди них немало противоядий. Вообще Ибн-Сина придавал противоядиям большое значение. В то время на Востоке были распространены умышленные отравления, в особенности посредством подмешивания яда к пище. Поэтому в «Каноне» даются специальные советы, как уберечься от яда, и подчеркивается, что попадание яда в пищеварительный тракт после еды облегчает течение отравлений. В «Каноне» приводится немало конкретных советов по применению противоядий при различных интоксикациях.[44] Например, отравленным солями предписывалось молоко и масло, а отравленным железными опилками и окалиной — магнитный железняк, который, как тогда считалось, собирает рассеивающиеся в организме железо и другие металлы. Особое место в сочинениях Ибн-Сины занимает описание укусов ядовитых членистоногих и змей и способов борьбы с их последствиями. Не оставил он без внимания и кишечные отравления, в частности ядовитыми грибами и испорченным мясом. В качестве противоядий Ибн-Сина рекомендовал антидот Митридата, а также инжир, цитварный корень, терьяк, вино. В начале XII в. на Востоке получило известность сочинение одного из последователей Ибн-Сины — Зайнуддина Джурджани под названием «Сокровище Хорезмшаха», написанное на таджикском языке (фарси). Это многотомный труд, который содержит большое число оригинальных сведений о характере и механизмах действия различных токсических веществ, о способах лечения отравлений. Что касается противоядий, то Джурджани описывает в основном те из них, которые упоминались еще античными авторами. Немало рекомендаций по наиболее рациональному использованию противоядий приводится в другом средневековом медицинском трактате, известном под названием «Салернский кодекс здоровья» и составленном Арнольдом из Виллановы (1235–1311 гг.).[45] Это замечательное произведение содержит множество медицинских рекомендаций по борьбе с отравлениями, изложенных в стихотворной форме. Вообще слова «яд» и «противоядие» довольно часто употребляются в «Кодексе». Вот только 2 примера:Яд и противоядие — фармакологические антагонисты
Совершенно очевидно, что прямое или опосредованное взаимодействие противоядия и токсичного вещества в организме должно носить антагонистический характер. Точнее говоря, антидотный эффект в его фармакологическом значении является результатом такого совместного действия веществ, которое выражается в полном или частичном ослаблении биологической активности одного вещества другим. В последнее время в области изучения интимных механизмов антагонизма различных веществ достигнуты определенные успехи. Мы рассмотрим некоторые основные положения теории антагонистических отношений биологически активных химических агентов в той мере, в какой это необходимо для понимания молекулярных основ действия антидотов.[59] Вначале надо отметить, что термин «антагонизм» в токсикологическом смысле имеет собирательное значение. Во-первых, взаимоотношения яда и антидота могут основываться на физическом, точнее — физико-химическом, антагонизме, который проявляется главным образом адсорбцией ядов такими веществами, как например активированный уголь. Будучи фармакологически инертными препаратами, сорбентные антидоты реализуют свое действие в основном еще до всасывания ядов в кровь за счет неспецифической фиксации их молекул. Тем самым ослабляется токсический эффект из-за уменьшения концентрации молекул яда в биофазе — среде, непосредственно окружающей биоструктуры. Подобным образом действуют окись цинка, белая глина (каолин),[60] крахмальный клейстер, а также ионообменные смолы — катиониты и аниониты, используемые, например, при отравлениях солями тяжелых металлов, алкалоидами, хлорированными углеводородами. Защитная мощность сорбентов подчас весьма значительна. Например, 1 г активированного угля, принятого внутрь, может связать несколько сотен миллиграммов сулемы или стрихнина. Однако существуют и такие адсорбенты, которые, способны связывать свободно циркулирующие в кровеносном русле атомы тяжелых металлов, микробные токсины, медикаментозные вещества. Одно из таких противоядий — поливинилпирролидон, точнее, его полимерные фракции с молекулярной массой около 12000 следующего строения: Оказалось (и это особенно ценно), что данный препарат не только сорбирует вещества, растворенные в крови, но и освобождает белки плазмы и даже клеток от фиксированных ими частиц ядовитых соединений.[61] Практическое применение нашел водно-солевой раствор поливинилпир-ролидона под названием гемодез.
Далее, яд и антидот могут вступать в химическое взаимодействие, и тогда принято говорить о химическом антагонизме. Следствием этого типа антагонизма являются реакции образования нерастворимых и, как правило, нетоксичных (или малотоксичных) соединений, как это имеет место при упоминавшихся реакциях взаимодействия глюкозы с цианидами или двууглекислой соды с кислотами. Химический антагонизм веществ сопровождается также взаимным подавлением их диссоциации или растворимости. При этом обезвреживание ядов вследствие химической трансформации или связывания их молекул может осуществляться как до их проникновения в кровеносное русло, так и при их циркуляции в нем или даже после фиксации биологической структурой. О нескольких фармакологических агентах, нейтрализующих токсичные вещества за счет простых реакций замещения и двойного обмена, уже шла речь в связи с историей противоядий. Вот еще иллюстрация данного аптидотного механизма:
AgNO3+NaCl→NaNO3+AgCl↓.
Из этой реакции следует, что поваренная соль является противоядием при интоксикации (передозировке) нитратом серебра.[62] Таков же принципиальный механизм действия и комбинированных препаратов, например антидота против мышьяка (antidotum arsenici), содержащего сульфат железа и окись магния. Сюда должны быть причислены дитиоловые противоядия и комплексоны, антидотное действие которых основано также на реакциях замещения и двойного обмена и о которых речь подробно пойдет в дальнейшем. В данной подгруппе антидотов имеются вещества, химически связывающие целые молекулы или биологически активные радикалы ядов с превращением в безвредные недиссоциирующие соединения, а также необратимо трансформирующие яды с образованием нетоксичных или значительно менее токсичных соединений. Это, в частности, реализуется посредством гидролитических и окислительно-восстановительных реакций. Так, многие ФОС быстро гидролизуются в щелочной среде:
Оказалось (и это особенно ценно), что данный препарат не только сорбирует вещества, растворенные в крови, но и освобождает белки плазмы и даже клеток от фиксированных ими частиц ядовитых соединений.[61] Практическое применение нашел водно-солевой раствор поливинилпир-ролидона под названием гемодез.
Далее, яд и антидот могут вступать в химическое взаимодействие, и тогда принято говорить о химическом антагонизме. Следствием этого типа антагонизма являются реакции образования нерастворимых и, как правило, нетоксичных (или малотоксичных) соединений, как это имеет место при упоминавшихся реакциях взаимодействия глюкозы с цианидами или двууглекислой соды с кислотами. Химический антагонизм веществ сопровождается также взаимным подавлением их диссоциации или растворимости. При этом обезвреживание ядов вследствие химической трансформации или связывания их молекул может осуществляться как до их проникновения в кровеносное русло, так и при их циркуляции в нем или даже после фиксации биологической структурой. О нескольких фармакологических агентах, нейтрализующих токсичные вещества за счет простых реакций замещения и двойного обмена, уже шла речь в связи с историей противоядий. Вот еще иллюстрация данного аптидотного механизма:
AgNO3+NaCl→NaNO3+AgCl↓.
Из этой реакции следует, что поваренная соль является противоядием при интоксикации (передозировке) нитратом серебра.[62] Таков же принципиальный механизм действия и комбинированных препаратов, например антидота против мышьяка (antidotum arsenici), содержащего сульфат железа и окись магния. Сюда должны быть причислены дитиоловые противоядия и комплексоны, антидотное действие которых основано также на реакциях замещения и двойного обмена и о которых речь подробно пойдет в дальнейшем. В данной подгруппе антидотов имеются вещества, химически связывающие целые молекулы или биологически активные радикалы ядов с превращением в безвредные недиссоциирующие соединения, а также необратимо трансформирующие яды с образованием нетоксичных или значительно менее токсичных соединений. Это, в частности, реализуется посредством гидролитических и окислительно-восстановительных реакций. Так, многие ФОС быстро гидролизуются в щелочной среде:
 Вот почему при попадании ФОС на кожу и слизистые оболочки в качестве противоядий рекомендуют использовать растворы щелочей.
Определенное значение имеет обезвреживание яда за счет реакций окисления, что можно видеть на примере взаимодействия гидразина с перекисью водорода:
N2H2+2Н2O2→N2+4Н2O.
Однако в присутствии уксусной кислоты перекись водорода действует как восстановитель, что используется при отравлениях перманганатом калия:[63]
2КМnO4+5Н2O2+6СН3CООН→2Мn(СН3СОО)2+2СН3СООК+3Н2О+5O.
В то же время КМnO4 применяют при отравлении различными органическими соединениями для окисления их в менее токсичные вещества (например, морфин окисляется в малотоксичный оксиморфин). К разбираемым антидотам надо отнести и органические кислоты (лимонную, уксусную, виннокаменную и др.), которые в малых концентрациях целесообразно применять при отравлениях щелочами. В свою очередь, и щелочные реагенты — жженая магнезия, углекислые соли, в частности мел (СаСО3), — рекомендуются как противоядия, нейтрализующие в организме кислоты. Можно назвать еще несколько практически значимых химических противоядий, превращающих яды в малорастворимые соединения: танин,[64] связывающий алкалоиды и некоторые соли (например, цинка) с образованием нетоксичных таннатов; сульфат меди, осаждающий фосфор; хлорид кальция, переводящий растворимые соли фтора в осадок. Учитывая принципиальное сходство механизма действия сорбентных и химических противоядий (непосредственное взаимодействие с ядом), целесообразно их рассматривать как одну группу, объединив названием антидотыпрямого действия.
И наконец, принципиально иной и значительно более сложный тип антагонизма яда и антидота наблюдается тогда, когда они взаимодействуют не прямо, а косвенно, через различные биоструктуры, оказывая на них стимулирующее или угнетающее действие. Такой антагонизм называется функциональным. Прежде чем раскрыть сущность данного явления, необходимо охарактеризовать те элементы клеток, с которыми взаимодействуют яды и антидоты вследствие своей структурной специфичности. В этой связи важнейшим является понятие «клеточные рецепторы» или просто «рецепторы». В молекулярной токсикологии ими принято называть компоненты белковых, мукополисахаридных или липидных молекул, которые расположены внутри или на поверхности клеток и которые способны взаимодействовать с токсичным агентом или антидотом, вызывая специфический эффект. Часто понятие «рецептор» отождествляется с активными центрами ферментов, т. е. функциональными группировками атомов, непосредственно реагирующими с молекулами биологически активных веществ.[65] Следовательно, токсикологическое (фармакологическое) значение слова «рецептор» отличается от физиологического, которое, как известно, определяет рецепторы как составной элемент нервной системы, воспринимающий раздражение.
Как подчеркнул профессор И. В. Комиссаров, для понимания молекулярного механизма фармакологического эффекта необходимо разграничивать понятия «рецептор», «рецепторная биохимическая структура» и «реактивная биохимическая система», имея в виду, что каждое предыдущее относится к последующему как часть к целому: если рецептор — это субмолекулярное образование, то структура — понятие молекулярного порядка (рецепторный белок), а реактивная биохимическая система включает ряд белковых и небелковых молекул, через которые реализуются взаимосвязанные ферментно-химические процессы. Не касаясь различных сложных, подчас противоречивых и недостаточно изученных сторон существа функционального антагонизма комбинирующихся в организме веществ, отметим зависимость конечного эффекта от соотношения доз яда и антидота, а также от числа и функционального состояния тех рецепторов (структур), которые являются объектом их воздействия.[66]
Один из видов функционального антагонизма для токсикологии имеет особое значение. Это — конкурентный антагонизм при взаимодействии яда и антидота с одними и теми же рецепторами клеток, что приводит (в зависимости от их концентрации) к определенному эффекту, свойственному одному из этих комбинирующихся в организме веществ. Отсюда следует, что сущность конкурентного антагонизма состоит именно в том, что присутствие в организме антагониста уменьшает число рецепторов, способных взаимодействовать с агонистом (в нашем примере — с токсичным фармакологическим агентом), а его итогом, как правило, является противоположное по направлению действие яда и антидота на одни и те же клеточные элементы. Иной характер взаимоотношений яда и антидота можно видеть на примере так называемого независимого антагонизма.[67] О нем принято говорить тогда, когда яд и антидот действуют на разные клеточные элементы или на функционально различные и самостоятельные рецепторные биохимические структуры одних и тех же клеток и тем самым стимулируют или тормозят те или иные физиологические функции.
Интерес токсикологов проявляется еще к одному виду функционального антагонизма, известному под названием неконкурентного антагонизма. Считается, что 2 вещества — яд и антидот — неконкурентно действуют на биохимическую рецепторную структуру, если они реагируют с достаточно удаленными друг от друга, но взаимозависимыми ее функциональными группами (рецепторами). В том случае, когда данная структура представлена ферментом, одно из комбинирующихся веществ взаимодействует с его активным центром (центрами), а другое — с участком фермента вне активного центра. Последний называют аллостерическим в отличие от изостерического, который включает активные центры фермента. Воздействуя на аллостерический участок рецепторной структуры, антидот может изменять функциональные свойства активного центра и благодаря этому влиять на прочность его связи с молекулой яда. С точки зрения возможного применения антидотов, естественно, наибольший интерес представляет такое неконкурентное взаимодействие двух веществ, которое приводит к ослаблению или подавлению эффекта одного из них. Таким образом, различные виды функционального антагонизма взаимодействующих в организме химических веществ дают основание рассматривать как особую группу такие антидоты, специфический эффект которых проявляется без непосредственного их контакта с ядом. Поэтому вполне будет оправдано их объединение под общим названием антидоты непрямого действия.
Вот почему при попадании ФОС на кожу и слизистые оболочки в качестве противоядий рекомендуют использовать растворы щелочей.
Определенное значение имеет обезвреживание яда за счет реакций окисления, что можно видеть на примере взаимодействия гидразина с перекисью водорода:
N2H2+2Н2O2→N2+4Н2O.
Однако в присутствии уксусной кислоты перекись водорода действует как восстановитель, что используется при отравлениях перманганатом калия:[63]
2КМnO4+5Н2O2+6СН3CООН→2Мn(СН3СОО)2+2СН3СООК+3Н2О+5O.
В то же время КМnO4 применяют при отравлении различными органическими соединениями для окисления их в менее токсичные вещества (например, морфин окисляется в малотоксичный оксиморфин). К разбираемым антидотам надо отнести и органические кислоты (лимонную, уксусную, виннокаменную и др.), которые в малых концентрациях целесообразно применять при отравлениях щелочами. В свою очередь, и щелочные реагенты — жженая магнезия, углекислые соли, в частности мел (СаСО3), — рекомендуются как противоядия, нейтрализующие в организме кислоты. Можно назвать еще несколько практически значимых химических противоядий, превращающих яды в малорастворимые соединения: танин,[64] связывающий алкалоиды и некоторые соли (например, цинка) с образованием нетоксичных таннатов; сульфат меди, осаждающий фосфор; хлорид кальция, переводящий растворимые соли фтора в осадок. Учитывая принципиальное сходство механизма действия сорбентных и химических противоядий (непосредственное взаимодействие с ядом), целесообразно их рассматривать как одну группу, объединив названием антидотыпрямого действия.
И наконец, принципиально иной и значительно более сложный тип антагонизма яда и антидота наблюдается тогда, когда они взаимодействуют не прямо, а косвенно, через различные биоструктуры, оказывая на них стимулирующее или угнетающее действие. Такой антагонизм называется функциональным. Прежде чем раскрыть сущность данного явления, необходимо охарактеризовать те элементы клеток, с которыми взаимодействуют яды и антидоты вследствие своей структурной специфичности. В этой связи важнейшим является понятие «клеточные рецепторы» или просто «рецепторы». В молекулярной токсикологии ими принято называть компоненты белковых, мукополисахаридных или липидных молекул, которые расположены внутри или на поверхности клеток и которые способны взаимодействовать с токсичным агентом или антидотом, вызывая специфический эффект. Часто понятие «рецептор» отождествляется с активными центрами ферментов, т. е. функциональными группировками атомов, непосредственно реагирующими с молекулами биологически активных веществ.[65] Следовательно, токсикологическое (фармакологическое) значение слова «рецептор» отличается от физиологического, которое, как известно, определяет рецепторы как составной элемент нервной системы, воспринимающий раздражение.
Как подчеркнул профессор И. В. Комиссаров, для понимания молекулярного механизма фармакологического эффекта необходимо разграничивать понятия «рецептор», «рецепторная биохимическая структура» и «реактивная биохимическая система», имея в виду, что каждое предыдущее относится к последующему как часть к целому: если рецептор — это субмолекулярное образование, то структура — понятие молекулярного порядка (рецепторный белок), а реактивная биохимическая система включает ряд белковых и небелковых молекул, через которые реализуются взаимосвязанные ферментно-химические процессы. Не касаясь различных сложных, подчас противоречивых и недостаточно изученных сторон существа функционального антагонизма комбинирующихся в организме веществ, отметим зависимость конечного эффекта от соотношения доз яда и антидота, а также от числа и функционального состояния тех рецепторов (структур), которые являются объектом их воздействия.[66]
Один из видов функционального антагонизма для токсикологии имеет особое значение. Это — конкурентный антагонизм при взаимодействии яда и антидота с одними и теми же рецепторами клеток, что приводит (в зависимости от их концентрации) к определенному эффекту, свойственному одному из этих комбинирующихся в организме веществ. Отсюда следует, что сущность конкурентного антагонизма состоит именно в том, что присутствие в организме антагониста уменьшает число рецепторов, способных взаимодействовать с агонистом (в нашем примере — с токсичным фармакологическим агентом), а его итогом, как правило, является противоположное по направлению действие яда и антидота на одни и те же клеточные элементы. Иной характер взаимоотношений яда и антидота можно видеть на примере так называемого независимого антагонизма.[67] О нем принято говорить тогда, когда яд и антидот действуют на разные клеточные элементы или на функционально различные и самостоятельные рецепторные биохимические структуры одних и тех же клеток и тем самым стимулируют или тормозят те или иные физиологические функции.
Интерес токсикологов проявляется еще к одному виду функционального антагонизма, известному под названием неконкурентного антагонизма. Считается, что 2 вещества — яд и антидот — неконкурентно действуют на биохимическую рецепторную структуру, если они реагируют с достаточно удаленными друг от друга, но взаимозависимыми ее функциональными группами (рецепторами). В том случае, когда данная структура представлена ферментом, одно из комбинирующихся веществ взаимодействует с его активным центром (центрами), а другое — с участком фермента вне активного центра. Последний называют аллостерическим в отличие от изостерического, который включает активные центры фермента. Воздействуя на аллостерический участок рецепторной структуры, антидот может изменять функциональные свойства активного центра и благодаря этому влиять на прочность его связи с молекулой яда. С точки зрения возможного применения антидотов, естественно, наибольший интерес представляет такое неконкурентное взаимодействие двух веществ, которое приводит к ослаблению или подавлению эффекта одного из них. Таким образом, различные виды функционального антагонизма взаимодействующих в организме химических веществ дают основание рассматривать как особую группу такие антидоты, специфический эффект которых проявляется без непосредственного их контакта с ядом. Поэтому вполне будет оправдано их объединение под общим названием антидоты непрямого действия.
Антидоты как лечебные препараты
Еще в 1818 г. Орфила сформулировал четкие требования, которым должно удовлетворять противоядие. Он считал, что это название можно присвоить веществу, обладающему следующими свойствами:[68] 1) необходимо, чтобы его можно было принимать большими дозами без всякой опасности; 2) оно должно действовать на яд, будь то жидкий или твердый, при температуре человеческого тела или еще более низкой; 3) его действие должно быть быстрым; 4) оно должно связываться с ядом в среде желудочного, слизистого, содержащего желчь и других соков, которые могут содержаться в желудке; 5) наконец, действуя на яд, оно должно лишать его вредных свойств. Эти положения в большой степени сохраняют свое значение и в настоящее время. Так, весьма современно звучит требование о необходимости быстрого действия противоядий и об устойчивости их по отношению к пищеварительным сокам. Однако не следует забывать, что во времена Орфила были известны только те антидоты, которые непосредственно реагируют с ядами. Поэтому,. естественно, тогда не учитывались такие новые их свойства, как например способность воздействовать па определенные физиологические функции или защищать биологические структуры от токсического влияния. Надо иметь в виду, что многие современные противоядия — сильнодействующие, а подчас и весьма токсичные синтетические препараты. Следовательно, применение их возможно только в определенных допустимых дозах, и тем из антидотов, которые при прочих равных условиях обладают большой терапевтической широтой, токсикологи отдают предпочтение. К сожалению, большинство быстродействующих современных антидотов разрушается в желудочно-кишечном тракте, что диктует необходимость вводить их в организм парентерально, т. е. посредством подкожных, внутримышечных и внутривенных инъекций, а также в виде вдыхаемого аэрозоля. Понятно, что данное обстоятельство затрудняет применение многих антидотов во внебольничной обстановке. Однако в последнее время созданы специальные приспособления в виде шприцев-тюбиков различных типов, с помощью которых можно вводить антидоты внутримышечно и подкожно в порядке само- и взаимопомощи на производстве и в домашних условиях. Вместе с тем химики-синтетики и токсикологи стремятся создать такие антидотные препараты, которые бы сохраняли свое фармакологическое действие при приеме внутрь. Одним из них является тарен — таблетированный антидот, используемый при интоксикациях фосфорорганическими ядами.ГЛАВА 3 Нервный импульс, яды и противоядия
Все большее распространение получают теперь химические соединения, избирательно воздействующие на функции нервной системы. Это связано, во-первых, с постоянно увеличивающимися возможностями контакта современного человека с большим числом нейротоксических веществ в промышленности и сельском хозяйстве (препараты группы гидразина, ФОС, карбаматы и др.) и, во-вторых, с расширением диапазона применения средств предупреждения и лечения различных нервно-психических расстройств (транквилизаторы, антидепрессанты, наркотики, аналептики и др.). Достоверные научные данные дают основание объединить названные группы веществ одним общим фармакологическим свойством — способностью влиять на передачу нервного импульса. Наиболее демонстративно это иллюстрируется рассмотрением биохимических аспектов действия ФОС и соответствующих антидотов.Фосфорорганические соединения
Синтезированные впервые в конце прошлого века ФОС привлекли к себе особенно пристальное внимание химиков и токсикологов с середины 30-х годов, когда их свойства более тщательно были исследованы из-за неожиданно обнаруженной высокой токсичности. Именно тогда в одной из лабораторий германской фирмы «И. Г. Фарбениндустри» под руководством Шрадера были синтезированы фосфорорганические инсектициды, проявлявшие биологическую активность в очень малых дозах. В дальнейшем в связи с подготовкой фашистской Германии к химической войне эта лаборатория переключилась на работы по созданию высокотоксичных ФОС, предназначенных для военных целей. Там были синтезированы такие известные отравляющие вещества из этого класса, как табун, зарин, зоман. Распространение ФОС обусловлено прежде всего повсеместным их использованием в качестве ядохимикатов. Достаточно назвать в связи с этим такие инсектициды, как хлорофос, фосфамид, карбофос, октаметил. Возрастает и число фосфорорганических медикаментозных средств, используемых в невропатологии, офтальмологии, хирургии (армии, фосфакол, фосарбид и др.). Множество ФОС применяется в химической промышленности, в частности, в качестве исходных и промежуточных продуктов органического синтеза. В нашей стране большие заслуги в синтезе и разработке способов применения ФОС, имеющих народнохозяйственное значение, принадлежат казанской школе химиков-органиков, возглавляемой академиком Б. А. Арбузовым. Обширные исследования были проведены этими учеными в области превращения эфиров кислот трехвалентного фосфора в эфиры фосфоновых кислот. Советскими и зарубежными исследователями были раскрыты и многие другие химические свойства этих веществ. Однако, как справедливо отмечает Франке (ГДР), «развитие химии ФОС отнюдь не завершено. Среди этих соединений можно ожидать появления еще более токсичных веществ. Большие возможности комбинаций, заметное изменение свойств при небольших изменениях строения создают богатое поле деятельности для химиков, фармацевтов, врачей, биологов, физиологов и др.».[69] По своему химическому строению ФОС представляют собою эфиры кислот пятивалентного фосфора (фосфорной, тнофосфорной, фосфоновой и др.). Их общий вид хорошо иллюстрируется следующей структурной формулой: где P — атом фосфора, R1 и R2, как правило, органические радикалы, а X — галоген (Cl, F), или CN-гpуппa, или производное бензола (например, нитрофенол).
Будучи в основном малолетучими жидкостями, ФОС способны проникать во внутренние среды организма через неповрежденную кожу и слизистые оболочки вследствие высокой липидотропности. Источником отравлений могут быть зараженная пища и вода, а также воздух, содержащий пары и аэрозоли ФОС. Однако картина отравления мало зависит от путей поступления ФОС в организм и в основном сводится к нарушениям функции цейтральной нервной системы, а также мышечной, дыхательной, сердечно-сосудистой систем, желудочно-кишечного тракта и органа зрения. У тяжело отравленного быстро появляется беспокойство, чувство страха, возбуждение, судороги. Эти симптомы развиваются на фона приступов удушья и кашля из-за спазма бронхов и обильного выделения секрета бронхиальных желез. Появляются боли в области сердца, расстраивается его ритм, подъем кровяного давления сменяется падением. Возникают боли в животе, спазмируется кишечник, наблюдается понос. Очень характерны изменения со стороны глаз: резко суживается зрачок, появляется слезотечение, нарушается функция зрения, особенно аккомодация, т. е. способность настраивать глаз на ближнее или дальнее видение. При попадании в организм смертельных доз ФОС и несвоевременном или нерациональном лечении быстро развивается обморочное состояние, наступает паралич дыхательного центра, что и является чаще всего непосредственной причиной гибели отравленных.
где P — атом фосфора, R1 и R2, как правило, органические радикалы, а X — галоген (Cl, F), или CN-гpуппa, или производное бензола (например, нитрофенол).
Будучи в основном малолетучими жидкостями, ФОС способны проникать во внутренние среды организма через неповрежденную кожу и слизистые оболочки вследствие высокой липидотропности. Источником отравлений могут быть зараженная пища и вода, а также воздух, содержащий пары и аэрозоли ФОС. Однако картина отравления мало зависит от путей поступления ФОС в организм и в основном сводится к нарушениям функции цейтральной нервной системы, а также мышечной, дыхательной, сердечно-сосудистой систем, желудочно-кишечного тракта и органа зрения. У тяжело отравленного быстро появляется беспокойство, чувство страха, возбуждение, судороги. Эти симптомы развиваются на фона приступов удушья и кашля из-за спазма бронхов и обильного выделения секрета бронхиальных желез. Появляются боли в области сердца, расстраивается его ритм, подъем кровяного давления сменяется падением. Возникают боли в животе, спазмируется кишечник, наблюдается понос. Очень характерны изменения со стороны глаз: резко суживается зрачок, появляется слезотечение, нарушается функция зрения, особенно аккомодация, т. е. способность настраивать глаз на ближнее или дальнее видение. При попадании в организм смертельных доз ФОС и несвоевременном или нерациональном лечении быстро развивается обморочное состояние, наступает паралич дыхательного центра, что и является чаще всего непосредственной причиной гибели отравленных.
Холиеэстераза и ацетилхолин
Согласно существующим представлениям, в основе механизма действия ФОС лежит избирательное торможение ими фермента ацетилхолинэстеразы, или просто холинэстеразы, которая катализирует гидролиз ацетилхолина-химического передатчика (медиатора) нервного возбуждения. Различают 2 типа холинэстеразы: истинную, содержащуюся преимущественно в тканях нервной системы, в скелетной мускулатуре, а также в эритроцитах, и ложную, содержащуюся главным образом в плазме крови, печени и некоторых других органах. Собственно ацетилхолинэстеразой является истинная, или специфическая, холинэстераза, так как только она гидролизует названный медиатор. И именно ее в дальнейшем мы будем обозначать термином «холинэстераза». Поскольку фермент и медиатор являются необходимыми химическими компонентами передачи нервных импульсов в синапсах — контактах между двумя нейронами или окончаниями нейрона и рецепторной клеткой, следует более подробно остановиться на их биохимической роли. Ацетилхолин синтезируется из спирта холина и ацетилкоэнзима А[70] под влиянием фермента холинацетилазы в митохондриях нервных клеток и накапливается в окончаниях их отростков в виде пузырьков диаметром около 50 нм. Предполагается, что каждый такой пузырек содержит несколько тысяч молекул ацетилхолина. При этом в настоящее время принято различать ацетилхолин, готовый к секреции и расположенный в непосредственной близости от активной зоны, и ацетилхолин вне активной зоны, находящийся в состоянии равновесия с первым и не готовый к выделению в сипаптическую щель. Кроме того, имеется еще так называемый стабильный фонд ацетилхолина (до 15%), не освобождающегося даже в условиях блокады его синтеза.[71] Под воздействием нервного возбуждения и ионов Са2+ молекулы ацетилхолина переходят в синаптическую щель — пространство шириною 20–50 нм, отделяющее окончание нервного волокна (пресинаптическую мембрану) от иннервируемой клетки. На поверхности последней расположена постсинаптическая мембрана с холинорецепторами — специфическими белковыми структурами, способными взаимодействовать с ацетилхолином. Воздействие медиатора на холинорецептор приводит к деполяризации (снижению заряда), временному изменению проницаемости постсинаптической мембраны для положительно заряженных ионов Na+ и проникновению их внутрь клетки, что в свою очередь выравнивает потенциал напряжения на ее поверхности (оболочке).[72] Это дает начало новому импульсу в нейроне следующей ступени или вызывает деятельность клеток того или иного органа: мышцы, железы и др. (рис 5). Фармакологические исследования выявили существенную разницу в свойствах холинорецепторов различных синапсов. Рецепторы одной группы, проявляющие избирательную чувствительность к мускарину (яду гриба мухомора), названы мускариночувствительными, или М-холинорецепторами; они представлены главным образом в гладких мышцах глаз, бронхов, желудочно-кишечного тракта, в клетках потовых и пищеварительных желез, в сердечной мышце. Холинорецепторы второй группы возбуждаются малыми дозами никотина и поэтому названы никотино-чувствительными, или Н-холинорецепторами. К ним относятся рецепторы вегетативных ганглиев, скелетных мышц, мозгового слоя надпочечниковых желез, центральной нервной системы.
Рис. 5. Основные структурные элементы и схема функционирования холинергического синапса (Голиков, Фишзон-Рысс, 1978). 1 — синаптические пузырьки; 2 — пресинаптические центры связывания ацетилхолина; 3 — синаптическая щель; 4 — миелиновая оболочка; 5 — митохондрии; 6 — шванновские клетки; ХР — холинорецептор; АХ — ацетил-холин; АХЭ — ацетилхолинэстераза; ХА — холинацетилаза
Молекулы ацетилхолина, выполнившие свою медиаторную функцию, должны быть немедленно инактивированы, в противном случае будет нарушена дискретность в проведении нервного импульса и проявится избыточная функция холинорецептора. Именно это осуществляет холинэстераза, мгновенно гидролизующая ацетилхолин. Каталитическая активность холинэстеразы превышает почти все известные ферменты: по разным данным, время расщепления одной молекулы ацетилхолина составляет около одной миллисекунды, что соизмеримо со скоростью передачи нервного импульса. Осуществление столь мощного каталитического эффекта обеспечивается наличием в молекуле холинэстеразы определенных участков (активных центров), обладающих исключительно хорошо выраженной реакционной способностью по отношению к ацетилхолину.[73] Будучи простым белком (протеином), состоящим только из одних аминокислот, молекула холинэстеразы, как теперь выяснено, исходя из ее молекулярной массы, содержит от 30 до 50 таких активных центров.
Рис. 6. Ферментативный гидролиз ацетилхолина. Объяснение в тексте
Как видно из рис. 6, участок поверхности холинэстеразы, непосредственно контактирующий с каждой молекулой медиатора, включает 2 центра, расположенных на расстоянии 0,4–0,5 мм: анионный, несущий отрицательный заряд, и эстеразный. Каждый из этих центров образован определенными группами атомов аминокислот, составляющих структуру фермента (гидроксилом, карбоксилом и др.). Ацетилхолин благодаря положительно заряженному атому азота (так называемой катионной головки) ориентируется за счет электростатических сил на поверхности холинэстеразы. При этом расстояние между атомом азота и кислотной группой медиатора соответствует расстоянию между активными центрами фермента. Анионный центр притягивает к себе катионную головку ацетилхолина и тем самым способствует сближению его эфирной группировки с эстеразным центром фермента. Затем рвется эфирная связь, ацетилхолин разделяется на 2 части: холиновую и уксусную, остаток уксусной кислоты присоединяется к эстеразному центру фермента и образуется так называемая ацетилирозанная холинэстераза. Этот крайне непрочный комплекс мгновенно подвергается спонтанному гидролизу, что освобождает фермент от остатка медиатора и приводит к образованию уксусной кислоты. С данного момента холииэстераза снова способна выполнять каталитическую функцию, а холин и уксусная кислота становятся исходными продуктами синтеза новых молекул ацетилхолина.Механизм действия фосфорорганических соединений
Многие ФОС вследствие особого химического сродства к холинэстеразе ингибируют, т. е. блокируют, ее молекулы посредством взаимодействия с эстеразным центром. Как это видно из приводимой схемы, молекула фосфорор-ганического яда реагирует с гидроксильной группой фермента, причем анионный его центр участия в реакция не принимает: Однако в начале 50-х годов в Швеции в лаборатории Таммелина были синтезированы такие ФОС, которые реагируют и с анионным центром фермента. При этом химики исходили из предположения, что если яд будет сходен по структуре с естественным субстратом холинэстеразы (ацетилхолином), то он окажет на этот фермент более сильное ингибирующее действие. И действительно, такими мощными антихолинэстеразными веществами оказались соединения, которые содержат в своем составе остаток холина, как например метилфторфосфорилхолин. Совершенно естественно, что при его взаимодействии с холинэстеразой положительно заряженный атом азота будет реагировать с анионным центром фермента. Это обеспечивает дополнительный контакт яда с активной поверхностью холинэстеразы и делает связь между ними более прочной:
Однако в начале 50-х годов в Швеции в лаборатории Таммелина были синтезированы такие ФОС, которые реагируют и с анионным центром фермента. При этом химики исходили из предположения, что если яд будет сходен по структуре с естественным субстратом холинэстеразы (ацетилхолином), то он окажет на этот фермент более сильное ингибирующее действие. И действительно, такими мощными антихолинэстеразными веществами оказались соединения, которые содержат в своем составе остаток холина, как например метилфторфосфорилхолин. Совершенно естественно, что при его взаимодействии с холинэстеразой положительно заряженный атом азота будет реагировать с анионным центром фермента. Это обеспечивает дополнительный контакт яда с активной поверхностью холинэстеразы и делает связь между ними более прочной:
 Можно представить также одномоментное ингибирование одной молекулой метилфторфосфорилхолнна двух молекул фермента: одну по анионному, вторую — по эстеразному центру. Как бы то ни было, яды Таммелина оказались в десятки раз более токсичными, чем даже такое сильнодействующее ФОС, как зарин. Образовавшаяся фосфорилированная холинэстераза в отличие от ацетилированной является соединением достаточно прочным и не подвергается самопроизвольному гидролизу. Оказалось, что процесс ингибирования холинэстеразы является двухэтапным. Вначале, на первом этапе, происходит обратимое, т. е. непрочное, ее блокирование, и лишь на втором этапе наступает необратимое блокирование фермента. Оба эти этапа являются результатом сложной, до конца еще не выясненной молекулярной перестройка в комплексе «ФОС-холинэстераза». Забегая несколько вперед, отметим значимость данного явления для практики применения некоторых антидотов, действие которых заключается в разрыве химической связи между ядом и ферментом. Таким образом, под влиянием антихолинэсте — разных веществ тормозится разрушение молекул ацетилхолина и он продолжает оказывать непрерывное действие на холинорецепторы. Отсюда следует, что отравление ФОС есть не что иное, как генерализованное перевозбуждение холинорецепторов, вызванное интоксикацией эндогенным, т. е. имеющим внутреннее происхождение, ацетилхолином. Вот почему основные симптомы отравления ФОС можно трактовать как проявление избыточной, нецелесообразной для организма деятельности ряда структур и органов, которая обеспечивается ацетилхолиновой медиацией (прежде всего это — функция нервных клеток, поперечнополосатых и гладких мышц, различных желез).
В настоящее время имеются доказательства непосредственного возбуждающего влияния некоторых ФОС на холинорецепторы. Тем самым не исключается, что ФОС оказывают токсический эффект, минуя холинэстеразный механизм:
Можно представить также одномоментное ингибирование одной молекулой метилфторфосфорилхолнна двух молекул фермента: одну по анионному, вторую — по эстеразному центру. Как бы то ни было, яды Таммелина оказались в десятки раз более токсичными, чем даже такое сильнодействующее ФОС, как зарин. Образовавшаяся фосфорилированная холинэстераза в отличие от ацетилированной является соединением достаточно прочным и не подвергается самопроизвольному гидролизу. Оказалось, что процесс ингибирования холинэстеразы является двухэтапным. Вначале, на первом этапе, происходит обратимое, т. е. непрочное, ее блокирование, и лишь на втором этапе наступает необратимое блокирование фермента. Оба эти этапа являются результатом сложной, до конца еще не выясненной молекулярной перестройка в комплексе «ФОС-холинэстераза». Забегая несколько вперед, отметим значимость данного явления для практики применения некоторых антидотов, действие которых заключается в разрыве химической связи между ядом и ферментом. Таким образом, под влиянием антихолинэсте — разных веществ тормозится разрушение молекул ацетилхолина и он продолжает оказывать непрерывное действие на холинорецепторы. Отсюда следует, что отравление ФОС есть не что иное, как генерализованное перевозбуждение холинорецепторов, вызванное интоксикацией эндогенным, т. е. имеющим внутреннее происхождение, ацетилхолином. Вот почему основные симптомы отравления ФОС можно трактовать как проявление избыточной, нецелесообразной для организма деятельности ряда структур и органов, которая обеспечивается ацетилхолиновой медиацией (прежде всего это — функция нервных клеток, поперечнополосатых и гладких мышц, различных желез).
В настоящее время имеются доказательства непосредственного возбуждающего влияния некоторых ФОС на холинорецепторы. Тем самым не исключается, что ФОС оказывают токсический эффект, минуя холинэстеразный механизм:
 В последние 10–15 лет токсикологи все чаще обращают внимание на эту особенность механизма влияния ФОС на биоструктуры. В частности, такое их неантихолинэстеразное действие проявляется в прямом возбуждении Н-холинорецепторов, от чего, как показывают экспериментальные данные, в свою очередь зависят никоти — ноподобные эффекты ФОС. В то же время их мускарино — подобное действие с достаточным основанием теперь рассматривается как результат ингибирования холинэстеразы.
Что касается сравнительной выраженности мускариновых и никотиновых эффектов у различных антихолинэстеразных веществ, то, согласно исследованию В. Б. Прозоровского,[74] можно рассматривать 3 их группы:
1) вызывающие преимущественное возбуждение М-холинорецепторов (эзерин, нибуфин, хлорофос);
2) вызывающие возбуждение как М-, так и Н-холинорецепторов (фосфакол, армин, диизопропилфторфосфат);
3) вызывающие преимущественное воздействие на Н-холинорецепторы (прозерин, тиофос, меркаптофос).
Из изложенного следует, по крайней мере теоретически, что при отравлении антихолинэстеразными ядами, в том числе ФОС, антидотами могли бы быть:
1) вещества, вступающие в прямое химическое взаимодействие с ядами;
2) вещества, тормозящие синтез и выход ацетилхолина в синаптическую щель;
3) вещества, замещающие поврежденный ядами фермент (т. е. препараты холинэстеразы);
4) вещества, препятствующие контакту яда с ферментом и тем самым защищающие его от токсического воздействия;
5) вещества, препятствующие контакту ацетилхолина с холинорецептором;
6) вещества, восстанавливающие активность фермента посредством вытеснения яда с его поверхности (т. е. реактивирующие структуру холинэстеразы).
Многочисленные токсикологические эксперименты показали, что всем этим веществам присуща та или иная степень специфического воздействия на токсический процесс, однако наибольшее практическое значение имеют 2 последние группы противоядий. Рассмотрим подробнее механизмы их действия.
В последние 10–15 лет токсикологи все чаще обращают внимание на эту особенность механизма влияния ФОС на биоструктуры. В частности, такое их неантихолинэстеразное действие проявляется в прямом возбуждении Н-холинорецепторов, от чего, как показывают экспериментальные данные, в свою очередь зависят никоти — ноподобные эффекты ФОС. В то же время их мускарино — подобное действие с достаточным основанием теперь рассматривается как результат ингибирования холинэстеразы.
Что касается сравнительной выраженности мускариновых и никотиновых эффектов у различных антихолинэстеразных веществ, то, согласно исследованию В. Б. Прозоровского,[74] можно рассматривать 3 их группы:
1) вызывающие преимущественное возбуждение М-холинорецепторов (эзерин, нибуфин, хлорофос);
2) вызывающие возбуждение как М-, так и Н-холинорецепторов (фосфакол, армин, диизопропилфторфосфат);
3) вызывающие преимущественное воздействие на Н-холинорецепторы (прозерин, тиофос, меркаптофос).
Из изложенного следует, по крайней мере теоретически, что при отравлении антихолинэстеразными ядами, в том числе ФОС, антидотами могли бы быть:
1) вещества, вступающие в прямое химическое взаимодействие с ядами;
2) вещества, тормозящие синтез и выход ацетилхолина в синаптическую щель;
3) вещества, замещающие поврежденный ядами фермент (т. е. препараты холинэстеразы);
4) вещества, препятствующие контакту яда с ферментом и тем самым защищающие его от токсического воздействия;
5) вещества, препятствующие контакту ацетилхолина с холинорецептором;
6) вещества, восстанавливающие активность фермента посредством вытеснения яда с его поверхности (т. е. реактивирующие структуру холинэстеразы).
Многочисленные токсикологические эксперименты показали, что всем этим веществам присуща та или иная степень специфического воздействия на токсический процесс, однако наибольшее практическое значение имеют 2 последние группы противоядий. Рассмотрим подробнее механизмы их действия.
Атропин и атропиноподобные вещества

Рис. 7. Химическое строение молекулы высокотоксичного ФОС, ацетилхолина и атропина (Gille, 1971). 1 — двойная связь (С=0 или Р=0); 2 — эфирная связь; 3 — алкильная группа у Р- или С-атома; 4 — одинаковое расстояние между центрами действия; 5 — катионная головка молекулы
Антидотный механизм, о котором пойдет речь, состоит в блокировании молекулами противоядий холинорецепторов и в прерывании или тормошении вследствие этого медиаторной функции ацетилхолина. Вещества такого типа действия получили в фармакологии название холиполитиков. Помимо уже знакомого нам атропина в настоящее время находят применение амизил, амедин, бензацин, апрофен, пентафен, тропацин, спазмолитин, мепанит и другие препараты, часть из которых значительно превосходит атропин по силе действия. К тому же атропин блокирует преимущественно М-холинорецепторы и мало влияет на никотиноподобное действие ФОС (т. е. слабо устраняет нарушения в передаче импульса с нерва на мышцу, деятельности сердца, надпочечниковых желез и некоторые другие симптомы). В то же время такие холинолитики, как пентафен, циклодол, динезин, а также ганглиоблокаторы[75] — гексоний, пентамин и др., проявляя антимускариновое действие, одновременно ослабляют никотиноподобные эффекты ФОС. Поэтому при отравлении антихолинэстеразными веществами наиболее рациональным считается комбинированное применение различных холинолитиков. Так, в одной из работ профессора Ю. С. Кагана[76] была показана высокая эффективность комбинации пентафена и мепанита при отравлении животных меркаптофосом — высокотоксичным ингибитором холинэстеразы. Автор учитывал при этом данные, полученные в лаборатории профессора М. Я. Михельсона, о неодинаковом действии на те или иные звенья нервной системы различных холинолитиков, являющихся третичными аминами (пентафен) или имеющими в своем составе четвертичный азот (мепанит). В этой связи следует иметь также в виду результаты опытов, приведенные в уже упомянутой работе В. Б. Прозоровского, который показал, что отравление антихолинэстеразными веществами, преимущественно возбуждающими М-холинорецепторы, легко предупреждается и лечится с помощью одних М-холинолитиков (например, атропином). Если же последние применять при отравлении ядами, действующими главным образом на Н-холинорецепторы, то они оказываются практически неэффективными, а антидот. ный эффект достигается только при использовании Н-холинолитиков (например, пентафена). Эти интересные данные, подтверждающие высокую специфичность холинолитических противоядий, дополняются установленной необходимостью обязательного комбинирования М-холинолитиков с Н-холинолитиками для успешного лечения отравлений веществами, возбуждающими как М-, так и Н-холинорецепторы. В чем же состоит молекулярный механизм действия холинолитических антидотов? Прежде всего надо отметить структурное сходство холинолитиков, в том числе атропина, с ацетилхолином и некоторыми ФОС (рис. 7). Данное обстоятельство, по-видимому, в немалой степени определяет химическое сродство этих противоядий и ряда ФОС к холинорецептору, а также существование конкурентного антагонизма между ними и медиатором за связь с рецептором. При этом в определенных дозах холинолитик проявляет большую способность взаимодействовать с холинорецептором, чем медиатор, и даже может вытеснять последний с холинорецептора. Разумеется, такой антидот будет блокировать и нормально функционирующие холинорецепторы, свободные от избытка ацетилхолина. Вот почему антидоты типа атропина могут применяться не только с лечебной, но и с профилактической целью: предварительное введение животным 1 мл 0,1%-ного водного раствора сульфата атропина (1 мг) внутримышечно или подкожно предотвращает или резко ослабляет отравление антихолинэстеразными веществами.
Рис. 8. Схематичное изображение активного участка холинорецептора (ХР), взаимодействия ацетилхолина с ХР и взаимодействия холинолитического антидота с ХР (Кузнецов, Голиков, 1962). Рецепторная часть ХР (I) построена из двух белковых молекул, на поверх ностях которых существует 2 активных центра, В одном из них — анионном — белковые цепи связаны ионными связями (А---Б), в другом — эстерофильном — водородными (В---Г). Молекула ацетилхолина, взаимодействуя с рецептором (II), присоединяется своим катионным концом к анионному центру, разрывая связь А---Б. Эфирная группировка ацетилхолина соединяется с эстерофильным центром, разрывая водородную связь В---Г В результате в структуре рецепторного белка возникает разрыв, образуется коридор, по которому осуществляется уравнивание концентраций ионов К+ и Na+ снаружи и внутри клетки, нервный импульс проходит через синапс. Молекула холинолитика (III) выключает ХР из механизма нервной передачи
Молекулярная сущность холинолитического антидотного эффекта иллюстрируется рис. 8, где в качестве холинолитика взят один из синтетических атропиноподобных препаратов и приведена вероятная схема его взаимодействия с холинорецептором. В результате такого взаимодейетвия обе белковые цепи холинорецептора как бы сшиваются и проведение нервного импульса становится невозможным.[77] Таким образом, холинолитические антидоты, образуя с холинорецептором комплекс, недоступный для ацетилхолина, на более или менее длительный срок выключают рецептор из механизма нервной передачи, что и определяет в конечном счете их действенность при отравлениях антихолинэстеразными ядами. Важно иметь в виду, что успешное лечение развившейся интоксикации ФОС достигается лишь высокими дозами атропина и других холинолитиков, причем в тяжелых случаях их эффективная разовая доза может превысить в несколько раз установленную суточную терапевтическзую дозу. Это связано с тем, что на фоне избыточной функции холинорецепторов чувствительность их к холинолитикам резко снижается. Известны случаи тяжелых отравлений ФОС, для лечения которых было израсходовано несколько сотен миллиграммов атропиноподобных веществ. Кроме того, ограниченная продолжительность действия этих препаратов диктует необходимость многократного введения их в организм при острых отравлениях. Но здесь тяжело отравленного поджидает опасность переатропинизации, признаки которой (сухость и покраснение кожи и слизистых оболочек, сердцебиение, шум в ушах, галлюцинации, расширение зрачков) указывают па необходимость немедленного прекращения антидотной терапии. Американский центр по лечению отравлений рекомендует отменять введение холинолитиков, как только у отравленного сужение зрачка сменится его расширением. Понятно, что препараты, снижающие силу и продолжительность действия холинолитиков при их длительном применении в массивных дозах, будут предотвращать избыточное угнетение холинорецепторов. Одним из ниx оказался поливинол — синтетический коллоидный заменитель плазмы, который удобно комбинировать с атропиноподобными веществами.[78] В связи с явлениями переатропинизации мы сделаем небольшое отступление. Прежде всего надо отметить, что употребление в больших дозах (количествах) настоев из растений семейства пасленовых или случайное попадание в пищу атропиноподобных веществ может привести к отравлениям, которые протекают с характерными нарушениями высшей нервной деятельности. О таких отравленных в народе говорят: «Белены объелся».[79] У них нарушается ориентировка во времени и пространстве, речь становится невнятной, возникают яркие зрительные галлюцинации, бред, расстраивается координация движений, появляется двигательное возбуждение. Вот как развиваются у людей симптомы отравления в зависимости от дозы атропина (мг):[80] • Сухость кожи, замедление пульса — 0,5 • Сухость во рту, жажда — 0,5–1 • Расширение зрачков, учащение пульса — 1–2 • Беспокойство, мышечная слабость, затруднение глотания, головная боль — 3–5 • Максимальное расширение зрачков, нарушение мышечной координации — 7 • Апатия, галлюцинация, бред, потеря сознания — 10 Нечто подобное наблюдается при попадании в организм синтетических психотомиметиков — производных гликолевой кислоты, например дитрана и бенактизина. Эти яды оказались веществами, блокирующими преимущественно М-холинорецепторы головного мозга и тем самым затрудняющими или извращающими передачу нервных импульсов в центральных холинергических структурах.[81]Совершенно очевидно, что их функциональными антагонистами могли бы оказаться вещества, способствующие стабилизации ацетилхолина в синапсах. И действительно, выраженный антидотный эффект при отравлениях холинолитическими соединениями можно наблюдать, например, при применении некоторых обратимых ингибиторов холинэстеразы, т. е. веществ, временно, нестойко угнетающих фермент. В их числе — прозерин, который взаимодействует с холинэстеразой по следующей схеме: При этом молекула прозерина благодаря положительно заряженному атому азота ориентируется за счет электростатических сил на поверхности холинэстеразы. В отличие от комплекса «яд-фермент» соединение прозерина с холинэстеразой сравнительно непрочно и в течение 2–4 ч подвергается спонтанному гидролизу, что приводит к восстановлению активности фермента. Однако, вероятно из-за наличия в молекуле прозерина положительно заряженного четвертичного атома азота, он слабо проникает через гематоэнцефалический барьер и потому недостаточно взаимодействует с холинэстеразой головного мозга. Данного недостатка лишен другой антихолинэстеразный препарат — физостигмин (эзерин), растительный аналог прозерина. Этот алкалоид является действующим началом ядовитых калабарских бобов — африканского тропического растения Physostigma venenosum Balf., которое употреблялось жителями Западной Африки для производства «божьего суда» над провинившимися. Практически используется салицилат физостигмина, который при приеме внутрь в дозе около 3–4 мг оказывает антидотное действие. Закономерно предположить, что и ФОС как антихолинэстеразные вещества будут проявлять подобное действие. Поэтому нет ничего удивительного в том, что такие лекарственные препараты из группы ФОС, как фосфакол и армин, уже в малых дозах снимают симптомы интоксикации холпнолитическими ядами.
И еще об одной группе антагонистов холинолитиков следует здесь упомянуть. Это вещества, возбуждающие холинорецепторы, т. е. действующие подобно ацетилхолину. К ним относятся такие синтетические препараты, как ацетилхолин-хлорид, карбахолин, а также растительный алкалоид пилокарпин. При этом в отличие от ацетилхолина антидотные эффекты карбахолина и пилокарпина проявляются в течение более длительного времени, так как данные препараты не гидролизуются под влиянием холинэстеразы. Надо иметь в виду, что в основе защитного действия веществ типа ацетилхолина лежит их конкурентный антагонизм с атропиноподобными соединениями за связь с одной и той же биохимической структурой — холинорецептором. Тем самым реализуется разнонаправленное действие двух групп веществ на одни и те же физиологические функции.
Как это на первый взгляд ни парадоксально, обратимые ингибиторы холинэстеразы могут проявлять себя и как антидоты ФОС. Такое их действие основано на защите холинэстеразы от стойкого угнетения ядом. Например, предварительное введение прозерина животным снижает процент их гибели при отравлении смертельными дозами ФОС. Но введение прозерина на фоне выраженного действия яда, напротив, усиливает его токсичность. По-видимому, здесь уже сказывается потенцирование действия обратимого и необратимого ингибиторов холинэстеразы.
При этом молекула прозерина благодаря положительно заряженному атому азота ориентируется за счет электростатических сил на поверхности холинэстеразы. В отличие от комплекса «яд-фермент» соединение прозерина с холинэстеразой сравнительно непрочно и в течение 2–4 ч подвергается спонтанному гидролизу, что приводит к восстановлению активности фермента. Однако, вероятно из-за наличия в молекуле прозерина положительно заряженного четвертичного атома азота, он слабо проникает через гематоэнцефалический барьер и потому недостаточно взаимодействует с холинэстеразой головного мозга. Данного недостатка лишен другой антихолинэстеразный препарат — физостигмин (эзерин), растительный аналог прозерина. Этот алкалоид является действующим началом ядовитых калабарских бобов — африканского тропического растения Physostigma venenosum Balf., которое употреблялось жителями Западной Африки для производства «божьего суда» над провинившимися. Практически используется салицилат физостигмина, который при приеме внутрь в дозе около 3–4 мг оказывает антидотное действие. Закономерно предположить, что и ФОС как антихолинэстеразные вещества будут проявлять подобное действие. Поэтому нет ничего удивительного в том, что такие лекарственные препараты из группы ФОС, как фосфакол и армин, уже в малых дозах снимают симптомы интоксикации холпнолитическими ядами.
И еще об одной группе антагонистов холинолитиков следует здесь упомянуть. Это вещества, возбуждающие холинорецепторы, т. е. действующие подобно ацетилхолину. К ним относятся такие синтетические препараты, как ацетилхолин-хлорид, карбахолин, а также растительный алкалоид пилокарпин. При этом в отличие от ацетилхолина антидотные эффекты карбахолина и пилокарпина проявляются в течение более длительного времени, так как данные препараты не гидролизуются под влиянием холинэстеразы. Надо иметь в виду, что в основе защитного действия веществ типа ацетилхолина лежит их конкурентный антагонизм с атропиноподобными соединениями за связь с одной и той же биохимической структурой — холинорецептором. Тем самым реализуется разнонаправленное действие двух групп веществ на одни и те же физиологические функции.
Как это на первый взгляд ни парадоксально, обратимые ингибиторы холинэстеразы могут проявлять себя и как антидоты ФОС. Такое их действие основано на защите холинэстеразы от стойкого угнетения ядом. Например, предварительное введение прозерина животным снижает процент их гибели при отравлении смертельными дозами ФОС. Но введение прозерина на фоне выраженного действия яда, напротив, усиливает его токсичность. По-видимому, здесь уже сказывается потенцирование действия обратимого и необратимого ингибиторов холинэстеразы.
Реактиваторы холинзстеразы
Второй практически значимый антидотный механизм при отравлениях антихолинэстеразными ядами, как уже отмечалось, состоит в восстановлении (реактивировании) каталитической функции ацетилхолинэстеразы. Принцип реактивации заключается в том, что достаточно сильный реагент, каким является антидот, разрушает химическую связь между ядом и ферментом. Следовательно, антидотный эффект проявляется уже после того, как токсичное вещество инактивировало биохимическую рецептивную структуру. Наиболее ценными антидотами такого рода являются химические вещества, которых объединяет наличие в молекуле оксимной (=N-ОН) группировки и которые поэтому получили название оксимов. Из большого их числа следует прежде всего назвать те, которые находят практическое применение: дипироксим (ТМБ-4), пралидоксим (2-ПАМ), изонитрозин, токсогонин. Механизм их реактивирующего действия можно видеть на примере взаимодействия дипироксима с комплексом «ди-изопропилфторфосфат-холинэстераза»: Как видно из приведенной схемы, наличие положительно заряженного азота в молекуле дипироксима помогает ее сближению с ингибированным ферментом.[82] При этом рвется связь яда с холинэстеразой и восстанавливается ее структура и функция. Затем реактиватор взаимодействует с ядом, образуя нетоксичный комплекс «дипироксим-ФОС», который в дальнейшем превращается в безвредные для организма продукты. Из структуры дипироксима следует, что одна его молекула может одномоментно участвовать в процессе реактивирования 2 молекул фермента. Это, по-видимому, лежит в основе высокой антидотной активности данного препарата. Но реактиваторы холинэстераз весьма эффективны также при профилактическом введении в организм, что связывается с их способностью обратимо тормозить холинэстеразу (вероятно, подобно прозерину) и тем защищать ее от последующего угнетения ФОС.
Очень важно стремиться ввести отравленному реактиватор в максимально короткие сроки от момента проникновения яда в организм, так как оторвать яд от фермента практически можно лишь на этапе обратимого его ингибирования. Ясно также, что чем длиннее этот этап, тем больше шансов на успех применения реактиваторов. Для ряда сильнодействующих ФОС данное время составляет примерно 30–100 мин.
При отравлении антихолинэстеразными ядами наиболее выраженным антидотным действием реактиваторы обладают тогда, когда они применяются совместно с холино-литиками. Именно такая комбинация считается самой рациональной, тем более что реактиваторы значительно усиливают антидотное действие холинолитиков. Это, например, было показано в работах зарубежного исследователя Келле[83] и у нас Г. К. Шеиным.[84] Так, Г. К. Шеин установил, что дипироксим совместно с атропином и арпеналом дает выраженный антидотный эффект при воздействии смертельных доз ФОС, в то время как сами эти холинолитики в тех же дозах не спасали животных от гибели.
В последнее время появились экспериментальные доказательства свойства реактиваторов холинэстераз непосредственно реагировать с ФОС с образованием нетоксичных комплексов или необратимо трансформировать их молекулы, или же ускорять их гидролиз в организме. Это, например, можно проиллюстрировать реакцией пралидоксима с зарином:
Как видно из приведенной схемы, наличие положительно заряженного азота в молекуле дипироксима помогает ее сближению с ингибированным ферментом.[82] При этом рвется связь яда с холинэстеразой и восстанавливается ее структура и функция. Затем реактиватор взаимодействует с ядом, образуя нетоксичный комплекс «дипироксим-ФОС», который в дальнейшем превращается в безвредные для организма продукты. Из структуры дипироксима следует, что одна его молекула может одномоментно участвовать в процессе реактивирования 2 молекул фермента. Это, по-видимому, лежит в основе высокой антидотной активности данного препарата. Но реактиваторы холинэстераз весьма эффективны также при профилактическом введении в организм, что связывается с их способностью обратимо тормозить холинэстеразу (вероятно, подобно прозерину) и тем защищать ее от последующего угнетения ФОС.
Очень важно стремиться ввести отравленному реактиватор в максимально короткие сроки от момента проникновения яда в организм, так как оторвать яд от фермента практически можно лишь на этапе обратимого его ингибирования. Ясно также, что чем длиннее этот этап, тем больше шансов на успех применения реактиваторов. Для ряда сильнодействующих ФОС данное время составляет примерно 30–100 мин.
При отравлении антихолинэстеразными ядами наиболее выраженным антидотным действием реактиваторы обладают тогда, когда они применяются совместно с холино-литиками. Именно такая комбинация считается самой рациональной, тем более что реактиваторы значительно усиливают антидотное действие холинолитиков. Это, например, было показано в работах зарубежного исследователя Келле[83] и у нас Г. К. Шеиным.[84] Так, Г. К. Шеин установил, что дипироксим совместно с атропином и арпеналом дает выраженный антидотный эффект при воздействии смертельных доз ФОС, в то время как сами эти холинолитики в тех же дозах не спасали животных от гибели.
В последнее время появились экспериментальные доказательства свойства реактиваторов холинэстераз непосредственно реагировать с ФОС с образованием нетоксичных комплексов или необратимо трансформировать их молекулы, или же ускорять их гидролиз в организме. Это, например, можно проиллюстрировать реакцией пралидоксима с зарином:
 Такое действие оксимов неизмеримо возрастает в случае их профилактического применения, что дает возможность защищать подопытных животных от смертельных доз некоторых ФОС.[85] Можно допустить, что в данном случае антидот как бы поджидает яд в организме.
Ряд авторов допускают наличие у реактиваторов и других антидотных свойств. Так, не исключается, что оксимы способны взаимодействовать с холинорецепторами и даже выполнять функцию холинэстеразы, т. е. инактивировать ацетилхолин. В частности, существует мнение, что реактиватор, с одной стороны, способен защищать холинорецептор от воздействия избытка медиатора, а с другой — взаимодействовать с комплексом «ФОС-хелинорецептор», освобождая последний от яда. Все это дает основание считать реактиваторы холинэстераз антидотами многостороннего действия.
В связи с изложенным небезынтересно исследование,[86] которое доказывает высокую специфичность реактиваторов холинэстераз как антидотов. Оно посвящено веществу под названием севин, представителю новой группы антихолинэстеразных ядохимикатов, производных карбаминовой кислоты (
Такое действие оксимов неизмеримо возрастает в случае их профилактического применения, что дает возможность защищать подопытных животных от смертельных доз некоторых ФОС.[85] Можно допустить, что в данном случае антидот как бы поджидает яд в организме.
Ряд авторов допускают наличие у реактиваторов и других антидотных свойств. Так, не исключается, что оксимы способны взаимодействовать с холинорецепторами и даже выполнять функцию холинэстеразы, т. е. инактивировать ацетилхолин. В частности, существует мнение, что реактиватор, с одной стороны, способен защищать холинорецептор от воздействия избытка медиатора, а с другой — взаимодействовать с комплексом «ФОС-хелинорецептор», освобождая последний от яда. Все это дает основание считать реактиваторы холинэстераз антидотами многостороннего действия.
В связи с изложенным небезынтересно исследование,[86] которое доказывает высокую специфичность реактиваторов холинэстераз как антидотов. Оно посвящено веществу под названием севин, представителю новой группы антихолинэстеразных ядохимикатов, производных карбаминовой кислоты ( ) карбаматов. Оказалось, что реактиваторы из класса оксимов почти не оказывают влиякая на течение интоксикации севином, и это связывается с тем, что данный яд блокирует холинэстеразу не посредством фосфорилирования, а за счет взаимодействия с эстеразным пунктом фермента его карбаминовой группировки (так называемое карбаминирование). В то же время холинолитические препараты (атропин, тропацин и др.) проявляют при отравлении карбаматами выраженное антидотное действие, что подчеркивает ведущее значение избыточной функции холинорецепторов при интоксикациях антихолинэстеразньми веществами разного химического строения.
Заканчивая описание основных антидотных механизмов при отравлениях антихолинэстеразными веществами, обратим внимание на любопытные результаты одной научной работы. Совершенно неожиданно защитное действие по отношению к ФОС выявилось у самих ФОС. Некоторое время назад академик Б. А. Арбузов с сотрудниками[87] сообщили о новых свойствах ряда ФОС с низкой токсичностью. Оказалось, что ФОС — производные кетоалкилфосфиновых кислот типа
) карбаматов. Оказалось, что реактиваторы из класса оксимов почти не оказывают влиякая на течение интоксикации севином, и это связывается с тем, что данный яд блокирует холинэстеразу не посредством фосфорилирования, а за счет взаимодействия с эстеразным пунктом фермента его карбаминовой группировки (так называемое карбаминирование). В то же время холинолитические препараты (атропин, тропацин и др.) проявляют при отравлении карбаматами выраженное антидотное действие, что подчеркивает ведущее значение избыточной функции холинорецепторов при интоксикациях антихолинэстеразньми веществами разного химического строения.
Заканчивая описание основных антидотных механизмов при отравлениях антихолинэстеразными веществами, обратим внимание на любопытные результаты одной научной работы. Совершенно неожиданно защитное действие по отношению к ФОС выявилось у самих ФОС. Некоторое время назад академик Б. А. Арбузов с сотрудниками[87] сообщили о новых свойствах ряда ФОС с низкой токсичностью. Оказалось, что ФОС — производные кетоалкилфосфиновых кислот типа
 не оказывали антихолинэстеразного действия. В то же время они проявляли выраженные антидотные свойства но отношению к токсичным ФОС, угнетающим холинэстеразу. Ученые установили, в частности, что с помощью препаратов, у которых R=OCH3, a R'=CH3, можно спасти от гибели 80–100% подопытных животных, отравленных абсолютно смертельными дозами таких сильнодействующих ФОС, как октаметил и фосфакол. Что касается молекулярного механизма описанного эффекта «ФОС против ФОС», то каких-либо убедительных данных на этот счет пока не имеется. Известно только, что по отношению к холинэстеразе кетоалкилфосфонаты не проявляют заметного реактивирующего и защитного действия, но несколько повышают ее активность в организме.
Представления о взаимосвязи нервного импульса, токсичных веществ и противоядий были бы неполными, если бы мы не рассмотрели структуру и функцию адренореактивных систем и токсикологические особенности соответствующих ядов и антидотов.
не оказывали антихолинэстеразного действия. В то же время они проявляли выраженные антидотные свойства но отношению к токсичным ФОС, угнетающим холинэстеразу. Ученые установили, в частности, что с помощью препаратов, у которых R=OCH3, a R'=CH3, можно спасти от гибели 80–100% подопытных животных, отравленных абсолютно смертельными дозами таких сильнодействующих ФОС, как октаметил и фосфакол. Что касается молекулярного механизма описанного эффекта «ФОС против ФОС», то каких-либо убедительных данных на этот счет пока не имеется. Известно только, что по отношению к холинэстеразе кетоалкилфосфонаты не проявляют заметного реактивирующего и защитного действия, но несколько повышают ее активность в организме.
Представления о взаимосвязи нервного импульса, токсичных веществ и противоядий были бы неполными, если бы мы не рассмотрели структуру и функцию адренореактивных систем и токсикологические особенности соответствующих ядов и антидотов.
Адренергические медиаторы и рецепторные структуры
До сих пор речь шла о веществах, которые прямо или косвенно связаны с функцией одного из химических передатчиков нервного возбуждения — ацетилхолина. Иной молекулярный механизм лежит в основе действия ядов и антидотов, вмешивающихся в обмен адреналина и норадреналина, — медиаторов второго типа, получивших общее название катехоламинов. Биохимическим предшественником этих веществ является жизненно важная аминокислота тирозин: В настоящее время как медиатор рассматривается также дофамин, который, как видно из приведенной схемы, является промежуточным продуктом биосинтеза норадреналина и адреналина. Физиологическая роль этих передатчиков нервного импульса проявляется в центральных и периферических структурах, которые принято называть адренергическими в отличие от описанных ранее холинергических, связанных с ацетилхолином. Установлено, что катехоламины обладают выраженными свойствами регуляторов ряда процессов жизнедеятельности. Поэтому они, прежде всего адреналин, нередко рассматриваются как гормональные вещества.
В настоящее время как медиатор рассматривается также дофамин, который, как видно из приведенной схемы, является промежуточным продуктом биосинтеза норадреналина и адреналина. Физиологическая роль этих передатчиков нервного импульса проявляется в центральных и периферических структурах, которые принято называть адренергическими в отличие от описанных ранее холинергических, связанных с ацетилхолином. Установлено, что катехоламины обладают выраженными свойствами регуляторов ряда процессов жизнедеятельности. Поэтому они, прежде всего адреналин, нередко рассматриваются как гормональные вещества.

Рис. 9. Предполагаемая схема фиксации адреналина в активных центрах адренорецептивных структур (Комиссаров, 1959)
Не касаясь многих сложных и до конца еще не изученных сторон биохимической организации адренергических систем, можно полагать, что выброс норадреналина (точнее, его смеси с адреналином, именуемой симпатином) в синаптическую щель и последующее его взаимодействие с рецепторньми структурами (адренорецепторами) являются непременным условием нормального функционирования соответствующих отделов нервной системы. Адренорецепторы, с которыми взаимодействуют катехоламины, неоднородны. Это доказывается тем, что характер ответных реакций разных органов даже на один и тот же катехоламин может быть неодинаковым, а один и тот же орган может разнонаправленно реагировать на введение различных катехоламинов. В связи с этим по предложению американского ученого Алквиста (1948 г.) принято рассматривать 2 типа адренорецепторов: α- и β-адренорецепторы. Возбуждение α-адренорецепторов связывается с сужением кровеносных сосудов, увеличением тонуса гладких мышц и усилением функции большинства соответствующих органов и структур, а стимуляция β-адренорецепторов, наоборот, угнетает деятельность этих органов, расширяет кровеносные сосуды, повышает частоту и силу сокращений сердца.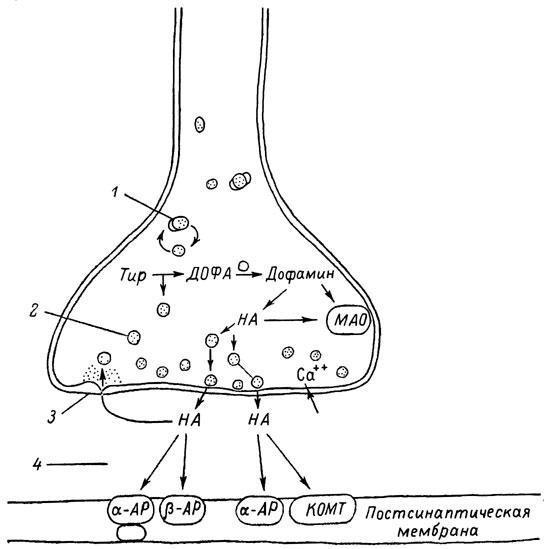
Рис. 10. Основные структурные элементы и схема функционирования адренер гического синапса (Голяков, Фишзон-Рысс, 1978). 1 — гранулы депонирования норадреналина (НА); 2 — синаптические пузырьки; з — обратный захват НА; 4 — сипаптическая щель; КОМТ — кате-хол-орто-метилтрансфераза; МАО — моноаминоксидаза; ДОФА — диокси-фенилалашш; Тир — тирозин; α-АР и β-AP — α- и β-адренорецепторы
Согласно современным взглядам, адренорецепторы представляют собою металлопротеиды, имеющие двучленное строение с атомом железа или марганца в роли связующего звена, что позволяет одновременно фиксироваться на них 2 молекулам медиатора. По крайней мере такая структура с достаточным основанием приписывается α-адренорецепторам (рис. 9). Мгновенная инактивация медиаторов в адренергических синапсах осуществляется большим числом ферментов,[88] из которых главное значение имеют моноаминоксидаза и катехоламин-орто-метилтрансфераза (КОМТ) (рис. 10). Данные ферменты катализируют окислительное дезаминирование катехоламинов. Биохимиками более изучена структура и функция моноаминоксидазы, которая в отличие от холинэстеразы является сложным металло-протеидом, имеющим в составе своей молекулы активную каталитическую часть особой химической структуры, именуемую в биохимии простетической, или коферментной и включающую пиридоксальфосфатную группировку и атомы меди. В свою очередь пиридоксальфосфат состоит из пиридоксина (витамина В6) и фосфорной кислоты. Согласно принятым данным,[89] именно пиридоксин и медь являются важнейшими компонентами активных каталитических центров моноаминоксидазы и ряда других ферментов, получивших общее название пиридоксалевых.Серотонин
Результаты экспериментальных и клинических исследований позволяют теперь с достаточной определенностью говорить о существовании такого медиатора нервного возбуждения, биохимическая роль которого связана в основном с высшей нервной деятельностью. Речь идет о серотонине (5-окситриптамине), который считается химическим передатчиком нервных импульсов в центральных синапсах главным образом стволовой части головного мозга. Источником образования серотонина в организме является одна из жизненно важных аминокислот — триптофан, который под действием специфического фермента (оксидазы) превращается в 5-окситриптофан, а последний декарбоксилируется (теряет СО2) и превращается в серотонин: Понятно, что после выполнения медиаторной функции (т. е. после воздействия на соответствующие рецепторы) молекулы серотонина, подобно другим медиаторам, мгновенно инактивируются. Это происходит вследствие дезаминирования и окисления под влиянием фермента моноаминоксидазы. Следовательно, катехоламины и серотонин связывает общность путей биотрансформации. В этой связи небезынтересно сопоставить химическую структуру адреналина и серотонина. Если допустить, что этиламиновая группа адреналина изогнута, то по своей конфигурации его молекула представляет собою разорванный индольный гетероцикл:[90]
Понятно, что после выполнения медиаторной функции (т. е. после воздействия на соответствующие рецепторы) молекулы серотонина, подобно другим медиаторам, мгновенно инактивируются. Это происходит вследствие дезаминирования и окисления под влиянием фермента моноаминоксидазы. Следовательно, катехоламины и серотонин связывает общность путей биотрансформации. В этой связи небезынтересно сопоставить химическую структуру адреналина и серотонина. Если допустить, что этиламиновая группа адреналина изогнута, то по своей конфигурации его молекула представляет собою разорванный индольный гетероцикл:[90]
 Основываясь на такой точке зрения, можно предположить, что биоструктуры, с которыми взаимодействует серотонин, близки по своему строению с адренорецепторами. Подобие химического строения серотонина с веществами, близкими к адреналину, имеет значение для понимания молекулярного механизма действия некоторых психотомиметических ядов.
Основываясь на такой точке зрения, можно предположить, что биоструктуры, с которыми взаимодействует серотонин, близки по своему строению с адренорецепторами. Подобие химического строения серотонина с веществами, близкими к адреналину, имеет значение для понимания молекулярного механизма действия некоторых психотомиметических ядов.
Гамма-аминомасляная кислота
В последние 25 лет все большее внимание биохимиков, фармакологов, токсикологов привлекает еще один медиатор передачи импульсов в нервной системе — гамма-аминомасляная кислота (ГАМК). Этот медиатор является нормальным продуктом обмена веществ у млекопитающих и образуется из глутаминовой кислоты при действии пиридоксалевого фермента глутаматдекарбоксилазы: Теперь считается доказанным,[91] что ГАМК тормозит развитие и проведение импульсов в центральной нервной системе. Следовательно, можно полагать, что по своему биохимическому действию ГАМК есть антагонист тех эндогенных и экзогенных веществ, которые вызывают или стимулируют в нервной системе возбудительный процесс. Освобождающаяся при раздражении тормозных нервных структур (проводящих путей, нервов, клеточных скоплений) ГАМК преодолевает синаптическую щель и вступает во взаимодействие с рецепторами постсинаптической мембраны (ГАМК-рецепторами). По И. А. Сытинскому, ГАМК-рецептор — субклеточная структура (фосфолипидно-белковьй комплекс) постсинаптической мембраны с активными участками, облегчающими сорбцию медиатора на его поверхности. Не исключается, что ГАМК-рецепторы, подобно адренорецепторам, имеют двучленное строение и, следовательно, могут активироваться 2 молекулами медиатора. Медкаторное действие ГАМК в центральной нервной системе можно также объяснить сходством ее химического и пространственного строения с ацетилхолином:
Теперь считается доказанным,[91] что ГАМК тормозит развитие и проведение импульсов в центральной нервной системе. Следовательно, можно полагать, что по своему биохимическому действию ГАМК есть антагонист тех эндогенных и экзогенных веществ, которые вызывают или стимулируют в нервной системе возбудительный процесс. Освобождающаяся при раздражении тормозных нервных структур (проводящих путей, нервов, клеточных скоплений) ГАМК преодолевает синаптическую щель и вступает во взаимодействие с рецепторами постсинаптической мембраны (ГАМК-рецепторами). По И. А. Сытинскому, ГАМК-рецептор — субклеточная структура (фосфолипидно-белковьй комплекс) постсинаптической мембраны с активными участками, облегчающими сорбцию медиатора на его поверхности. Не исключается, что ГАМК-рецепторы, подобно адренорецепторам, имеют двучленное строение и, следовательно, могут активироваться 2 молекулами медиатора. Медкаторное действие ГАМК в центральной нервной системе можно также объяснить сходством ее химического и пространственного строения с ацетилхолином:
 Поэтому учитывается возможность конкурентного антагонизма этих медиаторов в их действии на холинергические рецепторные структуры: взаимодействие с ГАМК защищает холинорецептор от стимулирующего влияния ацетилхолина.
Как и другие медиаторы, ГАМК разрушается в постсинаптических структурах с помощью специфического катализатора. Им является фермент ГАМК-трансаминаза. Важно при этом иметь в виду, что при инактивации ГАМК вновь образуется ее предшественник — глутаминовая кислота. С другой стороны, закономерно, что блокада трансаминазы приводит к избытку ГАМК в синапсах.
Поэтому учитывается возможность конкурентного антагонизма этих медиаторов в их действии на холинергические рецепторные структуры: взаимодействие с ГАМК защищает холинорецептор от стимулирующего влияния ацетилхолина.
Как и другие медиаторы, ГАМК разрушается в постсинаптических структурах с помощью специфического катализатора. Им является фермент ГАМК-трансаминаза. Важно при этом иметь в виду, что при инактивации ГАМК вновь образуется ее предшественник — глутаминовая кислота. С другой стороны, закономерно, что блокада трансаминазы приводит к избытку ГАМК в синапсах.
Яды — блокаторы пиридоксалевых ферментов
Ряд ядов избирательно влияет на медиаторную функцию катехоламинов, серотонина и ГАМК. Один из них — сероуглерод (CS2) — высокотоксичное производное дитиокарбаминовой кислоты ( ), широко применяющееся в производстве вискозных волокон, целлофана, ядохимикатов, четыреххлористого углерода, а также в качестве растворителя.
При попадании сероуглерода в организм через органы дыхания, кожу, зараженную пищу и воду возникают характерные явления нейроинтоксикации. Вначале отмечается возбуждение, нарушение координации движений, рвота, бред, а затем апатия, заторможенность, потеря памяти. В особо тяжелых случаях утрачивается сознание, угнетаются или даже исчезают зрачковые и сухожильные рефлексы, расстраивается дыхание и работа сердца.
Работами ряда исследователей прежде всего советских (З. X. Черный, Ж. И. Абрамова и др.), с достоверностью установлено, что сероуглерод является специфическим ингибитором моноаминоксидазы. Это в свою очередь приводит к нарушению обмена биогенных аминов, в особенности окисления серотонина, накоплению его и других медиаторов в синапсах и к избыточной функции адрено-рецепторных структур. В свете такого механизма становится понятным найденный упомянутыми авторами при сероуглеродной интоксикации дефицит в организме витамина В6 и меди.[92] Надо иметь также в виду, что в организме CS2 связывается с другими биоструктурами, содержащими свободные сульфгидрильные и аминные группы. Образующимся при этом тиокарбаматным соединениям приписывается способность связывать биоэлементы, в том числе медь, и тем вторично нарушать функцию металлсодержащих ферментов (моноаминоксидазы и др.).
Рассмотрим далее токсикологические особенности гидразина (N2H4) и его соединений, которые широко используются в промышленности (производство пластических масс, синтетических смол, каучука, красителей, взрывчатых веществ и др.), как ядохимикаты и химические реактивы, а также в клинической медицине при лечении туберкулеза, опухолевых заболеваний и в качестве психофармакологических средств. Кроме того, соединения гидразина как сильные восстановители применяются для стабилизации жиров, фруктовых соков и других продуктов, о некоторые из них используются как регуляторы роста растений. Несмотря на различия в химическом строении отдельных представителей этого класса соединений, их объединяют важнейшие признаки резорбтивного действия, которые мало зависят от путей поступления веществ в организм. При воздействии на организм больших доз гидразина и высокотоксичных веществ, синтезированных на его основе, на первый план выступают расстройства со стороны нервной системы: головная боль, возбуждение, судороги, потеря сознания, параличи, а также симптомы поражения печени.
Теперь не вызывает сомнения, что основным первичным объектом их токсического воздействия на молекулярном уровне является уже знакомый нам фермент глутаматдекарбоксилаза, а во взаимодействие с ядами вступает ее кофермент — пиридоксальфосфат. Один из возможных механизмов такой реакции представлен в виде следующей схемы:
), широко применяющееся в производстве вискозных волокон, целлофана, ядохимикатов, четыреххлористого углерода, а также в качестве растворителя.
При попадании сероуглерода в организм через органы дыхания, кожу, зараженную пищу и воду возникают характерные явления нейроинтоксикации. Вначале отмечается возбуждение, нарушение координации движений, рвота, бред, а затем апатия, заторможенность, потеря памяти. В особо тяжелых случаях утрачивается сознание, угнетаются или даже исчезают зрачковые и сухожильные рефлексы, расстраивается дыхание и работа сердца.
Работами ряда исследователей прежде всего советских (З. X. Черный, Ж. И. Абрамова и др.), с достоверностью установлено, что сероуглерод является специфическим ингибитором моноаминоксидазы. Это в свою очередь приводит к нарушению обмена биогенных аминов, в особенности окисления серотонина, накоплению его и других медиаторов в синапсах и к избыточной функции адрено-рецепторных структур. В свете такого механизма становится понятным найденный упомянутыми авторами при сероуглеродной интоксикации дефицит в организме витамина В6 и меди.[92] Надо иметь также в виду, что в организме CS2 связывается с другими биоструктурами, содержащими свободные сульфгидрильные и аминные группы. Образующимся при этом тиокарбаматным соединениям приписывается способность связывать биоэлементы, в том числе медь, и тем вторично нарушать функцию металлсодержащих ферментов (моноаминоксидазы и др.).
Рассмотрим далее токсикологические особенности гидразина (N2H4) и его соединений, которые широко используются в промышленности (производство пластических масс, синтетических смол, каучука, красителей, взрывчатых веществ и др.), как ядохимикаты и химические реактивы, а также в клинической медицине при лечении туберкулеза, опухолевых заболеваний и в качестве психофармакологических средств. Кроме того, соединения гидразина как сильные восстановители применяются для стабилизации жиров, фруктовых соков и других продуктов, о некоторые из них используются как регуляторы роста растений. Несмотря на различия в химическом строении отдельных представителей этого класса соединений, их объединяют важнейшие признаки резорбтивного действия, которые мало зависят от путей поступления веществ в организм. При воздействии на организм больших доз гидразина и высокотоксичных веществ, синтезированных на его основе, на первый план выступают расстройства со стороны нервной системы: головная боль, возбуждение, судороги, потеря сознания, параличи, а также симптомы поражения печени.
Теперь не вызывает сомнения, что основным первичным объектом их токсического воздействия на молекулярном уровне является уже знакомый нам фермент глутаматдекарбоксилаза, а во взаимодействие с ядами вступает ее кофермент — пиридоксальфосфат. Один из возможных механизмов такой реакции представлен в виде следующей схемы:
 Таким образом, гидразин и его соединения блокируют реакцию превращения глутаминовой кислоты в ГАМК. Имеются данные, согласно которым ряд гидразинов связывает также ГАМК-трансаминазу и, кроме того, тормозит синтез пиридоксальфосфата. Тем самым еще больше усложняется цепь нарушений передачи импульсов в центральной нервной системе, главным образом — тормозных. Этим, однако, не ограничивается механизм влияния рассматриваемых ядов на организм. Считается доказанным, что многие из них, подобно сероуглероду, ингибируют и моноаминоксидазу, а следовательно, тормозят окислительное дезаминирование катехоламинов и серотонина и приводят к их накоплению в адренергических структурах. Это в свою очередь вызывает избыточную функцию адренорецепторов центральной нервной системы и, по-видимому, лежит в основе возникновения таких симптомов, как психомоторное возбуждение, эйфория и т. п.
Итак, изложенное показывает, что многие ядовитые вещества вмешиваются в обмен биогенных аминов посредством блокирования пиридоксалевых ферментов. Основываясь на приведенных молекулярных механизмах и по аналогии с антихолинэстеразными ядами (см. с. 65), можно наметить несколько рациональных направлений антидотного воздействия на течение интоксикаций этими веществами. Однако существующие знания о структуре и биохимических свойствах адренореактивных систем и механизмах ингибирования пиридоксалевых ферментов позволяют реализовать (или предсказать реализацию в скором будущем) только те из них, при которых осуществляется:
а) заместительное действие противоядия и
б) влияние па функцию адренорецептивных структур
Таким образом, гидразин и его соединения блокируют реакцию превращения глутаминовой кислоты в ГАМК. Имеются данные, согласно которым ряд гидразинов связывает также ГАМК-трансаминазу и, кроме того, тормозит синтез пиридоксальфосфата. Тем самым еще больше усложняется цепь нарушений передачи импульсов в центральной нервной системе, главным образом — тормозных. Этим, однако, не ограничивается механизм влияния рассматриваемых ядов на организм. Считается доказанным, что многие из них, подобно сероуглероду, ингибируют и моноаминоксидазу, а следовательно, тормозят окислительное дезаминирование катехоламинов и серотонина и приводят к их накоплению в адренергических структурах. Это в свою очередь вызывает избыточную функцию адренорецепторов центральной нервной системы и, по-видимому, лежит в основе возникновения таких симптомов, как психомоторное возбуждение, эйфория и т. п.
Итак, изложенное показывает, что многие ядовитые вещества вмешиваются в обмен биогенных аминов посредством блокирования пиридоксалевых ферментов. Основываясь на приведенных молекулярных механизмах и по аналогии с антихолинэстеразными ядами (см. с. 65), можно наметить несколько рациональных направлений антидотного воздействия на течение интоксикаций этими веществами. Однако существующие знания о структуре и биохимических свойствах адренореактивных систем и механизмах ингибирования пиридоксалевых ферментов позволяют реализовать (или предсказать реализацию в скором будущем) только те из них, при которых осуществляется:
а) заместительное действие противоядия и
б) влияние па функцию адренорецептивных структур
Витамин В6, глутаминовая кислота и препараты меди как антидоты
Витамины B6, или пиридоксин , согласно экспериментальным и клиническим данным, проявляет выраженные антидотные свойства при отравлениях сероуглеродом, другими дитиокарбаматами и трихлорэтиленом. Например, при сероуглеродной интоксикации под воздействием пиридоксина наблюдается снижение циркуляции яда в крови и повышение его выделения с мочой, что, по-видимому, говорит об образовании нетоксичного комплекса сероуглерода с антидотом.[93] Не менее ценен пиридоксин и как антидот при гидразиновых интоксикациях. Биохимическая роль его здесь закономерна с учетом ферментного механизма действия данных ядов. А поскольку антидотный эффект пиридоксина проявляется на фоне уже развившейся интоксикации, то нельзя исключить способность этого вещества отрывать молекулы яда от блокированных пиридоксалевых ферментов с последующей их детоксикацией, т. е. действовать подобно реактиваторам холинэстераз. Надо учитывать также, что введение в организм пиридоксина как необходимого компонента названных ферментов облегчает и ускоряет синтез новых их молекул, а это, естественно, способствует нормализации нарушенного обмена медиаторов и торможению токсического процесса. Перед нами, таким образом, пример удачного использования заместительного противоядия — аналога одного из биохимических объект в воздействия токсичного вещества. Тем самым для борьбы с отравлениями используется способ, практическую значимость которого еще более 35 лет назад предсказал профессор Н. В. Лазарев. Он писал: «…вполне естественно надеяться, что в целом ряде случаев, вводя извне „сырые материалы“, нужные для синтеза фермента, деятельность которого угнетается ядом, мы сможем увеличить количество этого фермента, а тем частично вознаградить клетки за потерю молекул последнего в результате отравления».[94] Справедливость этих слов можно будет видеть и на примерах использования других антидотов.
Витамин В6 (в виде хлорида пиридоксина) при острых отравлениях рекомендуется назначать в больших дозах.[95] В то же время при хронических формах отравлений, а также с профилактической целью применяются сравнительно небольшие его количества. Так, специально разработанная сотрудниками Ленинградского НИИ гигиены труда и профессиональных заболеваний инструкция[96] рекомендует для нормализации функциональных сдвигов в организме при хронической интоксикации сероуглеродом ежедневную дозу пиридоксина, равную 50 мг (1 мл 5%-ного раствора). С этой же целью инструкция предписывает комбинировать пиридоксин с глутаминовой кислотой. Механизм ее действия, как считают,[97] состоит прежде всего в химическом связывании яда и ускорении его выведения из организма. С другой стороны, в качестве антидота глутаминовая кислота должна рассматриваться и как биохимический предшественник ГАМК. Это ее свойство может оказаться полезным для специфического воздействия на течение и других интоксикаций, при которых нарушается обмен данного медиатора.[98]
В последнее время для лечения различных нарушений функционирования центральной нервной системы все больше используется гаммалон — препарат гамма-амино-масляной кислоты. Его назначают внутрь в таблетках по 0,25 г и для введения в вену в виде 5%-ного раствора. Можно предположить, что этот препарат найдет практическое применение и как заместительное антидотное средство в первую очередь при гидразиновых отравлениях.
Тот факт, что яды-ингибиторы моноаминоксидазы имеют химическое сродство к меди, входящей в состав данного фермента, давно наводил исследователей на мысль о применении этого микроэлемента при соответствующих отравлениях. И действительно, оказалось, что соединения меди, в частности уксусномедная соль, препятствуют развитию нарушений обмена веществ при сероуглеродной и гидразиновых интоксикациях, резко понижают накопление этих ядов и продуктов их превращений в организме, а также нормализуют метаболизм биогенных аминов. Все это, несомненно, свидетельствует о том, что препараты меди проявляют свойства антидотов. Вполне оправданы поэтому рекомендации по их практическому применению. Так, в настоящее время предписывается дополнительно вводить ацетат меди (совместно с пиридоксином) в рацион лечебно-профилактического питания лиц, контактирующих на производстве с сероуглеродом и другими дитиокарбаматами, а также обязательно включать его в комплекс антидотных средств при соответствующих интоксикациях.
, согласно экспериментальным и клиническим данным, проявляет выраженные антидотные свойства при отравлениях сероуглеродом, другими дитиокарбаматами и трихлорэтиленом. Например, при сероуглеродной интоксикации под воздействием пиридоксина наблюдается снижение циркуляции яда в крови и повышение его выделения с мочой, что, по-видимому, говорит об образовании нетоксичного комплекса сероуглерода с антидотом.[93] Не менее ценен пиридоксин и как антидот при гидразиновых интоксикациях. Биохимическая роль его здесь закономерна с учетом ферментного механизма действия данных ядов. А поскольку антидотный эффект пиридоксина проявляется на фоне уже развившейся интоксикации, то нельзя исключить способность этого вещества отрывать молекулы яда от блокированных пиридоксалевых ферментов с последующей их детоксикацией, т. е. действовать подобно реактиваторам холинэстераз. Надо учитывать также, что введение в организм пиридоксина как необходимого компонента названных ферментов облегчает и ускоряет синтез новых их молекул, а это, естественно, способствует нормализации нарушенного обмена медиаторов и торможению токсического процесса. Перед нами, таким образом, пример удачного использования заместительного противоядия — аналога одного из биохимических объект в воздействия токсичного вещества. Тем самым для борьбы с отравлениями используется способ, практическую значимость которого еще более 35 лет назад предсказал профессор Н. В. Лазарев. Он писал: «…вполне естественно надеяться, что в целом ряде случаев, вводя извне „сырые материалы“, нужные для синтеза фермента, деятельность которого угнетается ядом, мы сможем увеличить количество этого фермента, а тем частично вознаградить клетки за потерю молекул последнего в результате отравления».[94] Справедливость этих слов можно будет видеть и на примерах использования других антидотов.
Витамин В6 (в виде хлорида пиридоксина) при острых отравлениях рекомендуется назначать в больших дозах.[95] В то же время при хронических формах отравлений, а также с профилактической целью применяются сравнительно небольшие его количества. Так, специально разработанная сотрудниками Ленинградского НИИ гигиены труда и профессиональных заболеваний инструкция[96] рекомендует для нормализации функциональных сдвигов в организме при хронической интоксикации сероуглеродом ежедневную дозу пиридоксина, равную 50 мг (1 мл 5%-ного раствора). С этой же целью инструкция предписывает комбинировать пиридоксин с глутаминовой кислотой. Механизм ее действия, как считают,[97] состоит прежде всего в химическом связывании яда и ускорении его выведения из организма. С другой стороны, в качестве антидота глутаминовая кислота должна рассматриваться и как биохимический предшественник ГАМК. Это ее свойство может оказаться полезным для специфического воздействия на течение и других интоксикаций, при которых нарушается обмен данного медиатора.[98]
В последнее время для лечения различных нарушений функционирования центральной нервной системы все больше используется гаммалон — препарат гамма-амино-масляной кислоты. Его назначают внутрь в таблетках по 0,25 г и для введения в вену в виде 5%-ного раствора. Можно предположить, что этот препарат найдет практическое применение и как заместительное антидотное средство в первую очередь при гидразиновых отравлениях.
Тот факт, что яды-ингибиторы моноаминоксидазы имеют химическое сродство к меди, входящей в состав данного фермента, давно наводил исследователей на мысль о применении этого микроэлемента при соответствующих отравлениях. И действительно, оказалось, что соединения меди, в частности уксусномедная соль, препятствуют развитию нарушений обмена веществ при сероуглеродной и гидразиновых интоксикациях, резко понижают накопление этих ядов и продуктов их превращений в организме, а также нормализуют метаболизм биогенных аминов. Все это, несомненно, свидетельствует о том, что препараты меди проявляют свойства антидотов. Вполне оправданы поэтому рекомендации по их практическому применению. Так, в настоящее время предписывается дополнительно вводить ацетат меди (совместно с пиридоксином) в рацион лечебно-профилактического питания лиц, контактирующих на производстве с сероуглеродом и другими дитиокарбаматами, а также обязательно включать его в комплекс антидотных средств при соответствующих интоксикациях.
Адреноблокаторы
Теоретически антидотньм эффектом при интоксикации ядами-ингибиторами пиридоксалевых ферментов должны обладать (по аналогии с холинолитиками) препараты, которые обратимо, но быстро и на достаточно длительный срок выключают адренорецепторы из механизма нервной передачи. Такими свойствами обладает большое число веществ, известных в фармакологии под названием адреноблокаторов. В зависимости от того, какой тип рецепторов преимущественно блокируется, их подразделяют на α- и β-адреноблокаторы. К первым относятся производные спорыньи (эрготамин, редергам), фентоламин, дибенамин, фенитрон. В числе вторых — пронеталол, индерал, дихлоризопротеренол, аптин, а также отечественный аналог индерала — анаприлин. Эти вещества, в особенности β-адреноблокаторы, все более широко используются в клинике внутренних болезнен при различных патологических состояниях (например, при болезнях сердечно-сосудистой системы). Можно с уверенностью предсказать их использование в качестве антидотов для снятия явлений перевозбуждения адренорецепторов.[99] Не исключено, что адреноблокаторы окажутся полезными и для профилактики отравлений ингибиторами моноаминоксидазы, а также веществами, непосредственно стимулирующими функцию адренорецепторов. В предполагаемом механизме действия адреноблокирующих антидотов можно усмотреть и структурный компонент. Это, например, иллюстрируется сопоставлением строения молекулы адреналина и β-адреноблокатора дихлоризопротеренола: Естественно поэтому предположить, что конкурентный антагонизм этих веществ основывается на присоединении их молекул к одним и тем же звеньям адренорецепторной структуры.
Таким образом, в перспективном плане адреноблокирующие соединения можно рассматривать как противоядия. Расширяющийся диапазон их терапевтического применения несомненно будет способствовать внедрению этих веществ в токсикологическую практику.
Естественно поэтому предположить, что конкурентный антагонизм этих веществ основывается на присоединении их молекул к одним и тем же звеньям адренорецепторной структуры.
Таким образом, в перспективном плане адреноблокирующие соединения можно рассматривать как противоядия. Расширяющийся диапазон их терапевтического применения несомненно будет способствовать внедрению этих веществ в токсикологическую практику.
Диэтиламид лизергиновой кислоты и его антагонисты
В связи с разбирающимися токсическими нарушениями функционирования адренергических систем заслуживают отдельного рассмотрения некоторые психотомиметические вещества. Прежде всего это достаточно хорошо известный диэтиламид лизергиновой кислоты (ДЛК): ДЛК — полусинтетическое вещество, полученное из ржаной спорыньи, которое завоевало за последние десятилетия в семействе психоядов главенствующее положение. Прошло уже более 35 лет с тех пор, как швейцарский фармаколог Гоффманн стал объектом случайного токсического воздействия ДЛК, несколько миллиграммов которого ему до этого удалось получить в виде кристаллического вещества. Поставив на себе опыт, Гоффман обнаружил, что в дозе 0,25 мг ДЛК вызывает многообразные остро протекающие расстройства психики: нарушается восприятие окружающей среды и своего тела, появляются различные галлюцинации, искажается эмоциональная деятельность и ориентация во времени и месте. В дальнейшем было выяснено, что ДЛК может привести также к развитию маниакального состояния, психомоторному возбуждению, бреду. В настоящее время считается, что действующая доза ДЛК для человека равна 0,07–0,15 мг, при этом психотоксический эффект отмечается в течение 4–6 ч.[100]
На механизм действия психотомиметических ядов типа ДЛК на центральную нервную систему не существует однозначного взгляда. Считается, что в минимальных дозах эти вещества прекращают действие серотонина, вытесняя его с поверхности рецептора и вступая с ним, таким образом, в конкурентные отношения. С другой стороны, имеются данные за то, что большие дозы препаратов типа ДЛК, блокируя моноаминоксидазу, препятствуют нормальному окислению серотонина и катехоламинов и способствуют их накоплению в синапсах. Высказывается также мнение, что ДЛК повышает чувствительность центральных адренергических рецепторов к действию свободных медиаторов. Поэтому предполагается, что в зависимости от дозы ДЛК либо тормозится, либо усиливается действие медиаторов на адренорецепторы. Все это ведет к па рушению нормального проведения импульсов в адренергических структурах центральной нервной системы, что и рассматривается как биохимическая основа тех или иных психических расстройств.[101] В последние годы все чаще подчеркивается значение нарушений при интоксикации ДЛК нормального процесса биотрансформации адреналина и норадреналина. Это приводит к превращению их в адренохром и адренолютин — вещества, одновременно близкие по структуре к серотонину и к некоторым психотомиметическим агентам (псилоцину, буфотенину и другим производным аминокислоты триптамина):
ДЛК — полусинтетическое вещество, полученное из ржаной спорыньи, которое завоевало за последние десятилетия в семействе психоядов главенствующее положение. Прошло уже более 35 лет с тех пор, как швейцарский фармаколог Гоффманн стал объектом случайного токсического воздействия ДЛК, несколько миллиграммов которого ему до этого удалось получить в виде кристаллического вещества. Поставив на себе опыт, Гоффман обнаружил, что в дозе 0,25 мг ДЛК вызывает многообразные остро протекающие расстройства психики: нарушается восприятие окружающей среды и своего тела, появляются различные галлюцинации, искажается эмоциональная деятельность и ориентация во времени и месте. В дальнейшем было выяснено, что ДЛК может привести также к развитию маниакального состояния, психомоторному возбуждению, бреду. В настоящее время считается, что действующая доза ДЛК для человека равна 0,07–0,15 мг, при этом психотоксический эффект отмечается в течение 4–6 ч.[100]
На механизм действия психотомиметических ядов типа ДЛК на центральную нервную систему не существует однозначного взгляда. Считается, что в минимальных дозах эти вещества прекращают действие серотонина, вытесняя его с поверхности рецептора и вступая с ним, таким образом, в конкурентные отношения. С другой стороны, имеются данные за то, что большие дозы препаратов типа ДЛК, блокируя моноаминоксидазу, препятствуют нормальному окислению серотонина и катехоламинов и способствуют их накоплению в синапсах. Высказывается также мнение, что ДЛК повышает чувствительность центральных адренергических рецепторов к действию свободных медиаторов. Поэтому предполагается, что в зависимости от дозы ДЛК либо тормозится, либо усиливается действие медиаторов на адренорецепторы. Все это ведет к па рушению нормального проведения импульсов в адренергических структурах центральной нервной системы, что и рассматривается как биохимическая основа тех или иных психических расстройств.[101] В последние годы все чаще подчеркивается значение нарушений при интоксикации ДЛК нормального процесса биотрансформации адреналина и норадреналина. Это приводит к превращению их в адренохром и адренолютин — вещества, одновременно близкие по структуре к серотонину и к некоторым психотомиметическим агентам (псилоцину, буфотенину и другим производным аминокислоты триптамина):
 В эксперименте на людях было доказано, что адренохром и адренолютин вызывают психические расстройства. В этой связи интересно предположение о механизме действия другого психотомиметика — мескалина, алкалоида мексиканского кактуса лофофора. Оказалось, что в процессе превращений в организме норадреналина, в частности при его метилировании, могут образовываться вещества, весьма сходные по строению с мескалином. Вполне логично предположить, что и реакции метаболизма мескалина (тот же процесс метилирования) имеют связь со структурными превращениями данного медиатора и должны рассматриваться как звенья единого биохимического механизма нарушений психической деятельности.
Изысканию антигаллюциногенных средств посвящено большое число как отечественных, так и зарубежных исследований. Так, весьма результативными оказались испытания различных фармакологических препаратов на крысах, у которых вызывался лизергиновый психоз.[102] В частности, было установлено, что предварительное (за 2 ч до отравления ДЛК) введение животным α- и β-адреноблокаторов заметно снижало у них выраженность нарушений поведения и двигательных расстройств, причем α-адреноблокатор феноксибензамин оказался наиболее эффективным антагонистом ДЛК. β-Адреноблокаторы пронеталол и индерал также нормализовали извращенное поведение животных, но в отличие от феноксибензамина почти не уменьшали двигательного возбуждения. В этой связи представляет интерес работа, выполненная О. Н. Давыдовой[103] в лаборатории профессора А. Н. Кудрина. В опытах на кошках была показана высокая противолизергиновая активность α-адреноблокатора фенитрона. Действие этого препарата особенно было выражено при предварительном или одновременном его введении животным с токсичными дозами ДЛК. Автором было также установлено, что фенитрон является активным антагонистом другого весьма распространенного психотоксического вещества — гашиша.
Из веществ, испытанных в качестве антагонистов ДЛК, следует назвать α-метилпаратирозин, который оказался сильным ангибитором синтеза катехоламинов в головном мозге. Этот препарат отчетливо препятствовал развитию лизергиновой интоксикации при введении животным за несколько часов до отравления, а также нормализовал расстройства поведения, если его вводили животным через 20–30 мин после ДЛК.
Пока еще нет опыта, позволяющего оценить практическую значимость представленных подходов к специфическому лекарственному воздействию на лизергиновые интоксикации. Однако определенные положительные сдвиги в этом направлении уже намечаются. Так, один из испытанных Диксоном (США) препаратов — дезерил, вмешивающийся в функцию центральных серотониновых структур, был с успехом использован для нормализации психической деятельности у больных.[104] Другой препарат подобного типа действия — мексамин (5-метокситриптамин):
В эксперименте на людях было доказано, что адренохром и адренолютин вызывают психические расстройства. В этой связи интересно предположение о механизме действия другого психотомиметика — мескалина, алкалоида мексиканского кактуса лофофора. Оказалось, что в процессе превращений в организме норадреналина, в частности при его метилировании, могут образовываться вещества, весьма сходные по строению с мескалином. Вполне логично предположить, что и реакции метаболизма мескалина (тот же процесс метилирования) имеют связь со структурными превращениями данного медиатора и должны рассматриваться как звенья единого биохимического механизма нарушений психической деятельности.
Изысканию антигаллюциногенных средств посвящено большое число как отечественных, так и зарубежных исследований. Так, весьма результативными оказались испытания различных фармакологических препаратов на крысах, у которых вызывался лизергиновый психоз.[102] В частности, было установлено, что предварительное (за 2 ч до отравления ДЛК) введение животным α- и β-адреноблокаторов заметно снижало у них выраженность нарушений поведения и двигательных расстройств, причем α-адреноблокатор феноксибензамин оказался наиболее эффективным антагонистом ДЛК. β-Адреноблокаторы пронеталол и индерал также нормализовали извращенное поведение животных, но в отличие от феноксибензамина почти не уменьшали двигательного возбуждения. В этой связи представляет интерес работа, выполненная О. Н. Давыдовой[103] в лаборатории профессора А. Н. Кудрина. В опытах на кошках была показана высокая противолизергиновая активность α-адреноблокатора фенитрона. Действие этого препарата особенно было выражено при предварительном или одновременном его введении животным с токсичными дозами ДЛК. Автором было также установлено, что фенитрон является активным антагонистом другого весьма распространенного психотоксического вещества — гашиша.
Из веществ, испытанных в качестве антагонистов ДЛК, следует назвать α-метилпаратирозин, который оказался сильным ангибитором синтеза катехоламинов в головном мозге. Этот препарат отчетливо препятствовал развитию лизергиновой интоксикации при введении животным за несколько часов до отравления, а также нормализовал расстройства поведения, если его вводили животным через 20–30 мин после ДЛК.
Пока еще нет опыта, позволяющего оценить практическую значимость представленных подходов к специфическому лекарственному воздействию на лизергиновые интоксикации. Однако определенные положительные сдвиги в этом направлении уже намечаются. Так, один из испытанных Диксоном (США) препаратов — дезерил, вмешивающийся в функцию центральных серотониновых структур, был с успехом использован для нормализации психической деятельности у больных.[104] Другой препарат подобного типа действия — мексамин (5-метокситриптамин):
 Будучи структурным аналогом серотонина, мексамин в отличие от него преодолевает гематоэнцефалический барьер и проникает в головной мозг. В опытах на собаках профессор Г. И. Мильштейн[105] установил, что мексамин является эффективным антагонистом ДЛК. Это, по мнению автора, косвенно доказывает, что лизергиновый психоз является результатом нарушений в обмене серотонина. В этой связи практическую ценность имели данные Р. Б. Стрелкова и В. А. Хасабовой,[106] которые доказали (авторы ставили опыты на себе и на добровольцах) переносимость больших доз мексамина (до 6,5 мг/кг при приеме внутрь), что дало основания для дальнейшего испытания этого препарата как возможного антидота ДЛК.
Пример с мексамином еще раз подтверждает научное значение известного положения, выдвинутого академиком АМН СССР В. М. Карасином: «Несомненно, что любая фармакологическая реакция имеет биохимический прототип: чуждый организму химический агент лишь в том случае может вступить в реакцию с той или иной биохимической структурой, если по своему химическому строению или поведению он сходен с каким-либо веществом, свойственным организму».[107]
Будучи структурным аналогом серотонина, мексамин в отличие от него преодолевает гематоэнцефалический барьер и проникает в головной мозг. В опытах на собаках профессор Г. И. Мильштейн[105] установил, что мексамин является эффективным антагонистом ДЛК. Это, по мнению автора, косвенно доказывает, что лизергиновый психоз является результатом нарушений в обмене серотонина. В этой связи практическую ценность имели данные Р. Б. Стрелкова и В. А. Хасабовой,[106] которые доказали (авторы ставили опыты на себе и на добровольцах) переносимость больших доз мексамина (до 6,5 мг/кг при приеме внутрь), что дало основания для дальнейшего испытания этого препарата как возможного антидота ДЛК.
Пример с мексамином еще раз подтверждает научное значение известного положения, выдвинутого академиком АМН СССР В. М. Карасином: «Несомненно, что любая фармакологическая реакция имеет биохимический прототип: чуждый организму химический агент лишь в том случае может вступить в реакцию с той или иной биохимической структурой, если по своему химическому строению или поведению он сходен с каким-либо веществом, свойственным организму».[107]
ГЛАВА 4 Тиоловые яды и их противоядия
На производстве и в быту современный человек довольно часто сталкивается с так называемыми тиоловыми ядами — ртутью, свинцом, мышьяком, кадмием, сурьмой и др. Некоторые из этих веществ входят в состав лекарственных препаратов. Всех их объединяет избирательная способность вступать в химическое взаимодействие с сульфгидрильными (-SH), или тиоловыми, группами различных макромолекул организма, в первую очередь — ферментных и других белковых структур, а также некоторых аминокислот. Сульфгидрильным соединениям[108] приписывается исключительная роль в осуществлении биохимических процессов и поддержании жизнедеятельности. Теперь известно более 100 ферментов, активность которых может тормозиться при блокировании в их молекулах SH-групп.[109] С веществами, содержащими сульфгидрильные группы, связано проведение нервного импульса, тканевое дыхание, мышечное сокращение, проницаемость клеточных мембран и другие важнейшие функции. Вот почему избирательное сродство ядовитых соединений к SH-группам приводит к блокированию (нарушению) течения ряда биохимических процессов, что и лежит в основе развития соответствующих отравлений.Яды — блокаторы сульфгидрильных групп биомолекул
Ртуть. В чистом виде применяется в производстве некоторых медицинских и других препаратов, взрывчатых веществ (гремучая ртуть), ядохимикатов (гранозан), а также для заполнения термометров, барометров и других измерительных приборов. Промышленное значение имеют высокотоксичные неорганические соединения ртути, в частности сулема (HgCl2), из которой получают другие ртутные соединения и которая применяется при травлении стали. Сулема вызывает смертельные отравления при приеме внутрь в количестве 0,2–0,3 г. Пары ртути, пыль ее соединений, проникая в организм, поражают желудочно-кишечный тракт, почки, нервную систему с характерным развитием при тяжелых интоксикациях психических и двигательных расстройств. Ртуть и ее соединения постепенно выводятся из организма (элиминируются) почками и железами внешней секреции, в том числе молочными. Оценивая динамику выделения ртути, можно, во-первых, судить о течении интоксикации,[110] а во-вторых, — об эффективности проводимого лечения. Свинец. Достаточно назвать производство аккумуляторов, полиграфическое дело, изготовление свинцовых красок, эмали, глазури, чтобы представить, насколько реальны вредности, связанные со свинцом. Источником бытовых отравлений, к примеру, могут стать пища и вода, длительно хранившиеся в посуде, покрытой свинцовой глазурью. Тяжелое отравление возникает при приеме внутрь от 2 до 3 г солей свинца, в частности ацетата. Проникший в организм свинец быстро обнаруживается почти во всех органах и тканях, ко основная его часть фиксируется в эритроцитах и костях. В наибольшей степени свинец поражает нервную систему, кроветворение, желудочно-кишечный тракт, печень. Особенно характерны свинцовые полиневриты и параличи, анемия, схваткообразные боли в животе («свинцовая колика»), спазм кровеносных сосудов. Элиминация свинца осуществляется, подобно ртути, главным образом через почки и кишечник. Мышьяк. Соединения мышьяка применяются в стекольной, красильной, кожевенной, фармацевтической и других отраслях промышленности. Чистый металлический мышьяк малотоксичен, но его окислы и соли — сильные яды; особенно ядовит мышьяковистый ангидрид, или белый мышьяк (As2O3), который вызывает смертельное отравление в дозе 60–70 мг. Чаще всего соединения мышьяка проникают в организм в виде пыли и с зараженной пищей и водой. Они могут длительно фиксироваться в костях, печени, волосах,[111] коже. Мышьяковая интоксикация в основном проявляется нарастающим снижением кровяного давления, повышением проницаемости стенок сосудов для форменных элементов крови, различными признаками поражения центральной нервной системы вплоть до развития судорожно-паралитического синдрома, а также резкими расстройствами обменных процессов. Кадмий. Чистый кадмий, его соли и кислоты широко применяются в электроплавильном, аккумуляторном, электролитическом производстве, при изготовлении красок, люминофоров, а также в ядерных энергетических установках как поглотитель нейтронов. 50–60 мг кадмия при приеме внутрь вызывают смертельное отравление. Особо токсичны CdO и CdSO4, которые, поступая в организм в виде паров, дыма или пыли, поражают органы дыхания (судорожный кашель, одышка, отек легких), желудочно-кишечный тракт (рвота, понос), печень и почки. При этом нарушается фосфорно-кальциевый и белковый обмен, что, в частности, снижает прочность костей и приводит к выведению белков плазмы через почки (протеинурия). Сурьма. В чистом виде применяется при изготовлении различных сплавов. Окислы сурьмы используются для изготовленияогнестойких текстильных материалов, огнеупорных красок, эмали, керамики, а различные ее соли (сульфиты, хлориды) — для окрашивания металлических изделий, вулканизации каучука, производства спичек, в пиротехнике. При обработке кислотами металлов, содержащих сурьму, выделяется ядовитый газ — стибин (SbH3). Сурьма и ее соединения поступают в организм главным образом через органы дыхания, они могут длительно задерживаться в печени, коже, волосах. Острое отравление проявляется сильным раздражением слизистых оболочек глаз и верхних дыхательных путей, может наблюдаться поражение желудочно-кишечного тракта, центральной нервной системы, печени, почек. Соединения трехвалентной сурьмы, в первую очередь стибин, вызывают поражение крови (анемия), желтуху. Надо отметить, что одним из источников опасного воздействия названных и других ядовитых металлов на организм человека является все возрастающее загрязнение водоемов промышленными сточными водами. В одном из специальных отчетов Всемирной организации здравоохранения указывается на постоянно увеличивающееся содержание в реках и озерах таких особо ядовитых химических элементов, как мышьяк, кадмий, хром, свинец, ртуть, селен, ванадий. Так, например, одна из наиболее мощных рек Западной Европы — Рейн, протекающая по территории шести государств, давно уже загрязнена, вода ее мало пригодна для питья и хозяйственных целей, а большинство городов, расположенных на берегах этой реки, снабжается подрусловыми водами.[112] Это же можно сказать о Великих озерах и реке Миссисипи в США и о многих других водоемах. Но, пожалуй, в наибольшей степени от загрязнения водоемов сточными водами страдают жители Японии, где экономическая плотность, т. е. отношение выпуска промышленной продукции к площади удобной земли, в 10–12 раз превосходит аналогичный показатель других высокоразвитых стран. В этой стране, в частности, были отмечены массовые ртутные отравления из-за употребления в пищу зараженной рыбы (залив Минамата), а также тяжелые поражения нескольких сотен людей кадмием, который проник в почву и воду (бассейн р. Джинцу) из расположенных поблизости плавилен и шахт.[113] Здесь уместно вспомнить о громадных количествах токсичных веществ, которые проникают в Мировой океан из атмосферы. Подсчеты показывают, что на его поверхность выпадает, в частности, ежегодно до 200 тыс. тонн свинца и 5 тыс. тонн ртути. Это, естественно, приводит к неблагоприятному воздействию на животные и растительные морские организмы. Так, например, в прибрежных водах Скандинавских стран отмечено значительное увеличение содержания ртути (до 1 мг на 1 кг биомассы), что сделало непригодными к употреблению многие виды рыб.[114] Аналогичная ситуация складывается в заливах и морях, омывающих Японские острова, США и другие промышленно развитые страны.Механизмы действия тиоловых ядов
Каков же общий механизм взаимодействия ядов с сульфгидрильными соединениями? Прежде всего надо отметить, что в результате реакции ионов металлов с SH-группами образуются слабо диссоциирующие и, как правило, нерастворимые соединения — меркаптиды. При этом одновалентные металлы реагируют по такой общей схеме: R-SH+Ме+→R-S-Ме+Н+ Если металлический ион двухвалентный, то он блокирует одномоментно две SH-группы: Помимо этого основного способа ингибирования сульфгидрильные группы белков и аминокислот могут легко окисляться. Это чаще всего происходит при их контакте с различными акцепторами электронов (например, с перекисями, хинонами, йодом) и приводит к образованию дисульфидов — веществ типа R-S-S-R. Инактивация сульфгидрильных групп может также вызываться рядом органических галоидных соединений посредством необратимого замещения водорода в радикале SH на углеродный радикал с образованием прочной сероуглеродной (-S-С-) связи. Различные тяжелые металлы обладают разным химическим сродством к сульфгидрильным группам. Сильнее всего оно выражено у ртути, трехвалентного мышьяка, серебра, а также у свинца и трехвалентной сурьмы.[115]
В связи с особой токсикологической значимостью реакции образования меркантидов интересно рассмотреть механизм токсического действия люизита (хлорвинилди-хлорарсина) — весьма ядовитого производного трехвалентного мышьяка, синтезированного в Германии и в США в конце первой мировой войны. В последующие годы этот яд военной химии продолжал вызывать к себе интерес токсикологов из-за возможности использования его в качестве отравляющего вещества. Вот почему во время второй мировой войны в некоторых странах велись поиски специфического противолюизитного препарата. Такой антидот был создан в Англии в середине 40-х годов в лаборатории Питерса.[116] Успешному испытанию препарата предшествовало раскрытие механизма действия люизита. Оказалось, что этот яд наиболее выраженно тормозит углеводный обмен, причем особенно уязвимыми являются реакции окислительного декарбоксилирования одного из конечных продуктов распада Сахаров в организме — пировиноградной кислоты. Данное звено обмена катализируется пируватоксидазной группой ферментов, важнейшим компонентом (кофактором) которых является дигидролипоевая кислота. При взаимодействии люизита с этим веществом образуется циклический меркаптид:
Помимо этого основного способа ингибирования сульфгидрильные группы белков и аминокислот могут легко окисляться. Это чаще всего происходит при их контакте с различными акцепторами электронов (например, с перекисями, хинонами, йодом) и приводит к образованию дисульфидов — веществ типа R-S-S-R. Инактивация сульфгидрильных групп может также вызываться рядом органических галоидных соединений посредством необратимого замещения водорода в радикале SH на углеродный радикал с образованием прочной сероуглеродной (-S-С-) связи. Различные тяжелые металлы обладают разным химическим сродством к сульфгидрильным группам. Сильнее всего оно выражено у ртути, трехвалентного мышьяка, серебра, а также у свинца и трехвалентной сурьмы.[115]
В связи с особой токсикологической значимостью реакции образования меркантидов интересно рассмотреть механизм токсического действия люизита (хлорвинилди-хлорарсина) — весьма ядовитого производного трехвалентного мышьяка, синтезированного в Германии и в США в конце первой мировой войны. В последующие годы этот яд военной химии продолжал вызывать к себе интерес токсикологов из-за возможности использования его в качестве отравляющего вещества. Вот почему во время второй мировой войны в некоторых странах велись поиски специфического противолюизитного препарата. Такой антидот был создан в Англии в середине 40-х годов в лаборатории Питерса.[116] Успешному испытанию препарата предшествовало раскрытие механизма действия люизита. Оказалось, что этот яд наиболее выраженно тормозит углеводный обмен, причем особенно уязвимыми являются реакции окислительного декарбоксилирования одного из конечных продуктов распада Сахаров в организме — пировиноградной кислоты. Данное звено обмена катализируется пируватоксидазной группой ферментов, важнейшим компонентом (кофактором) которых является дигидролипоевая кислота. При взаимодействии люизита с этим веществом образуется циклический меркаптид:
 Можно думать, что блокирование дигидролипоевой кислоты облегчается пространственным соответствием SH-групп в ее молекуле и атомов хлора при мышьяке люизита.
Можно думать, что блокирование дигидролипоевой кислоты облегчается пространственным соответствием SH-групп в ее молекуле и атомов хлора при мышьяке люизита.
Дитиоловые антидоты
Британский антилюизит
Основываясь на таком механизме действия люизита, естественно предположить, что образование подобного комплекса «яд-рецептор» произойдет и тогда, когда вместо дигидролипоевой кислоты в реакции будет участвовать другой дитиол, т. е. соединение, содержащее 2 близко расположенные SH-группы, Именно из этого исходили Питерс и его сотрудники, когда вели поиск противолюизитного препарата. За его основу они взяли трехатомный спирт глицерин, в молекулу которого вместо двух рядом расположенных гидроксилов ввели 2 тиоловые группы. Так был синтезирован 2,3-димеркаптопропанол, получивший название британского антилюизита (БАЛ):[117] Нетрудно представить, что если в реакции с люизитом вместо дигидролиноевой кислоты будет участвовать 2,3-димеркаyтопропанол, то обе его SH-группы вступят в реакцию образования циклического меркантида. Оказалось, что последний является более прочным соединением, чем комплекс «яд-фермент». Иными словами, в итоге конкуренции за связь с ядом естественного и искусственного донатора тиоловых групп второй из них оказывается более эффективным средством детоксикации люизита. Но если бы действие антидота реализовалось только по такой схеме, то оно проявлялось бы при наличии в организме лишь свободных молекул яда. На самом деле БАЛ способен разрушать комплекс «яд-рецептор» и тем реактивировать дигидролиноевую кислоту:
Нетрудно представить, что если в реакции с люизитом вместо дигидролиноевой кислоты будет участвовать 2,3-димеркаyтопропанол, то обе его SH-группы вступят в реакцию образования циклического меркантида. Оказалось, что последний является более прочным соединением, чем комплекс «яд-фермент». Иными словами, в итоге конкуренции за связь с ядом естественного и искусственного донатора тиоловых групп второй из них оказывается более эффективным средством детоксикации люизита. Но если бы действие антидота реализовалось только по такой схеме, то оно проявлялось бы при наличии в организме лишь свободных молекул яда. На самом деле БАЛ способен разрушать комплекс «яд-рецептор» и тем реактивировать дигидролиноевую кислоту:
 Нарастающее образование недиссоциирующего и малотоксичного комплексного соединения «яд-антидот» сдвигает установившееся равновесие между ядом и ферментом в сторону введенного антидота. К тому же необходимо учитывать, что связанный с антидотом яд постепенно выводится из организма через кишечник и почки. Это ценное свойство димеркаптопропанола, которое роднит его с реактиваторама холинэстераз, позволяет бороться с интоксикациями в выраженных их стадиях. Но значение его состоит не только и не столько в антидотных свойствах по отношению к люизиту, интоксикации которым весьма проблематичны. Главное — это способность димеркаптопропанола обезвреживать многие другие тиоловые яды, с которыми контактирует современный человек. Вот почему приходится считаться и с некоторыми отрицательными сторонами БАЛа как лечебного препарата. Во-первых, небольшая широта терапевтического действия[118] не позволяет его использовать в больших дозах (сотые доли грамма — лечебная доза, десятые доли грамма — токсическая). Во-вторых, плохая растворимость в воде заставляет вводить антидот в специальных масляных растворах, что затрудняет всасывание его в кровь и существенно замедляет лечебное действие. Эти обстоятельства, а также расширяющиеся возможности контакта многих людей с тиоловымя веществами на производстве и в повседневной жизни вызвали необходимость усовершенствования британского антилюизита.
Нарастающее образование недиссоциирующего и малотоксичного комплексного соединения «яд-антидот» сдвигает установившееся равновесие между ядом и ферментом в сторону введенного антидота. К тому же необходимо учитывать, что связанный с антидотом яд постепенно выводится из организма через кишечник и почки. Это ценное свойство димеркаптопропанола, которое роднит его с реактиваторама холинэстераз, позволяет бороться с интоксикациями в выраженных их стадиях. Но значение его состоит не только и не столько в антидотных свойствах по отношению к люизиту, интоксикации которым весьма проблематичны. Главное — это способность димеркаптопропанола обезвреживать многие другие тиоловые яды, с которыми контактирует современный человек. Вот почему приходится считаться и с некоторыми отрицательными сторонами БАЛа как лечебного препарата. Во-первых, небольшая широта терапевтического действия[118] не позволяет его использовать в больших дозах (сотые доли грамма — лечебная доза, десятые доли грамма — токсическая). Во-вторых, плохая растворимость в воде заставляет вводить антидот в специальных масляных растворах, что затрудняет всасывание его в кровь и существенно замедляет лечебное действие. Эти обстоятельства, а также расширяющиеся возможности контакта многих людей с тиоловымя веществами на производстве и в повседневной жизни вызвали необходимость усовершенствования британского антилюизита.
Унитиол
В начале 50-х годов киевскими токсикологами и химиками под руководством академика АМН СССР А. И. Черкеса и профессора В. Е. Петрунькина был синтезирован и с успехом испытан отечественный препарат унитиол. По своему химическому строению он отличается от БАЛа только тем, что его гидроксил замещен на радикал S03Na и молекула подверглась гидратации. Следовательно, унитиол — это 2,3-димеркантопропансульфонат натрия: Но именно это небольшое изменение структуры сделало унитиол хорошо растворимым в воде и одновременно значительно усилило его антидотную активность в сравнении с димеркаптопропанолом.[119] Унитиол прочно вошел в арсенал антидотно-лечебных средств, и теперь уже накоплен большой опыт успешного его использования при отравлениях различными соединениями мышьяка, ртути, свинца, кадмия, никеля, хрома, кобальта, ряда радиоактивных элементов.[120]Вот как, например, реагирует унитиол с сулемой:
Но именно это небольшое изменение структуры сделало унитиол хорошо растворимым в воде и одновременно значительно усилило его антидотную активность в сравнении с димеркаптопропанолом.[119] Унитиол прочно вошел в арсенал антидотно-лечебных средств, и теперь уже накоплен большой опыт успешного его использования при отравлениях различными соединениями мышьяка, ртути, свинца, кадмия, никеля, хрома, кобальта, ряда радиоактивных элементов.[120]Вот как, например, реагирует унитиол с сулемой:
 В известной мере эта реакция может считаться общей схемой детоксикации дитиолами солей и других ядовитых соединений двухвалентных металлов (например, окислов). Такого типа комплексы образуются при взаимодействии эквивалентных количеств унитиола и ионов металла. Однако ртуть, кадмий и другие элементы могут давать и укрупненные комплексы, если соединение «унитиол-металл» вступает в реакцию с дополнительной молекулой антидота:
В известной мере эта реакция может считаться общей схемой детоксикации дитиолами солей и других ядовитых соединений двухвалентных металлов (например, окислов). Такого типа комплексы образуются при взаимодействии эквивалентных количеств унитиола и ионов металла. Однако ртуть, кадмий и другие элементы могут давать и укрупненные комплексы, если соединение «унитиол-металл» вступает в реакцию с дополнительной молекулой антидота:
 Весьма эффективным оказалось применение унитиола при интоксикации ртутьорганическими ядохимикатами, в частности гранозаном, действующее начало которого — этилмеркурхлорид — содержит до 75% ртути. Так, в литературе сообщалось об успешном лечении 6 лиц, отравившихся хлебом из зерна, протравленного этим фунгицидом. В то же время 3 человека с подобной интоксикацией, не лечившихся унитиолом, погибли.[121] Частым источником гранозановых интоксикаций (особенно у детей) становится употребление протравленных семян подсолнечника. Гранозан очень медленно выводится из организма, что, в частности, создает возможности заражения грудных детей через молоко матери.
Весьма эффективным оказалось применение унитиола при интоксикации ртутьорганическими ядохимикатами, в частности гранозаном, действующее начало которого — этилмеркурхлорид — содержит до 75% ртути. Так, в литературе сообщалось об успешном лечении 6 лиц, отравившихся хлебом из зерна, протравленного этим фунгицидом. В то же время 3 человека с подобной интоксикацией, не лечившихся унитиолом, погибли.[121] Частым источником гранозановых интоксикаций (особенно у детей) становится употребление протравленных семян подсолнечника. Гранозан очень медленно выводится из организма, что, в частности, создает возможности заражения грудных детей через молоко матери.

Рис. 11. Результаты лечения унитиолом кроликов (% выживших животных), отравленных мышьяком, ртутью и кадмием в дозах, дающих 80% смертности у полеченных животных (Бравер-Чернобульская, Белоножко, 1959)
В разработку антидотных методов лечения и профилактики интоксикаций ртутьорганическими соединениями внесли вклад труды профессора С. И. Ашбеля (г. Горький) и его сотрудников. Так, имя был успешно применен унитиол в виде аэрозоля с помощью оригинальных аэрозольингаляционных установок. Авторы обосновывают такой метод антидотной терапии тем, что вследствие поступления ртутьорганических ядохимикатов в организм через легкие (при их производстве и применении) последние становятся основным депо этого яда.[122] Вдыхание унитиолового аэрозоля показано и при выполнении работы в условиях возможного воздействия этих веществ на организм (т. е. профилактически), тем более при малейшем подозрении на начинающуюся интоксикацию. Вообще ингаляционный метод введения антидота в организм находит применение также и для лечения и профилактики интоксикаций другими ядами. Эффективность унитиола можно еще проиллюстрировать экспериментальными данными (рис. 11). И все же, несмотря на многие положительные свойства, унитиол как лечебный препарат не свободен и от недостатков. Многолетний опыт его применения свидетельствует, что при передозировке или повышенной чувствительности к нему организма могут возникнуть головная боль, снижение кровяного давления, появиться сыпь. Кроме того, длительное использование унитиола приводит к усиленному выведению из организма таких микроэлементов, как медь и марганец. Вот почему вполне оправданными стали поиски дитиоловых антидотных средств, которые бы были лишены нежелательного побочного действия.Димеркаптоянтарная кислота (сукцимер)
Одним из таких препаратов оказалась димеркапто-янтарная кислота (ДМЯ): , синтезированная В. Л. Ниренбург на кафедре органической химии Уральского политехнического института. То, что ДМЯ проявляет четко выраженное защитное действие при отравлении животных соединениями мышьяка и ртути, было впервые показано И. Е. Оконишниковой (1962 г.). Наличие двух рядом расположенных SH-групп приводит при ее взаимодействии с тиоловыми ядами к образованию такого же нетоксичного комплекса, какой формировался при использовании унитиола и других подобных антидотов. В последующем антидотные свойства ДМЯ были подтверждены серией убедительных экспериментов, которые, в частности, показали, что она является надежным противоядием при отравлении животных мышьяксодержащими веществами, в том числе лекарственными (новар-сенолом и др.).[123] Так, если ДМЯ вводилась не позднее чем через 2 ч после отравления абсолютно смертельными дозами мышьяковых ядов, то выживало от 80 до 100% подопытных животных. Если ее вводили в организм за 15 мин до отравления, то выживало 100% животных. ДМЯ имеет большую терапевтическую широту и лишена какого-либо нежелательного побочного действия. При ее применении отмечена большая скорость выведения мышьяка из организма отравленных животных, чем под влиянием унитиола. Как положительное свойство ДМЯ следует отметить, что она включает активный метаболит — янтарную кислоту, активирующую ряд ферментных процессов при интоксикации тиоловыми ядами. Все это позволило рекомендовать ДМЯ в качестве антидота, который в лечебной практике получил новое название — сукцимер.[124]
, синтезированная В. Л. Ниренбург на кафедре органической химии Уральского политехнического института. То, что ДМЯ проявляет четко выраженное защитное действие при отравлении животных соединениями мышьяка и ртути, было впервые показано И. Е. Оконишниковой (1962 г.). Наличие двух рядом расположенных SH-групп приводит при ее взаимодействии с тиоловыми ядами к образованию такого же нетоксичного комплекса, какой формировался при использовании унитиола и других подобных антидотов. В последующем антидотные свойства ДМЯ были подтверждены серией убедительных экспериментов, которые, в частности, показали, что она является надежным противоядием при отравлении животных мышьяксодержащими веществами, в том числе лекарственными (новар-сенолом и др.).[123] Так, если ДМЯ вводилась не позднее чем через 2 ч после отравления абсолютно смертельными дозами мышьяковых ядов, то выживало от 80 до 100% подопытных животных. Если ее вводили в организм за 15 мин до отравления, то выживало 100% животных. ДМЯ имеет большую терапевтическую широту и лишена какого-либо нежелательного побочного действия. При ее применении отмечена большая скорость выведения мышьяка из организма отравленных животных, чем под влиянием унитиола. Как положительное свойство ДМЯ следует отметить, что она включает активный метаболит — янтарную кислоту, активирующую ряд ферментных процессов при интоксикации тиоловыми ядами. Все это позволило рекомендовать ДМЯ в качестве антидота, который в лечебной практике получил новое название — сукцимер.[124]
Липоевая кислота
Как дитиоловый антидот приобретает значение липоевая (тиоктовак) кислота — окисленная форма дигидролипоевой кислоты: Впервые она была выделена из печени животных в 1951 г. в лаборатории американского исследователя Рида, где в дальнейшем определили ее химическую структуру и синтезировали. В организме (ежедневная потребность в ней — 1–2 мг) липоевая кислота ферментативно быстро восстанавливается в дигидролипоевую кислоту с 2 активными сульфгидрильными группами, обладающими выраженными редуцирующими свойствами. Эксперименты на животных и лечебная практика свидетельствуют об определенной ее эффективности при отравлениях соединениями мышьяка, сурьмы и некоторыми другими подобными ядами.[125] Следует отметить значимость ее как ценного лекарственного препарата при ряде патологических состояний, связанных с нарушением обмена веществ, прежде всего углеводного и жирового, а также при заболеваниях печени. Постоянно присутствуя в крови и тканях организма и являясь «точкой приложения» тиоловых ядов, липоевая кислота на фоне интоксикации может проявлять себя, с одной стороны, как антидот прямого и реактивирующего действия, а с другой (и это важно подчеркнуть) — как заместительный антидот.
Остановимся еще на одном антидотном механизме, связанном с использованием сульфгидрильных соединений. Речь идет о специфическом лечении отравлений бромистым метилом (CH3Br) — одним из широко используемых средств борьбы с вредителями растений, сорняками и грызунами. Будучи очень токсичным для человека и теплокровных животных ядом судорожно-паралитического действия, — СH3Вr метилирует различные функциональные группы белков, в первую очередь -SH, -СООН, -NН2. Попытки использовать БАЛ, унитиол и другие вещества для лечения отравлений бромистым метилом оказались безуспешными. Единственным эффективным препаратом,; как было показано в опытах на кроликах и крысах, оказался важный биохимический компонент жизнедеятельности — аминокислота цистеин[126] (
Впервые она была выделена из печени животных в 1951 г. в лаборатории американского исследователя Рида, где в дальнейшем определили ее химическую структуру и синтезировали. В организме (ежедневная потребность в ней — 1–2 мг) липоевая кислота ферментативно быстро восстанавливается в дигидролипоевую кислоту с 2 активными сульфгидрильными группами, обладающими выраженными редуцирующими свойствами. Эксперименты на животных и лечебная практика свидетельствуют об определенной ее эффективности при отравлениях соединениями мышьяка, сурьмы и некоторыми другими подобными ядами.[125] Следует отметить значимость ее как ценного лекарственного препарата при ряде патологических состояний, связанных с нарушением обмена веществ, прежде всего углеводного и жирового, а также при заболеваниях печени. Постоянно присутствуя в крови и тканях организма и являясь «точкой приложения» тиоловых ядов, липоевая кислота на фоне интоксикации может проявлять себя, с одной стороны, как антидот прямого и реактивирующего действия, а с другой (и это важно подчеркнуть) — как заместительный антидот.
Остановимся еще на одном антидотном механизме, связанном с использованием сульфгидрильных соединений. Речь идет о специфическом лечении отравлений бромистым метилом (CH3Br) — одним из широко используемых средств борьбы с вредителями растений, сорняками и грызунами. Будучи очень токсичным для человека и теплокровных животных ядом судорожно-паралитического действия, — СH3Вr метилирует различные функциональные группы белков, в первую очередь -SH, -СООН, -NН2. Попытки использовать БАЛ, унитиол и другие вещества для лечения отравлений бромистым метилом оказались безуспешными. Единственным эффективным препаратом,; как было показано в опытах на кроликах и крысах, оказался важный биохимический компонент жизнедеятельности — аминокислота цистеин[126] ( ). При этом антидотные свойcтва цистеина связываются с наличием в его молекуле всех тех функциональных групп, которые угнетаются ядом. Эти химические радикалы препарата конкурентно взаимодействуют с активно метилирующим бромистым метилом. Иными словами, в организме цистеин берет на себя метальную группу СН3Вr, тем самым предохраняя от повреждения белковые структуры. Доступность и малая токсичность цистеина дали основание рекомендовать его в качестве антидота для практического применения.[127]
). При этом антидотные свойcтва цистеина связываются с наличием в его молекуле всех тех функциональных групп, которые угнетаются ядом. Эти химические радикалы препарата конкурентно взаимодействуют с активно метилирующим бромистым метилом. Иными словами, в организме цистеин берет на себя метальную группу СН3Вr, тем самым предохраняя от повреждения белковые структуры. Доступность и малая токсичность цистеина дали основание рекомендовать его в качестве антидота для практического применения.[127]
Комплексоны и их антидотное действие
В последние десятилетия наблюдается все возрастающий интерес токсикологов к особому классу химических соединений, получивших название комплексонов.[128] Эти вещества отличаются способностью образовывать прочные неионизирующие водорастворимые комплексы со многими неорганическими катионами, в том числе с тяжелыми металлами. Проникновение комплексонов в самые разнообразные отрасли производства, науки, медицины началось, по-видимому, в конце 30-х годов, когда этилен-диаминтетрауксусная кислота (ЭДТА) была запатентована германской фирмой «И. Г. Фарбениндустри» в качестве средства смягчения воды. Широкие исследования с использованием этих веществ начались у нас и за границей примерно с конца 40-х годов, когда стало ясно, что при их помощи можно ускорить выведение из организма токсичных металлов. Молекулы комплексонов практически не подвергаются расщеплению или какому-либо изменению в биологической среде, что является их важной фармакологической особенностью. В качестве антидотов среди комплексонов наибольшее распространение получили различные соли ЭДТА, которая имеет такое химическое строение: Как видно из приведенной формулы, ЭДТА — амино-поликарбоновая (четырехосновная) кислота, она способна образовывать прочные комплексные соединения со многими металлами. Однако сильнее это свойство проявляется у ее солей — натриевых, кальциевых, кобальтовых и др. Вот как протекает взаимодействие одного из наиболее распространенных комплексонов — тетацина (CaNa2ЭДТА) с ионами свинца:
Как видно из приведенной формулы, ЭДТА — амино-поликарбоновая (четырехосновная) кислота, она способна образовывать прочные комплексные соединения со многими металлами. Однако сильнее это свойство проявляется у ее солей — натриевых, кальциевых, кобальтовых и др. Вот как протекает взаимодействие одного из наиболее распространенных комплексонов — тетацина (CaNa2ЭДТА) с ионами свинца:
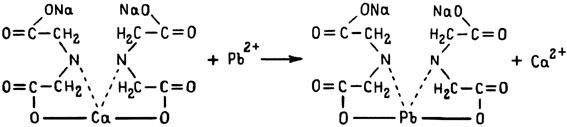 Из схемы следует, что в образовавшемся хелатном комплексе, как и в исходной соли СаNа2ЭДТА, металл (в данном случае Рb) связан не только валентными связями с карбоксильными группами, но и координационно — с атомами азота. Связь эта является прочной, она лишает яд присущей ему токсичности. СаNа2ЭДТА хорошо растворим в воде и потому легко выводится из организма через почки. Со времени первого лечебного использования тетацина при свинцовой интоксикации (1952 г.) этот комплексов нашел широкое применение в клинике профессиональных заболеваний[129] и продолжает оставаться незаменимым антидотом свинца и по сей день. Совершенно идентично тетацин обменивает ион кальция на ионы других двухвалентных металлов: ртути, кобальта, кадмия, бария. Он оказывает антидотное действие при введении в организм в виде 5%-ного или 10%-ного раствора, основой которого является физиологический раствор хлорида натрия или глюкозы, причем максимальная эффективная доза составляет 2 г препарата в сутки. Этот состав может использоваться и для промывания желудка отравленных с целью связывания яда, еще не всосавшегося в кровь. Очень эффективно применение СаNа2ЭДТА посредством аэроингаляция, когда антидот быстро всасывается и долго циркулирует в крови. Под влиянием аэрозоля CaNa2ЭДTA у отравленных отмечалось значительное усиление экскреции свинца почками, что свидетельствует о мобилизации металла из тканевых депо и переходе его в плазму крови.[130] Надо, однако, отметить, что в процессе комплексонотерапии возможно и некоторое усиление симптомов интоксикации, по-видимому, из-за увеличения обратного всасывания металла из пищеварительного тракта, куда он переходит через желчь и стенку кишечника из плазмы.
Обращает внимание структурное сходство разбираемой реакции с реакциями связывания яда молекулами дитиолов: в обоих случаях образуется замкнутая связь хелатного типа. Вот почему вполне оправдано причисление унитиола и других дитиолов к комплексообразующим антидотам. Но в отличие от соединения «яд-ЭДТА» соединение «яд-дитиол» мало или почти нерастворимо в воде, что уменьшает скорость его выведения из организма.
Помимо CaNa2ЭДTA практическое значение в качестве противоядий имеют и другие соли этилендиаминтетра-ацетата: СаЭДТА, Na2ЭДTA (трилон Б), Со2ЭДТА, а также производное диэтилентриаминпентоуксусной кислоты — СаNа3ДТПА (пентацин).[131] Так, при отравлении кальцием и его соединениями — СаО (негашеная известь), Са(ОН)2 (гашеная известь), СаС2 (карбид кальция) — показано применение трилона Б, молекулы которого присоединяя ионы Са2+, превращаются в тетацин:
Из схемы следует, что в образовавшемся хелатном комплексе, как и в исходной соли СаNа2ЭДТА, металл (в данном случае Рb) связан не только валентными связями с карбоксильными группами, но и координационно — с атомами азота. Связь эта является прочной, она лишает яд присущей ему токсичности. СаNа2ЭДТА хорошо растворим в воде и потому легко выводится из организма через почки. Со времени первого лечебного использования тетацина при свинцовой интоксикации (1952 г.) этот комплексов нашел широкое применение в клинике профессиональных заболеваний[129] и продолжает оставаться незаменимым антидотом свинца и по сей день. Совершенно идентично тетацин обменивает ион кальция на ионы других двухвалентных металлов: ртути, кобальта, кадмия, бария. Он оказывает антидотное действие при введении в организм в виде 5%-ного или 10%-ного раствора, основой которого является физиологический раствор хлорида натрия или глюкозы, причем максимальная эффективная доза составляет 2 г препарата в сутки. Этот состав может использоваться и для промывания желудка отравленных с целью связывания яда, еще не всосавшегося в кровь. Очень эффективно применение СаNа2ЭДТА посредством аэроингаляция, когда антидот быстро всасывается и долго циркулирует в крови. Под влиянием аэрозоля CaNa2ЭДTA у отравленных отмечалось значительное усиление экскреции свинца почками, что свидетельствует о мобилизации металла из тканевых депо и переходе его в плазму крови.[130] Надо, однако, отметить, что в процессе комплексонотерапии возможно и некоторое усиление симптомов интоксикации, по-видимому, из-за увеличения обратного всасывания металла из пищеварительного тракта, куда он переходит через желчь и стенку кишечника из плазмы.
Обращает внимание структурное сходство разбираемой реакции с реакциями связывания яда молекулами дитиолов: в обоих случаях образуется замкнутая связь хелатного типа. Вот почему вполне оправдано причисление унитиола и других дитиолов к комплексообразующим антидотам. Но в отличие от соединения «яд-ЭДТА» соединение «яд-дитиол» мало или почти нерастворимо в воде, что уменьшает скорость его выведения из организма.
Помимо CaNa2ЭДTA практическое значение в качестве противоядий имеют и другие соли этилендиаминтетра-ацетата: СаЭДТА, Na2ЭДTA (трилон Б), Со2ЭДТА, а также производное диэтилентриаминпентоуксусной кислоты — СаNа3ДТПА (пентацин).[131] Так, при отравлении кальцием и его соединениями — СаО (негашеная известь), Са(ОН)2 (гашеная известь), СаС2 (карбид кальция) — показано применение трилона Б, молекулы которого присоединяя ионы Са2+, превращаются в тетацин:
 Данные литературы последних 10–15 лет свидетельствуют о значительной антидотной эффективности при свинцовых отравлениях нового комплексообразующего вещества — D-пеницилламина (D-ПАМ), который представляет собою диметилцистеин, т. е. аминокислоту следующей химической структуры:
Данные литературы последних 10–15 лет свидетельствуют о значительной антидотной эффективности при свинцовых отравлениях нового комплексообразующего вещества — D-пеницилламина (D-ПАМ), который представляет собою диметилцистеин, т. е. аминокислоту следующей химической структуры:
 Защитное действие D-ПАМ, по-видимому, в первую очередь обусловливается наличием трех близко расположенных функционально активных групп (сульфгидрильной, аминной, карбоксильной). Оказалось, что D-ПАМ особенно хорошо проявляет себя при маловыраженных, легких формах отравлений, когда необходим длительный прием препарата внутрь для элиминации металла из организма. Хорошая переносимость отечественного препарата D-ПАМ подтверждается многими авторами. D-ПАМ рекомендуется в течение нескольких педель принимать перорально также после того, когда отравленный будет выведен из тяжелого состояния с помощью инъекций солей ЭДТА. Сравнительный анализ показал значительно более выраженную элиминационную эффективности D-ПАМ в сопоставлении с СаNа2ЭДТА (рис. 12).
Защитное действие D-ПАМ, по-видимому, в первую очередь обусловливается наличием трех близко расположенных функционально активных групп (сульфгидрильной, аминной, карбоксильной). Оказалось, что D-ПАМ особенно хорошо проявляет себя при маловыраженных, легких формах отравлений, когда необходим длительный прием препарата внутрь для элиминации металла из организма. Хорошая переносимость отечественного препарата D-ПАМ подтверждается многими авторами. D-ПАМ рекомендуется в течение нескольких педель принимать перорально также после того, когда отравленный будет выведен из тяжелого состояния с помощью инъекций солей ЭДТА. Сравнительный анализ показал значительно более выраженную элиминационную эффективности D-ПАМ в сопоставлении с СаNа2ЭДТА (рис. 12).

Рис. 12. Выведение свинца из организма при приеме тетацинкальция в дозе 2 г в сутки (пунктирная линия) и D-пеницилламина в дозе 0,9 г в сутки (сплошная линии) (Архипоза и др., 1875)
Высокой степенью комплексообразования отличается также фитин — сложный органический препарат, представляющий собой смесь кальциевых и магниевых солей инозитфосфорных кислот. Его получают из обезжиренных конопляных жмыхов. По данным профессора Ж. И. Абрамовой,[132] фитин полностью защищает животных, отравленных смертельными дозами свинца. При этом он в отличие от солей ЭДТА выводит яд преимущественно через желудочно-кишечный тракт, а не через ночки. Фитин — совершенно безвредный лечебный препарат с дневной дозой около 1,5 г; он может быть рекомендован и при отравлении другими ядовитыми металлами, причем для полного выведения яда из организма допускается назначение такой дозы фитина в течение нескольких недель.Особенности механизма комплексообразования. Комплексоны и биоэлементы
Антидотное действие комплексонов зависит от прочности образующегося металлокомплекса, что в свою очередь определяется величиной константы устойчивости (или равновесия) соответствующих реакций хелатообразования. Исходя из этой величины, можно установить степень химического сродства отдельных металлов к комплексонам, а значит, и предвидеть возможность связывания ими различных металлов. Так, по возрастающей степени устойчивости комплекса «металл-ЭДТА» металлы располагаются в таком порядке: Sr, Mg, Ca, Fe2+, Mn, Co, Zn, Cd, Pb, Cu, Hg, Ni. Отсюда следует, что, например, кальциевые соли ЭДТА являются эффективными антидотами при отравлении свинцом и кадмием, так как эти металлы вытесняют из комплексона кальций, имеющий меньшую константу устойчивости с ЭДТА. По той же причине выведение из организма стронция и магния не будет ускоряться кальциевыми солями ЭДТА, а марганца и железа — кобальтовой ее солью. В то же время надо учитывать, что эффективность комплексонов в отношении токсичных металлов зависит не только от прочности образуемого комплекса «металл-хелат» и константы вытеснения металлом кальция, но и от прочности связи извлекаемого металла с биокомплексами организма.[133] Иногда длительное поступление в организм малых количеств ядовитых металлов приводит к фиксированию их различными внутренними органами и тканями, вследствие чего их концентрация в крови и моче существенно не повышена. И если имеется подозрение на интоксикацию, то пациенту дают один из комплексонов, что резко увеличивает выведение яда с мочой и указывает на его присутствие в организме. При этом по мере связывания антидотом свободно циркулирующего металла последний постепенно переходит из тканевых депо в плазму крови и затем через почки в мочу. Иными словами, процесс комплексообразования приводит к нарушению установившегося равновесия между ионизированным металлом плазмы и металлом, содержащимся, например, в эритроцитах, а также в печени, селезенке, костной ткани и др. Небезынтересно в связи с этим, что некоторые комплексоны, например тетацин, используются при обследовании яиц, ранее подвергавшихся на производстве воздействию свинца. После длительного перерыва в работе диагностическим показателем наличия у них свинцового депо в организме является выведение металла с мочой (0,35 мг в сутки и более) в результате однократной инъекции комплексона. Так как комплексоны связывают и ускоряют выведение из организма многих металлов, то по отношению к ним не остаются безучастными и биоэлементы, находящиеся в свободном состоянии (Na, К, Са и др.) или входящие в состав жизненно важных металлопротеидов. Вот почему введение в организм комплексонов не может не повлиять на течение обменных процессов и на действие ряда чужеродных веществ, поскольку их биотрансформация определяется функцией ферментов, молекулы которых включают тот или иной металл. Так, при обследовании 71 человека, соприкасавшегося во время работы со свинцом или ртутью и получавшего тетацин или унитиол с лечебной и диагностической целью, было установлено, что при длительном применении эти препараты резко увеличивают выведение из организма меди и марганца через почки. Эти данные привели к выводу о необходимости дополнительного введения названных жизненно важных микроэлементов с целью восполнения их потерь.[134] С другой стороны, эксперименты свидетельствуют, что некоторое аминополикарбоновые комплексоны (тетацин, пентацин) активируют такие металлопротеидные ферменты, как цитохромоксидаза, каталаза и др. Это связывается со способностью комплексонов изменять валентность атомов железа и других микроэлементов.[135] Между тем еще в 1956 г. было показано,[136] что животных можно защитить от смертельной дозы токсина газовой гангрены, вводя им растворы Na2ЭДТA и СаЭДТА. Оказалось, что этот микробный яд есть не что иное, как фермент лецитиназа,[137] который активируется ионами Zn2+ и Со2+. Поэтому, связывая эти ионы с помощью комплексонов, удается резко снизить действие токсина. Вообще надо отметить широкий диапазон возможного влияния хелатообразующих соединений на различные биохимические процессы и физиологические функции. В дальнейшем мы еще сможем проиллюстрировать это примерами из области токсикологии. Теперь же, в заключение данной главы, вкратце коснемся одного аспекта практического применения комплексонов. Поскольку соли ЭДТА и других аминополикарбоновых кислот не разлагаются в организме, характеризуются большой терапевтической широтой и быстро выводятся почками, отдельные токсикологи рекомендуют применять их и для предупреждения некоторых профессиональных отравлений (например, свинцовых, марганцевых, ртутных). В производственных условиях это возможно посредством вдыхания аэрозолей или приема внутрь таблеток, содержащих антидот. Однако с учетом вероятности развития побочных явлений (нарушение функции почек, связывание кальция сыворотки крови и многих микроэлементов, изменение активности некоторых ферментов и др.) ряд авторов отрицательно относится к профилактическому применению комплексонов. В связи с этим в нескольких лабораториях проводились изыскания таких профилактических средств, которые бы при длительном повседневном применении (в том числе и непосредственно на производстве) не вызывали нежелательных сдвигов в состоянии организма и в то же время обладали выраженным защитным действием. Эти свойства выявлены у пектинов — полимерных веществ пищевого происхождения, которые построены в виде цепей со звеньями следующего строения: Таким образом, каждое из этих звеньев включает 2 молекулы галактуроновых кислот, соединенных гидролизующимися связями. В литературе особенно подчеркивается антидотное значение их карбоксильных групп, которые способны присоединять катионы многих металлов с образованием пектинатов. Кроме того, следует иметь в виду, что пектины — коллоидные вещества с выраженными сорбционными свойствами.[138] Эти физические особенности, по-видимому, в немалой степени определяют их защитное действие при интоксикациях. Теперь уже накопилось достаточно экспериментальных данных, бесспорно свидетельствующих о профилактическом действии пектина при отравлениях тяжелыми металлами. Особенно четко такой эффект проявляется при проникновении в организм свинца, всасывание которого под влиянием пектинов резко тормозится. Для работающих в контакте с этим металлом О. Г. Архиповой и соавторами была разработана инструкция, согласно которой пектин вводится в организм в виде специально изготовленного мармелада с 5–8%-ным содержанием препарата (по 125 г ежедневно в течение 2–5,5 мес). При этом одновременно отмечалось увеличение выведения яда главным образом через желудочно-кишечный тракт. Каких-либо побочных явлений и осложнений длительный прием пектина не вызывал.[139]
Таким образом, в настоящее время можно говорить об определенных успехах экспериментальной и клинической токсикологии в изыскании и применении лекарственных средств антидотного действия, пригодных как для лечения, так и для предупреждения отравлений тиоловыми ядами. Практическое использование этих средств оказалось особенно результативным при профессиональных интоксикациях соединениями мышьяка, свинца, ртути.
Таким образом, каждое из этих звеньев включает 2 молекулы галактуроновых кислот, соединенных гидролизующимися связями. В литературе особенно подчеркивается антидотное значение их карбоксильных групп, которые способны присоединять катионы многих металлов с образованием пектинатов. Кроме того, следует иметь в виду, что пектины — коллоидные вещества с выраженными сорбционными свойствами.[138] Эти физические особенности, по-видимому, в немалой степени определяют их защитное действие при интоксикациях. Теперь уже накопилось достаточно экспериментальных данных, бесспорно свидетельствующих о профилактическом действии пектина при отравлениях тяжелыми металлами. Особенно четко такой эффект проявляется при проникновении в организм свинца, всасывание которого под влиянием пектинов резко тормозится. Для работающих в контакте с этим металлом О. Г. Архиповой и соавторами была разработана инструкция, согласно которой пектин вводится в организм в виде специально изготовленного мармелада с 5–8%-ным содержанием препарата (по 125 г ежедневно в течение 2–5,5 мес). При этом одновременно отмечалось увеличение выведения яда главным образом через желудочно-кишечный тракт. Каких-либо побочных явлений и осложнений длительный прием пектина не вызывал.[139]
Таким образом, в настоящее время можно говорить об определенных успехах экспериментальной и клинической токсикологии в изыскании и применении лекарственных средств антидотного действия, пригодных как для лечения, так и для предупреждения отравлений тиоловыми ядами. Практическое использование этих средств оказалось особенно результативным при профессиональных интоксикациях соединениями мышьяка, свинца, ртути.
ГЛАВА 5 Гемоглобин, яды и противоядия
Гемоглобин
Большое число веществ, используемых в промышленности, в медицинской практике и встречающихся в быту, обладает преимущественным действием на гемоглобин — кровяной пигмент, заключенный в эритроцитах и являющийся основным переносчиком кислорода от легких к тканям. Как известно, гемоглобин — сложный протеид, молекула которого построена из 2 частей: простого белка — глобина и простетической части — гема. Гем представляет собою производное протопорфирина и состоит из 4 пиррольных колец, соединенных между собою метановыми (=СН-) группами, с центрально расположенным атомом двухвалентного железа: Одна молекула гемоглобина включает 4 подобных гема и, следовательно, 4 атома железа. А так как кислород в гемоглобине непосредственно фиксируется железом, то такая молекула может, постепенно насыщаясь, присоединить 4 атома кислорода. Поэтому в кровеносном русле одновременно присутствуют восстановленный гемоглобин (Нb4) и в разной степени окисленный гемоглобин — оксигемоглобин: Hb4О2, Hb4(О2)2, Нb4(О2)3, Нb4(О2)4.[140]
Содержание гемоглобина в эритроцитах взрослого человека составляет около 750 г, из них 2,6 г приходятся на железо. На протяжении всей жизни в организме идут распад и синтез гемоглобина. Оба процесса связаны с продолжительностью нормального функционирования эритроцитов в кровеносных сосудах, равной 100–120 дням. Гемоглобин, выделяющийся из отслуживших свой срок эритроцитов, затем распадается. Нормальный процесс распада гемоглобина протекает главным образом в печени, при этом за сутки разрушается около 8 г гемоглобина и освобождается 25–26 мг железа, которое, как и другие продукты распада гемоглобина, выделяется из организма в основном через кишечник. Следовательно, для сохранения баланса гемоглобина суточное поступление железа в организм не должно быть меньше 25 мг.
Одна молекула гемоглобина включает 4 подобных гема и, следовательно, 4 атома железа. А так как кислород в гемоглобине непосредственно фиксируется железом, то такая молекула может, постепенно насыщаясь, присоединить 4 атома кислорода. Поэтому в кровеносном русле одновременно присутствуют восстановленный гемоглобин (Нb4) и в разной степени окисленный гемоглобин — оксигемоглобин: Hb4О2, Hb4(О2)2, Нb4(О2)3, Нb4(О2)4.[140]
Содержание гемоглобина в эритроцитах взрослого человека составляет около 750 г, из них 2,6 г приходятся на железо. На протяжении всей жизни в организме идут распад и синтез гемоглобина. Оба процесса связаны с продолжительностью нормального функционирования эритроцитов в кровеносных сосудах, равной 100–120 дням. Гемоглобин, выделяющийся из отслуживших свой срок эритроцитов, затем распадается. Нормальный процесс распада гемоглобина протекает главным образом в печени, при этом за сутки разрушается около 8 г гемоглобина и освобождается 25–26 мг железа, которое, как и другие продукты распада гемоглобина, выделяется из организма в основном через кишечник. Следовательно, для сохранения баланса гемоглобина суточное поступление железа в организм не должно быть меньше 25 мг.
Окись углерода
Из всех токсичных веществ наибольшим сродством к гемоглобину обладает окись углерода (СО), или угарный газ, — продукт неполного окисления углерода, образующийся там, где углеродсодержащие вещества сгорают в условиях недостаточного доступа воздуха. Развитие промышленности, транспорта, механизация сельского хозяйства и возрастающее в связи с этим потребление нефти, газа, угля приводят к тому, что с каждым годом все большее число людей на производстве и в быту подвергается воздействию продуктов горения. Хотя химический состав горючих веществ разнообразен, в число конечных продуктов горения в том или ином количестве всегда входит окись углерода. Окись углерода присутствует в светильном, генераторном, взрывных и выхлопных газах как постоянный компонент. Немало окиси углерода в табачном дыме и других дымах. Отравления окисью углерода возможны, например, в химической промышленности, где она является исходным продуктом синтеза ряда веществ (ацетона, метилового спирта и др.). Надо помнить и об опасном воздействии окиси углерода на человека при неправильной топке печей и при нарушениях правил пользования бытовыми газовыми приборами. Окись углерода обладает выраженными свойствами восстановителя, ее молекула включает 2 ненасыщенные валентности ( ) и потому может присоединять ряд химических элементов. В этой связи должны быть упомянуты токсичные карбонилы металлов, например соединения окиси углерода с никелем и железом, которые используются в химической промышленности. Поступая в организм, карбонилы выделяют окись углерода:
Ni(СО)4 → Ni + 4CO.
тeтракарбонил
никеля
Подобная реакция может протекать и при нагревании карбонилов, в особенности на активированном угле и других пористых материалах, а также при воздействии сильных окислителей, например хлора:
Fe(CO)5 + Cl2 → 5CO + FeCl2.
пентакарбонил
железа
Как это на первый взгляд ни парадоксально, одним из источников окиси углерода является сам человек, организм которого производит я выделяет во внешнюю среду (с выдыхаемым воздухом) за сутки около 10 мл СО. Это так называемая эндогенная, т. е. образующаяся во внутренних средах организма, окись углерода. Многими исследователями было показано, что она отщепляется от молекул гемоглобина при его превращении в желчный пигмент билирубин.[141] Поскольку билирубин образуется не только из гемоглобина, но и из других металлопротеидов (цитохромов, миоглобина, порфирина и др.), постольку последние также могут быть источником эндогенной СО. Таким образом, окись углерода является продуктом нормального метаболизма и ее выделение человеком в окружающую среду подобно удалению из организма углекислоты, аммиака и других образующихся в процессе обмена веществ химических соединений.
Хотя первые сведения о существовании эндогенной СО появились в литературе около 85 лет назад, только в последние десятилетия этому факту начали придавать существенное значение, что связано прежде всего с необходимостью обеспечения нормальной воздушной среды для специалистов, длительно находящихся в герметизированных помещениях (кабина самолета и космического корабля, кессон и т. п.). Именно в таких условиях человек вынужден вдыхать воздух, в котором накапливается эндогенная окись углерода, и это может стать причиной аутоинтоксикации. Чтобы предупредить такое опасное явление, необходимо использовать специальные приспособления для поглощения окиси углерода.
) и потому может присоединять ряд химических элементов. В этой связи должны быть упомянуты токсичные карбонилы металлов, например соединения окиси углерода с никелем и железом, которые используются в химической промышленности. Поступая в организм, карбонилы выделяют окись углерода:
Ni(СО)4 → Ni + 4CO.
тeтракарбонил
никеля
Подобная реакция может протекать и при нагревании карбонилов, в особенности на активированном угле и других пористых материалах, а также при воздействии сильных окислителей, например хлора:
Fe(CO)5 + Cl2 → 5CO + FeCl2.
пентакарбонил
железа
Как это на первый взгляд ни парадоксально, одним из источников окиси углерода является сам человек, организм которого производит я выделяет во внешнюю среду (с выдыхаемым воздухом) за сутки около 10 мл СО. Это так называемая эндогенная, т. е. образующаяся во внутренних средах организма, окись углерода. Многими исследователями было показано, что она отщепляется от молекул гемоглобина при его превращении в желчный пигмент билирубин.[141] Поскольку билирубин образуется не только из гемоглобина, но и из других металлопротеидов (цитохромов, миоглобина, порфирина и др.), постольку последние также могут быть источником эндогенной СО. Таким образом, окись углерода является продуктом нормального метаболизма и ее выделение человеком в окружающую среду подобно удалению из организма углекислоты, аммиака и других образующихся в процессе обмена веществ химических соединений.
Хотя первые сведения о существовании эндогенной СО появились в литературе около 85 лет назад, только в последние десятилетия этому факту начали придавать существенное значение, что связано прежде всего с необходимостью обеспечения нормальной воздушной среды для специалистов, длительно находящихся в герметизированных помещениях (кабина самолета и космического корабля, кессон и т. п.). Именно в таких условиях человек вынужден вдыхать воздух, в котором накапливается эндогенная окись углерода, и это может стать причиной аутоинтоксикации. Чтобы предупредить такое опасное явление, необходимо использовать специальные приспособления для поглощения окиси углерода.
Механизм токсического действия окиси углерода
Проникая с атмосферным воздухом в легкие, окись углерода быстро преодолевает альвеолярно-капиллярную мембрану, растворяется в плазме крови, диффундирует в эритроциты и вступает в обратимое химическое взаимодействие как с окисленным, так и восстановленным гемоглобином по схеме: Hb2 + CO HbCO + O2
или Hb + СО
HbCO + O2
или Hb + СО  HbСО.
Образующийся патологический комплекс карбоксигемоглобин (НbСО) не способен присоединять к себе кислород. При этом в молекуле гемоглобина СО соединяется с атомами железа (карбонил?), вытесняя кислород. Понятно, что одна молекула гемоглобина (точнее, 4 ее гема) может присоединить до 4 молекул СО.
Кровь весьма интенсивно поглощает окись углерода из-за высокого ее химического сродства к гемоглобину. Оказалось, что окись углерода примерно в 250 раз более активно связывается с гемоглобином, чем кислород. Иными словами, в конкуренции за гемоглобин окись углерода имеет выраженное преимущество перед кислородом. Расчет показывает, что при содержании в воздухе 0,07% СО и 21% О2 количество образующегося в крови НbO2 становится равным количеству НbСО. Такое равновесие может установиться, если во вдыхаемом человеком воздухе концентрация окиси углерода, близкая к 0,07% будет поддерживаться в течение многих часов (по некоторым данным, нескольких суток). Вот почему небольшие количества окиси углерода, в том числе эндогенной, могут оказаться опасными при длительном воздействии на организм в замкнутых пространствах. Надо еще иметь в виду, что диссоциация карбоксигемоглобина происходит очень медленно (в 3500 раз медленнее, чем диссоциация оксигемоглобина), и это также способствует его накоплению в крови.
Чем выше концентрация СО в воздухе, тем быстрее достигается опасное для жизни содержание карбоксигемоглобина в крови, составляющее 50% и более по отношению ко всему гемоглобину (рис. 13). Соотношение между количеством в крови НbСО и НbО2, с одной стороны, и концентрациями СО и О2 во вдыхаемом воздухе — с другой, принято оценивать с помощью константы Дугласа:
HbСО.
Образующийся патологический комплекс карбоксигемоглобин (НbСО) не способен присоединять к себе кислород. При этом в молекуле гемоглобина СО соединяется с атомами железа (карбонил?), вытесняя кислород. Понятно, что одна молекула гемоглобина (точнее, 4 ее гема) может присоединить до 4 молекул СО.
Кровь весьма интенсивно поглощает окись углерода из-за высокого ее химического сродства к гемоглобину. Оказалось, что окись углерода примерно в 250 раз более активно связывается с гемоглобином, чем кислород. Иными словами, в конкуренции за гемоглобин окись углерода имеет выраженное преимущество перед кислородом. Расчет показывает, что при содержании в воздухе 0,07% СО и 21% О2 количество образующегося в крови НbO2 становится равным количеству НbСО. Такое равновесие может установиться, если во вдыхаемом человеком воздухе концентрация окиси углерода, близкая к 0,07% будет поддерживаться в течение многих часов (по некоторым данным, нескольких суток). Вот почему небольшие количества окиси углерода, в том числе эндогенной, могут оказаться опасными при длительном воздействии на организм в замкнутых пространствах. Надо еще иметь в виду, что диссоциация карбоксигемоглобина происходит очень медленно (в 3500 раз медленнее, чем диссоциация оксигемоглобина), и это также способствует его накоплению в крови.
Чем выше концентрация СО в воздухе, тем быстрее достигается опасное для жизни содержание карбоксигемоглобина в крови, составляющее 50% и более по отношению ко всему гемоглобину (рис. 13). Соотношение между количеством в крови НbСО и НbО2, с одной стороны, и концентрациями СО и О2 во вдыхаемом воздухе — с другой, принято оценивать с помощью константы Дугласа:
 Эта величина, которая получила также название коэффициента отравления, показывает, что количество образующегося карбоксигемоглобина прямо пропорционально парциальному давлению окиси углерода и обратно пропорционально парциальному давлению кислорода. С другой стороны, чем больше во вдыхаемом воздухе (и следовательно, в кровеносном русле) кислорода, тем меньше образуется НbСО и тем быстрее он диссоциирует.
Эта величина, которая получила также название коэффициента отравления, показывает, что количество образующегося карбоксигемоглобина прямо пропорционально парциальному давлению окиси углерода и обратно пропорционально парциальному давлению кислорода. С другой стороны, чем больше во вдыхаемом воздухе (и следовательно, в кровеносном русле) кислорода, тем меньше образуется НbСО и тем быстрее он диссоциирует.

Рис. 13. График токсичности окиси углерода (Франке, 1973). По оси ординат — содержание HbCO в крови, об. %; по оси абсцисс — время, ч
По данным различных авторов, величина К для крови человека колеблется от 204 до 279, т. е. во столько раз скорость образования НbСО превосходит скорость образования НbO2.[142] Однако помимо парциального давления интенсивность поглощения кровью окиси углерода зависит также от длительности ее воздействия на организм и величины легочной вентиляции (минутного объема дыхания). В этой связи определенный интерес представляет формула, предложенная Лилиенталем (1946 г.): % НbСО = pCO·t·υ·0,05, где рСО — парциальное давление окиси углерода в мм рт. ст.; t — время воздействия в минутах; υ — минутный объем дыхания, т. е. произведение глубины вдоха в литрах на число вдохов за 1 мин. Итак, механизм действия окиси углерода определяется блокированием дыхательной функции гемоглобина и развитием вследствие этого гемического, или кровяного, типа кислородной недостаточности. Но степень интоксикации окисью углерода возрастает в связи с тем, что образовавшийся НbСО тормозит кислородную функцию нормального гемоглобина: в присутствии НbСО реакция диссоциации оксигемоглобина (НbO2 Hb+O2) замедляется и потому еще больше снижается поступление кислорода к клеткам. Вот почему НbСО, уменьшая поглощение кровью кислорода в легких, в то же время затрудняет разгрузку HbO2 в тканях. По-видимому, в этом следует искать объяснение случаев развития тяжелых интоксикаций при сравнительно небольшом количестве НbСО в крови (до 30%).
Поскольку химическое сродство к двухвалентному железу является основной причиной взаимодействия окиси углерода с гемоглобином, можно полагать, что и другие хромопротеиды, содержащие в своих молекулах ионы Fe2+, должны реагировать с этим ядом. Теперь уже не вызывает сомнений, что такого рода реакции могут в значительной степени влиять на течение интоксикаций. Имеется много экспериментальных данных, показывающих, что острые тяжелые отравления окисью углерода сопровождаются нарушением процессов потребления кислорода клетками. Воснове этих нарушений лежит прежде всего блокирование ядом железосодержащих ферментов — цитохромов и цитохромоксидазы.[143] Следовательно, при воздействии СО к гипоксии кровяного типа присоединяется тканевая гипоксия, в еще большей степени отягчающая течение интоксикации угарным газом. У отравленного отмечаются признаки нарастающего поражения центральной нервной системы: головная боль, головокружение, нарушение координации движений и рефлекторной сферы, а также ряд сдвигов психической деятельности, напоминающих алкогольное опьянение (эйфория, утрата самоконтроля, нецелесообразные поступки и т. п.). Характерно покраснение кожи пораженных. Когда количество НbСО в крови превышает 50–60%, развиваются судороги, утрачивается сознание и, если не принять экстренные меры, человек может погибнуть вследствие остановки дыхания и работы сердца.
Hb+O2) замедляется и потому еще больше снижается поступление кислорода к клеткам. Вот почему НbСО, уменьшая поглощение кровью кислорода в легких, в то же время затрудняет разгрузку HbO2 в тканях. По-видимому, в этом следует искать объяснение случаев развития тяжелых интоксикаций при сравнительно небольшом количестве НbСО в крови (до 30%).
Поскольку химическое сродство к двухвалентному железу является основной причиной взаимодействия окиси углерода с гемоглобином, можно полагать, что и другие хромопротеиды, содержащие в своих молекулах ионы Fe2+, должны реагировать с этим ядом. Теперь уже не вызывает сомнений, что такого рода реакции могут в значительной степени влиять на течение интоксикаций. Имеется много экспериментальных данных, показывающих, что острые тяжелые отравления окисью углерода сопровождаются нарушением процессов потребления кислорода клетками. Воснове этих нарушений лежит прежде всего блокирование ядом железосодержащих ферментов — цитохромов и цитохромоксидазы.[143] Следовательно, при воздействии СО к гипоксии кровяного типа присоединяется тканевая гипоксия, в еще большей степени отягчающая течение интоксикации угарным газом. У отравленного отмечаются признаки нарастающего поражения центральной нервной системы: головная боль, головокружение, нарушение координации движений и рефлекторной сферы, а также ряд сдвигов психической деятельности, напоминающих алкогольное опьянение (эйфория, утрата самоконтроля, нецелесообразные поступки и т. п.). Характерно покраснение кожи пораженных. Когда количество НbСО в крови превышает 50–60%, развиваются судороги, утрачивается сознание и, если не принять экстренные меры, человек может погибнуть вследствие остановки дыхания и работы сердца.
Кислород как антидот
Уже из приведенной реакции окиси углерода с окси-гемоглобином следует, что повышение в дыхательной среде парциального давления кислорода будет ускорять диссоциацию карбоксигемоглобина и выведение СО из организма. Иными словами, обратимость взаимодействия окиси углерода с гемоглобином позволяет предсказать направление его реактивирования. И хотя здесь эффективным конкурентным антагонистом токсичного агента является естественный и постоянно необходимый организму элемент внешней среды кислород, он с достаточным основанием может быть назван антидотом. Лечебное действие кислорода при отравлении даже смертельными концентрациями угарного газа поражает своей быстротой: находившийся на грани гибели человек при вдыхании кислорода или кислородно-воздушной смеси уже через несколько минут возвращается к жизни. Особенно эффективна кислородотерапия в сочетании со стимуляцией дыхания, ибо только при полноценном дыхательном акте можно добиться максимального поступления кислорода в организм. Это достигается как с помощью фармакологических средств (лобелии, цититон, коразол и др.) так и различных приемов искусственного дыхания. Известно, что углекислота является физиологическим возбудителем дыхательного центра — группы нервных клеток продолговатого мозга, управляющих актом дыхания. Вот почему усилить работу легких можно также посредством ингаляций карбогена, который представляет собою углекислотно-кислородную смесь, содержащую от 3 до 7% СО2. Ряд токсикологов подчеркивает, что при увеличении в крови парциального давления СО2 облегчается процесс диссоциации НbСО в эритроцитах и HbO2 в тканях. Последнее особенно важно, так как тем самым облегчается кислородная функция свободной от яда части кровяного пигмента.[144] Интересно отметить, — что предварительная ингаляция кислорода способствует созданию резистентности организма к окиси углерода. Это очень убедительно демонстрирует следующий опыт. Если одну мышь поместить в литровую колбу, заполненную кислородом, а вторую — в такую же колбу с атмосферным воздухом и в обе колбы ввести по 25 мл окиси углерода, то через несколько десятков секунд можно наблюдать молниеносно протекающую интоксикацию с судорогами и быструю гибель второй мыши, в то время как первая мышь не проявляет никаких признаков отравления в течение длительного времени. Хотя этот опыт впервые был продемонстрирован более полувека назад, до настоящего времени нет достаточно удовлетворительного объяснения его результатов. При дыхании в атмосфере чистого кислорода количество его, растворенное в плазме крови, значительно возрастает, и это, по-видимому, тормозит реакцию образования карбоксигемоглобина: кислород, подобно буферу, каким-то образом защищает гемоглобин от СО. Как бы то ни было, даже кратковременное вдыхание кислорода может способствовать предупреждению интоксикации угарным газом, например когда предстоит выполнение работы в отравленной атмосфере.Гипербарическая оксигенация при отравлениях окисью углерода
Но наиболее действенным и перспективным при отравлениях окисью углерода надо признать применение кислорода под избыточным давлением. Этот метод лечения с использованием специальных компрессионных камер, получивший название гипербарической оксигенации (ГБО), достаточно хорошо зарекомендовал себя на практике. Каковы же его физиологические обоснования? Артериальная кровь здорового человека при нормальном барометрическом давлении насыщена кислородом на 96–98%; при этом количество содержащегося в ней кислорода достигает 19,4 объемных процентов (об.%). Иными словами, каждые 100 мл крови транспортируют 19,4 мл кислорода, из которых 19,1 мл приходится на кислород, химически связанный с гемоглобином, и только 0,3 мл — на кислород, растворенный в плазме. Следовательно, в естественных условиях жизнедеятельности поддержание кислородного баланса обеспечивается в организме главным образом гемоглобином, а значение растворенного в плазме кислорода в обменных процессах ничтожно. Оказалось, что можно резко увеличить транспортную функцию плазмы крови, если повысить во вдыхаемом воздухе парциальное давление кислорода. Это видно из простого расчета по формуле: где К — количество растворенного в плазме кислорода в об. %; а — содержание в об.% растворенного в плазме кислорода при нормальном (760 мм рт. ст.) барометрическом давлении; рО2 — парциальное давление кислорода в альвеолярном воздухе в мм рт. ст. Так, при дыхании в атмосфере чистого кислорода количество его, растворенное в плазме крови, будет
где К — количество растворенного в плазме кислорода в об. %; а — содержание в об.% растворенного в плазме кислорода при нормальном (760 мм рт. ст.) барометрическом давлении; рО2 — парциальное давление кислорода в альвеолярном воздухе в мм рт. ст. Так, при дыхании в атмосфере чистого кислорода количество его, растворенное в плазме крови, будет  ≈ 2 об.%. Если же давление кислорода повысить до одной избыточной атмосферы, то величина К составит
≈ 2 об.%. Если же давление кислорода повысить до одной избыточной атмосферы, то величина К составит  ≈ 4,3 об.%. При давлении в 2 избыточные атмосферы К=6,5 об. %, т. е. количество растворенного в плазме кислорода возрастает более чем в 20 раз. Именно это позволяет обеспечить нормальный газообмен и тогда, когда блокирован гемоглобин. Более того, количество физически растворенного в плазме кислорода достигает такого уровня, что необходимость в гемоглобине как переносчике кислорода практически отпадает. Это, например, подтверждает поставленный в Голландии весьма демонстративный опыт, о котором было сообщено в 1964 г.[145] У поросят выпускали кровь и замещали ее плазмой или кровезаменителем (дакродексом). Затем животные помещались в барокамеру, в которой создавалось давление кислорода в 2 избыточные атмосферы. Животным обеспечивалось управляемое дыхание и поддержание работы сердца. Оказалось, что в таких условиях можно длительно поддерживать жизнедеятельность практически без гемоглобина, и это еще раз подтвердило факт усвоения тканями свободного кислорода независимо от способа его доставки к ним.
Еще в 1895 г. Холден показал, что мыши остаются живыми, несмотря на содержание во вдыхаемой смеси смертельной концентрации окиси углерода, если их подвергать воздействию кислорода под давлением 2 атм. В дальнейшем опытами на других животных, в том числе на обезьянах, многими исследователями была подтверждена эффективность ГБО при интоксикациях окисью углерода. В этой связи следует упомянуть поставленные на добровольцах эксперименты, о которых в 1949 г. сообщили американские исследователи Питтс и Пейс. Вначале люди находились в среде с угарным газом до тех пор, пока количество HbСО не достигало 20–30%, после чего их помещали в барокамеру с кислородом под давлением 2,5 атм. В результате была отмечена быстрая диссоциация карбоксигемоглобина.[146]
Вероятно, не случайно первое успешное применение ГБО при отравлении людей окисью углерода связано с практикой глубоководных погружений, при которых, как известно, используются барокамеры высокого давления. И осуществлено это было в нашей стране. В 1958 г. водолазный врач К. М. Рапопорт сообщил[147] о полном выздоровлении 24 лиц, отравленных окисью углерода (в том числе четверых в крайне тяжелом состоянии). Это достигалось воздействием кислорода под повышенным давлением в обычных водолазных рекомпрессионных камерах. Давление в них повышалось до 2–4 атм, а время пребывания под максимальным давлением колебалось в зависимости от состояния отравленных от 15 до 45 мин. Автором были получены разительные результаты при лечении лиц, находившихся в безнадежном положении. Эти четверо отравленных пришли в сознание на 19–35-й минуте пребывания под давлением кислорода в 3 атм. В дальнейшем давление в барокамере постепенно (в течение 105 мин) снижалось до атмосферного, и пораженные были выведены из нее в удовлетворительном состоянии. После кратковременного стационарного обследования они выписались из клиники вполне здоровыми. Наблюдение за ними в течение года показало отсутствие каких-либо последствий интоксикации.
Теперь уже число случаев успешного применения ГБО при отравлениях СО исчисляется десятками. Например, сообщается, что с помощью кислорода под давлением можно добиться полного излечения тяжело отравленного, если даже он находился в бессознательном состоянии до 3,5 ч.[148] Большинство авторов приходят к выводу, что ГБО целесообразно применять и тогда, когда содержание карбоксигемоглобина в крови сравнительно невелико. При этом подчеркивается, что увеличение количества физически растворенного кислорода в плазме крови не единственная причина эффективности ГБО. Следует иметь также в виду, что кислород под избыточным давлением ускоряет диссоциацию НbСО.
≈ 4,3 об.%. При давлении в 2 избыточные атмосферы К=6,5 об. %, т. е. количество растворенного в плазме кислорода возрастает более чем в 20 раз. Именно это позволяет обеспечить нормальный газообмен и тогда, когда блокирован гемоглобин. Более того, количество физически растворенного в плазме кислорода достигает такого уровня, что необходимость в гемоглобине как переносчике кислорода практически отпадает. Это, например, подтверждает поставленный в Голландии весьма демонстративный опыт, о котором было сообщено в 1964 г.[145] У поросят выпускали кровь и замещали ее плазмой или кровезаменителем (дакродексом). Затем животные помещались в барокамеру, в которой создавалось давление кислорода в 2 избыточные атмосферы. Животным обеспечивалось управляемое дыхание и поддержание работы сердца. Оказалось, что в таких условиях можно длительно поддерживать жизнедеятельность практически без гемоглобина, и это еще раз подтвердило факт усвоения тканями свободного кислорода независимо от способа его доставки к ним.
Еще в 1895 г. Холден показал, что мыши остаются живыми, несмотря на содержание во вдыхаемой смеси смертельной концентрации окиси углерода, если их подвергать воздействию кислорода под давлением 2 атм. В дальнейшем опытами на других животных, в том числе на обезьянах, многими исследователями была подтверждена эффективность ГБО при интоксикациях окисью углерода. В этой связи следует упомянуть поставленные на добровольцах эксперименты, о которых в 1949 г. сообщили американские исследователи Питтс и Пейс. Вначале люди находились в среде с угарным газом до тех пор, пока количество HbСО не достигало 20–30%, после чего их помещали в барокамеру с кислородом под давлением 2,5 атм. В результате была отмечена быстрая диссоциация карбоксигемоглобина.[146]
Вероятно, не случайно первое успешное применение ГБО при отравлении людей окисью углерода связано с практикой глубоководных погружений, при которых, как известно, используются барокамеры высокого давления. И осуществлено это было в нашей стране. В 1958 г. водолазный врач К. М. Рапопорт сообщил[147] о полном выздоровлении 24 лиц, отравленных окисью углерода (в том числе четверых в крайне тяжелом состоянии). Это достигалось воздействием кислорода под повышенным давлением в обычных водолазных рекомпрессионных камерах. Давление в них повышалось до 2–4 атм, а время пребывания под максимальным давлением колебалось в зависимости от состояния отравленных от 15 до 45 мин. Автором были получены разительные результаты при лечении лиц, находившихся в безнадежном положении. Эти четверо отравленных пришли в сознание на 19–35-й минуте пребывания под давлением кислорода в 3 атм. В дальнейшем давление в барокамере постепенно (в течение 105 мин) снижалось до атмосферного, и пораженные были выведены из нее в удовлетворительном состоянии. После кратковременного стационарного обследования они выписались из клиники вполне здоровыми. Наблюдение за ними в течение года показало отсутствие каких-либо последствий интоксикации.
Теперь уже число случаев успешного применения ГБО при отравлениях СО исчисляется десятками. Например, сообщается, что с помощью кислорода под давлением можно добиться полного излечения тяжело отравленного, если даже он находился в бессознательном состоянии до 3,5 ч.[148] Большинство авторов приходят к выводу, что ГБО целесообразно применять и тогда, когда содержание карбоксигемоглобина в крови сравнительно невелико. При этом подчеркивается, что увеличение количества физически растворенного кислорода в плазме крови не единственная причина эффективности ГБО. Следует иметь также в виду, что кислород под избыточным давлением ускоряет диссоциацию НbСО.
Другие средства специфического лечения отравлений окисью углерода
В настоящее время имеются лечебные препараты, к которым, может быть, формально в большей степени, чем к кислороду, подходит название «антидот» при их использовании в случае интоксикации СО. В числе таких средств назовем вещества, вступающие в прямое химическое взаимодействие с окисью углерода. Прежде всего это препараты двухвалентного железа и кобальта. Например, введение отравленному восстановленного железа резко ускоряет удаление СО из организма (в виде соединений FeCO). Тем самым при увеличении в организме внегемоглобинового железа создается своеобразный отвлекающий фактор, с помощью которого эритроциты предохраняются от действия СО. На этом основании А. М. Рашевская и Л. А. Зорина[149] — отечественные специалисты, много работающие в области токсикологии ядов, избирательно действующих на кровь, — считают, что при вынужденном длительном контакте с малыми концентрациями СО надо применять препараты двухвалентного железа с профилактической целью. В частности, они рекомендуют для этого принимать до 5 мл ферковена — смеси сахарата железа и глюконата кобальта в растворе углеводов (в 1 мл препарата содержится 20 мг железа и 0,09 мг кобальта). По имеющимся данным, Со2ЭДТА также оказывает положительное действие при отравлении СО, химически связывая яд. Следовательно, практическая токсикология располагает радом эффективных противоядий при интоксикации одним из самых распространенных ядов — окисью углерода. Однако поиски новых средств борьбы с отравлениями угарным газом продолжаются.Яды-метгемоглобинообразователи
Существует много веществ, которые выключают гемоглобин из процесса переноса кислорода посредством окисления входящего в состав его молекулы атома железа. Превращение Fe2+ в Fe3+ лишает гемоглобин способности обратимо связываться с кислородом. Такое изменение химической структуры гемоглобина лежит в основе перехода его в новую форму — метгемоглобин (MtHb). Доказано, что в нормальных условиях жизнедеятельности кровь человека и животных содержит от 1 до 2% MtHb. В отличие от НbО2, в котором к атомам Fe2+ лабильно присоединен кислород, MtHb, (точнее, атомы Fe3+ его молекулы), как полагают большинство исследователей, прочно связывает отрицательно заряженные гидроксильные группы. Естественно, что яды-метгемоглобинообразователи тормозят кислородную функцию гемоглобина и, подобно окиси углерода, вызывают гемическую (кровяную) гипоксию. В настоящее время известно большое число химических соединений, вызывающих токсические метгемоглобинемии. Так, профессор М. С. Кушаковский[150] рассматривает следующие 5 групп веществ-метгемоглобинообразователей: 1) нитросоединения, в том числе органические (окислы азота, нитриты и нитраты, тринитротолуол); 2) аминосоединения (анилин, гидроксиламин, фенилгидразин, аминофенолы и их многочисленные производные, среди которых компоненты красителей, ваксы для обуви); 3) окислители (хлораты, перманганаты, хиноны, нафталин); 4) окислительно-восстановительные краски (метиленовый синий, крезиловый голубой); 5) лекарственные препараты (нитроглицерин, амилнитрит, новокаин, сульфаниламиды, аспирин, барбитураты и др.). Этот перечень показывает, сколь велика в производственных и бытовых условиях вероятность блокирования кислородпередающей функции крови вследствие образования метгемоглобина. Например, исследования Ф. Н. Субботина[151] показали, что соли азотной кислоты, содержащиеся в питьевой воде, могут вызвать у людей синдром метгемоглобинемии. Серьезную опасность они представляют для детей, как наиболее ранимых. Выяснилось, что такого рода заболевание связано чаще всего с потреблением колодезной воды, богатой нитратами. Источником последних являются аммиачно-селитровые удобрения, попадающие в грунтовые воды и воды открытых водоемов. Поступая в организм, нитраты под влиянием микрофлоры кишечника переходят в нитриты (соли азотистой кислоты), которые всасываются в кровь и превращают большее или меньшее количество гемоглобина в метгемоглобин.[152] Кроме того, известно, что нитраты и нитриты довольно широко используются при обработке мяса в консервном и колбасном производстве. Это также может наносить вред здоровью, прежде всего лицам с сердечнососудистой патологией, заболеваниями органов дыхания и страдающим малокровием, т. е. живущим и без того на пределе кислородного обеспечения. Вот почему вопрос о необходимости исключения солей азотной и азотистой кислот из состава пищевых продуктов приобретает все большую актуальность.[153] Ряд летучих веществ пищевого происхождения, образующихся, например, при кулинарной обработке лука, чеснока, хрена и редьки, также является метгемоглобинообразователями. Так, обследование работников столовых выявило у 33% из них повышение уровня метгемоглобина до 6,5%.[154] При остро протекающих тяжелых метгемоглобиновых отравлениях возникает резкая головная боль, головокружение, тошнота, рвота, оглушенность, затемнение или даже потеря сознания. Отмечается серо-синяя окраска слизистых оболочек и кожи, увеличиваются размеры печени. Кровь отравленных приобретает шоколадно-бурый цвет, в ней определяется метгемоглобин, количество которого прямо пропорционально тяжести интоксикации. При такой степени отравления оно достигает 60–70% по отношению ко всей массе гемоглобина. При этом из-за дефицита насыщения крови кислородом показатель ее аргериовенозной разницы по кислороду уменьшается. В то же время надо учитывать впервые установленный в нашей стране факт снижения скорости диссоциации НbО2 в кровеносных капиллярах при наличии в крови большого количества MtHb (подобно тому, что наблюдается в присутствии НbСО).[155] Это снижение может быть при тяжелых отравлениях значительным (почти в 2 раза) и существенно отягчать состояние отравленных. Каковы же современные взгляды на возможности специфического воздействия на интоксикации метгемоглобинообразователями? Теоретически можно предположить, что если образование метгемоглобина является в основном результатом воздействия на кровь окислителей, то их химические антагонисты-восстановители — должны реактивировать видоизмененный ядом кровяной пигмент. И действительно, реальное значение в качестве противоядий здесь приобрели вещества с противоокислительными свойствами, получившие общее название антиоксидантов.Восстановители гемоглобина
Глюкоза. Одним из наиболее изученных средств такого рода считается глюкоза. Рядом отечественных и зарубежных исследователей показано ее благотворное влияние на процесс восстановления гемоглобина (деметгемоглобинизацию). Так, в опытах на собаках установлено, что при одновременном введении в организм глюкозы и большой дозы анилина в крови почти не определяется MtHb, в то время как у контрольных животных наблюдалась выраженная метгемоглобинемия. Весьма интересными были опыты с птицами, у которых в норме определяется очень высокий уровень сахара в крови. Оказалось, что у них кровяной пигмент почти не окисляется при воздействии таких сильных метгемоглобинообразователей, как амидо- и нитросоединения бензола. Однако если концентрацию сахара в крови у птиц снизить введением инсулина, то при тех же условиях опыта наблюдается ускорение образования метгемоглобина.[156] Механизм восстановления метгемоглобина глюкозой объясняют по-разному. Со времени классических работ Варбурга, А. И. Баха и других ученых, установивших биохимические закономерности окислительно-восстановительных процессов, известно, что глюкоза, окисляясь в организме, становится сильным восстановителем, в том числе и по отношению к гемоглобину. Такому действию глюкозы способствуют, в частности, ферментативные реакции дегидрирования при ее распаде в организме. Следовательно, и само восстановление метгемоглобина в гемоглобин в конечном счете — ферментативный процесс. С другой стороны, антидотное действие глюкозы усиливается защитными свойствами ее метаболита — глюкуроновой кислоты. Увеличение последней в организме усиливает нейтрализацию метгемоглобинообразующих ядов и токсичных продуктов их превращений (например, путем образования парных фенолглюкуроновых кислот). Хотя деметгемоглобинизирующее действие глюкозы само по себе не оспаривается, ряд исследователей обращают внимание на то, что для восстановления метгемоглобина со скоростью, на которую способны соответствующие ферменты эритроцитов, достаточно глюкозы, постоянно растворенной в крови. Поэтому, согласно данной точке зрения, повышение концентрации глюкозы в крови не может существенно изменить течение естественного процесса деметгемоглобинизации. Тем не менее в практическом плане следует учитывать, что в современных токсикологических руководствах глюкоза продолжает официально значиться в числе средств, — активно восстанавливающих метгемоглобин. Метиленовый синий. Вторым веществом, которое принято рассматривать как антидот при токсических метгемоглобинемиях, является метиленовый синий: Оказалось, что это соединение обладает высоким окислительно-восстановительным потенциалом. Присоединяя 2 атома водорода, метиленовый синий восстанавливается, а восстановленная его форма в присутствии кислорода окисляется метгемоглобином. При этом последний в свою очередь восстанавливается в гемоглобин. Тем самым в крови создается равновесие между восстановленной и окисленной формами метиленового синего, с одной стороны, и гемоглобином и метгемоглобином — с другой. Равновесие это возникает при появлении в крови уже небольших количеств метгемоглобина. Вот почему на фоне метгемоглобиновой интоксикации (как показывает клинический опыт) малые дозы метиленового синего (50 мг) будут способствовать восстановлению метгемоглобина, в то время как в больших дозах (250–300 мг) это вещество, наоборот, становится метгемоглобинообразователем (рис. 14).
Оказалось, что это соединение обладает высоким окислительно-восстановительным потенциалом. Присоединяя 2 атома водорода, метиленовый синий восстанавливается, а восстановленная его форма в присутствии кислорода окисляется метгемоглобином. При этом последний в свою очередь восстанавливается в гемоглобин. Тем самым в крови создается равновесие между восстановленной и окисленной формами метиленового синего, с одной стороны, и гемоглобином и метгемоглобином — с другой. Равновесие это возникает при появлении в крови уже небольших количеств метгемоглобина. Вот почему на фоне метгемоглобиновой интоксикации (как показывает клинический опыт) малые дозы метиленового синего (50 мг) будут способствовать восстановлению метгемоглобина, в то время как в больших дозах (250–300 мг) это вещество, наоборот, становится метгемоглобинообразователем (рис. 14).

Рис. 14. Схема разнонаправленного действия метиленового синего на гемоглобин
Механизм восстанавливающего действия метиленового синего на MtHb многие исследователи связывают также с обменом в организме сахаров, в частности с усилением окисления их метаболита — молочной кислоты — и превращением ее в пировиноградную кислоту. Эта реакция сопровождается гидрированием метиленового синего, который в свою очередь окисляется метгемоглобином. Надо, однако, — отметить, что у метиленового синего как антидота есть и отрицательные свойства. Самое опасное из них (и, к счастью, редко наблюдаемое) — внутрисосудистый гемолиз, т. е. разрушающее действие на эритроциты, — что приводит к выходу из них гемоглобина и растворению его в плазме крови. Возможны также у отдельных людей и нарушения со стороны центральной нервной системы, сердца, легких. Все это, конечно, снижает значение метиленового синего как лечебного препарата и не позволяет применять его в течение длительного времени. Сульфгидрильные соединения. Поскольку ни глюкоза, ни метиленовый синий не могут считаться достаточно приемлемыми восстановителями гемоглобина, вполне оправданными стали поиски антидотов такого типа действия среди других противоокислительных веществ. И здесь определенный успех был достигнут при изучении ряда органических соединений, содержащих SH-группы. Так, в лаборатории профессора М. С. Кушаковского было показано, что β-меркаптоэтиламин, или цистеамин (HS-CH2-СH2-NH2·HCl), и ряд других меркаптосоединений (например, вещество строения HS-СН2-СН2-ОН) обладают способностью активно вмешиваться в ферментативные реакции восстановления метгемоглобина. Это же можно сказать и о многих аминодисульфидах, а также о метилированных производных цистеамина (N-диметил-цистеамин) и цистамина (N-N'-тетрадиметилцистамин). Важным свойством некоторых из названных веществ является их способность предупреждать образование метгемоглобина. Практически наиболее ценным сульфгидрильным антидотом оказался гидрохлорид цистамина [157], который к тому же заметно препятствует гемолизу.
Так как при метгемоглобиновых интоксикациях, как и при отравлении окисью углерода, блокируется кислородная функция крови, то логично предположить, что увеличение содержания кислорода в плазме даже при высокой концентрации метгемоглобина дает основание надеяться на благоприятный исход отравления. Очень убедительно в экспериментах на морских свинках это показали Б. Р. Гланц и В. Д. Тонкопий.[158] Помещая животных, отравленных смертельными дозами нитрита натрия, в барокамеру с чистым кислородом под давлением 2 избыточные атмосферы на 2 ч, исследователи добивались 100%-ного их выживания. При этом они обнаружили, что, хотя кислород под давлением не оказывает прямого влияния на процесс нормализации гемоглобина, время кислородной компрессии достаточно для сохранения жизнедеятельности организма до момента начала спонтанного восстановления метгемоглобина. Эти и другие подобные эксперименты свидетельствуют о важности экстренного введения в организм больших количеств кислорода при отравлении метгемоглобинообразующими ядами.
[157], который к тому же заметно препятствует гемолизу.
Так как при метгемоглобиновых интоксикациях, как и при отравлении окисью углерода, блокируется кислородная функция крови, то логично предположить, что увеличение содержания кислорода в плазме даже при высокой концентрации метгемоглобина дает основание надеяться на благоприятный исход отравления. Очень убедительно в экспериментах на морских свинках это показали Б. Р. Гланц и В. Д. Тонкопий.[158] Помещая животных, отравленных смертельными дозами нитрита натрия, в барокамеру с чистым кислородом под давлением 2 избыточные атмосферы на 2 ч, исследователи добивались 100%-ного их выживания. При этом они обнаружили, что, хотя кислород под давлением не оказывает прямого влияния на процесс нормализации гемоглобина, время кислородной компрессии достаточно для сохранения жизнедеятельности организма до момента начала спонтанного восстановления метгемоглобина. Эти и другие подобные эксперименты свидетельствуют о важности экстренного введения в организм больших количеств кислорода при отравлении метгемоглобинообразующими ядами.
Гемолитические яды и мекаптид (антарсин)
Остановимся еще на одной группе веществ, блокирующих кислородпередающую функцию крови. Это гемолитические яды, действие которых, как уже отмечалось, приводит к выходу гемоглобина из эритроцитов в плазму крови. В настоящее время процесс гемолиза рассматривается, с одной стороны, как следствие разрушения ядами оболочки эритроцитов, в частности посредством ингибирования сульфгидрильных групп белков эритроцитарных мембран, а с другой — изменений в сложной цепочке ферментных процессов, лежащих в основе поддержания целостности структуры красных кровяных телец.[159] Внеэритроцитарный гемоглобин теряет способность связываться с кислородом; при этом он частично превращается в желчные пигменты и другие, близкие к ним по строению, продукты, а частично выводится из организма через почки. Чем интенсивнее гемолиз, тем меньше гемоглобина задерживается в организме и тем больше его переходит в мочу. Это последнее явление, именуемое гемоглобинурией, — один из характерных и грозных признаков внутрисосудистого гемолиза. Существует немало веществ, вызывающих гемолиз. Это и некоторые гидразинопроизводные, например фенил-гидразин ( ), и бертолетова соль(КСlO3), и отдельные медикаментозные средства (сульфаниламиды, хинин, фенацетин и др.). Однако наиболее типичным гемолитическим ядом считается мышьяковистый водород (AsH3), который образуется в производственных условиях как побочный продукт воздействия технических кислот на различные материалы, содержащие мышьяк. Будучи бесцветным тяжелым газом AsH3 проникает в организм главным образом через легкие, при этом значительная часть яда подвергается окислению и переходит в элементарный мышьяк и его окислы, которые можно обнаружить в крови и внутренних органах. Как сильный восстановитель AsH3 взаимодействует с кислородсодержащими макромолекулами организма, прежде всего с оксигемоглобином. После скрытого периода продолжительностью 3–5 ч в крови отравленного уменьшается количество эритроцитов, возникают такие опасные симптомы, как торможение мочеотделения из-за поражения почек, расстройство функции печени, падение кровяного давления.
Многие годы поиски антидота при отравлении AsH3 были безуспешны. Около 15 лет назад совместный труд киевских токсикологов и химиков увенчался созданием отечественного препарата антарсина (2,3-димеркаптопропил-п-толилсульфида)[160] — эффективного антидота мышьяковистого водорода:
), и бертолетова соль(КСlO3), и отдельные медикаментозные средства (сульфаниламиды, хинин, фенацетин и др.). Однако наиболее типичным гемолитическим ядом считается мышьяковистый водород (AsH3), который образуется в производственных условиях как побочный продукт воздействия технических кислот на различные материалы, содержащие мышьяк. Будучи бесцветным тяжелым газом AsH3 проникает в организм главным образом через легкие, при этом значительная часть яда подвергается окислению и переходит в элементарный мышьяк и его окислы, которые можно обнаружить в крови и внутренних органах. Как сильный восстановитель AsH3 взаимодействует с кислородсодержащими макромолекулами организма, прежде всего с оксигемоглобином. После скрытого периода продолжительностью 3–5 ч в крови отравленного уменьшается количество эритроцитов, возникают такие опасные симптомы, как торможение мочеотделения из-за поражения почек, расстройство функции печени, падение кровяного давления.
Многие годы поиски антидота при отравлении AsH3 были безуспешны. Около 15 лет назад совместный труд киевских токсикологов и химиков увенчался созданием отечественного препарата антарсина (2,3-димеркаптопропил-п-толилсульфида)[160] — эффективного антидота мышьяковистого водорода:
 В последующем он получил новое название — мекаптид.[161] В основе молекулярного механизма действия мекаптида лежит сложный, до конца еще не изученный биохимический процесс. Уже при первом взгляде на химическую структуру мекаптида (сульфгидрильное соединение) возникает вопрос, каким образом проявится его антидотный эффект, если он не будет вступать в прямую реакцию с восcтановителем, каким является AsH3. Здесь предполагается 2 возможности. Во-первых, это прямая реакция мекаптида с мышьяком или его окислами, образовавшимися из AsH3 в организме. В результате такой реакции возникает нетоксичный комплекс «мекаптид-арсин» по той же схеме, по какой взаимодействуют другие дитиолы с мышьяком. Во-вторых, допускается, что в результате окислительных превращений молекула антидота может видоизменять свое строение с образованием соединений, содержащих дисульфидные группы. Последние, как подчеркивают И. Г. Мизюкова и В. Е. Петрунькин,[162] выступают в роли окислителей мышьяковистого водорода. В результате образуются продукты его окисления с последующим превращением их в малотоксичные вещества — циклические тиоарсениты, быстро выводящиеся из организма через почки. Названные авторы отмечают интересный факт: применение унитиола не только не тормозит развития интоксикации мышьяковистым водородом, но и может (особенно в начальном периоде отравления) усиливать его действие. Это связывается с тем, что как восстановитель унитиол препятствует окислению AsH3 и, кроме того, он не может проникнуть в эритроциты. В то же время унитиол рекомендуется применять в более поздние сроки отравления мышьяковистым водородом (на 5–7-е сутки). Тогда окисление яда естественным путем или под влиянием мекаптида в основном заканчивается, и унитиол ускоряет выведение мышьяка из организма посредством описанных ранее химических реакций.
В последующем он получил новое название — мекаптид.[161] В основе молекулярного механизма действия мекаптида лежит сложный, до конца еще не изученный биохимический процесс. Уже при первом взгляде на химическую структуру мекаптида (сульфгидрильное соединение) возникает вопрос, каким образом проявится его антидотный эффект, если он не будет вступать в прямую реакцию с восcтановителем, каким является AsH3. Здесь предполагается 2 возможности. Во-первых, это прямая реакция мекаптида с мышьяком или его окислами, образовавшимися из AsH3 в организме. В результате такой реакции возникает нетоксичный комплекс «мекаптид-арсин» по той же схеме, по какой взаимодействуют другие дитиолы с мышьяком. Во-вторых, допускается, что в результате окислительных превращений молекула антидота может видоизменять свое строение с образованием соединений, содержащих дисульфидные группы. Последние, как подчеркивают И. Г. Мизюкова и В. Е. Петрунькин,[162] выступают в роли окислителей мышьяковистого водорода. В результате образуются продукты его окисления с последующим превращением их в малотоксичные вещества — циклические тиоарсениты, быстро выводящиеся из организма через почки. Названные авторы отмечают интересный факт: применение унитиола не только не тормозит развития интоксикации мышьяковистым водородом, но и может (особенно в начальном периоде отравления) усиливать его действие. Это связывается с тем, что как восстановитель унитиол препятствует окислению AsH3 и, кроме того, он не может проникнуть в эритроциты. В то же время унитиол рекомендуется применять в более поздние сроки отравления мышьяковистым водородом (на 5–7-е сутки). Тогда окисление яда естественным путем или под влиянием мекаптида в основном заканчивается, и унитиол ускоряет выведение мышьяка из организма посредством описанных ранее химических реакций.
Глава 6 ЦИАНИДЫ И АНТИЦИАНИДЫ
Синильная кислота и другие цианиды
До настоящего времени важнейшим представителем цианидов считается синильная кислота (HCN). Эта легкая летучая жидкость с характерным запахом горького миндаля является весьма сильным ядом: в количестве 0,05 г она уже вызывает у человека смертельное отравление. Полученная впервые в чистом виде в 80-х годах XVIII столетия шведским фармацевтом и химиком Карлом Шееле синильная кислота[163] и теперь привлекает к себе пристальное внимание многих специалистов. Цианистые соединения использовались уже в древние времена, хотя, конечно, их химическая природа тогда не была известна. Так, древнеегипетские жрецы умели изготавливать из листьев персика эссенцию, которой они умерщвляли провинившихся людей. В Париже, в Лувре, на рулоне папируса имеется предостерегающее изречение: «Не произносите имени Иао под страхом наказания персиком», а в храме Изиды найдена надпись: «Не открывай — иначе умрешь от персика». Сейчас мы знаем, что действующей составной частью здесь являлась синильная кислота, образующаяся в процессе ферментативных превращений некоторых веществ растительного происхождения. Ряд выдающихся химиков прошлого изучали строение, способы производства и использования цианидов. Так, в 1811 г. Гей-Люссак впервые показал, что синильная кислота представляет собою водородное соединение радикала, состоящего из углерода и азота, а Бунзен в середине XIX в. разработал метод промышленного получения цианида калия. Прошло уже много лет с тех пор, когда цианид калия и другие цианиды имели значение как средства предумышленных отравлений и когда к этим быстродействующим ядам особый интерес проявляли судебно-медицинские эксперты. Истории известны случаи применения цианидов для массового поражения людей. Например, французская армия использовала во время первой мировой войны синильную кислоту в качестве отравляющего вещества, в гитлеровских лагерях уничтожения фашисты применяли ядовитые газы циклоны (эфиры цианмуравьиной кислоты), американские войска в Южном Вьетнаме использовали против мирного населения токсичные органические цианиды (газы типа CS). Известно также, что в США длительное время применяется смертная казнь посредством отравления осужденных парами синильной кислоты в специальной камере. Благодаря высокой химической активности и способности взаимодействовать с многочисленными соединениями различных классов цианиды широко применяются во многих отраслях промышленности, сельского хозяйства, в научных исследованиях, и это создает немало возможностей для интоксикаций. Так, синильная кислота и большое число ее производных используются при извлечении благородных металлов из руд, при гальванопластическом золочении и серебрении, в призводстве ароматических веществ, химических волокон, пластических масс, каучука, органического стекла, стимуляторов роста растений, гербицидов. Цианиды применяются также в качестве инсектицидов, удобрений и дефолиантов. Синильная кислота выделяется в газообразном состоянии при многих производственных процессах, а также образуется при контакте цианидов с другими кислотами и влагой. Могут быть и отравления цианидами вследствие употребления в пищу большого количества семян миндаля, персика, абрикоса, вишни, сливы и других растений семейства розоцветных или настоек из их плодов. Оказалось, что все они содержат гликозид амигдалин, который в организме под влиянием фермента эмульсина разлагается с образованием синильной кислоты, бензальдегида и 2 молекул глюкозы: Наибольшее количество амигдалина содержится в горьком миндале, в очищенных зернах которого его около 3%. Несколько меньше амигдалина (до 2%) в сочетании с эмульсином содержится в семенах абрикоса. Клинические наблюдения показали,[164] что гибель отравленных наступала обычно после употребления в пищу около 100 очищенных семян абрикоса, что соответствует примерно 1 г амигдалина. Подобно амигдалину отщепляют синильную кислоту такие растительные гликозиды, как линамарин, находящийся в льне, и лауроцеразин, содержащийся в листьях лавровишневого дерева. Весьма много цианистых веществ в молодых бамбуках и их побегах (до 0,15% сырой массы). В животном мире синильная кислота встречается в секрете кожных желез тысяченожек (Fontaria gracilis).
Токсичность цианидов для различных видов животных различна. Так, высокая резистентность к синильной кислоте отмечена у холоднокровных, в то время как многий теплокровные животные весьма к ней чувствительны. Что касается человека, то, по-видимому, он более устойчив к действию синильной кислоты, чем некоторые высшие животные. Это подтверждает, например, опыт, поставленный с большим риском для себя известным английским физиологом Баркрофтом, который в специальной камере вместе с собакой подвергался воздействию синильной кислоты в концентрации 1:6000. Опыт продолжался до тех пор, пока собака не впала в коматозное состояние и у нее не появились судороги. Экспериментатор в это время у себя не отмечал каких-либо признаков отравления. Лишь спустя 10–15 мин после извлечения из камеры погибающей собаки у него отмечалось нарушение внимания и тошнота.
Имеется немало данных, свидетельствующих об образовании цианидов в организме человека в физиологических условиях. Цианиды эндогенного происхождения обнаружены в биологических жидкостях, в выдыхаемом воздухе, в моче. Считается, что нормальный их уровень в плазме крови может достигать 140 мкг/л. В связи с этим должен быть упомянут и витамин В12 (цианокобаламин), который, как известно, является фактором роста, — необходимым организму для нормального кроветворения и функционирования нервной системы, печени и других органов. По химической структуре витамин В12 — сложное полициклическое соединение с атомом кобальта в центре молекулы к которому присоединена CN-группа.
Наибольшее количество амигдалина содержится в горьком миндале, в очищенных зернах которого его около 3%. Несколько меньше амигдалина (до 2%) в сочетании с эмульсином содержится в семенах абрикоса. Клинические наблюдения показали,[164] что гибель отравленных наступала обычно после употребления в пищу около 100 очищенных семян абрикоса, что соответствует примерно 1 г амигдалина. Подобно амигдалину отщепляют синильную кислоту такие растительные гликозиды, как линамарин, находящийся в льне, и лауроцеразин, содержащийся в листьях лавровишневого дерева. Весьма много цианистых веществ в молодых бамбуках и их побегах (до 0,15% сырой массы). В животном мире синильная кислота встречается в секрете кожных желез тысяченожек (Fontaria gracilis).
Токсичность цианидов для различных видов животных различна. Так, высокая резистентность к синильной кислоте отмечена у холоднокровных, в то время как многий теплокровные животные весьма к ней чувствительны. Что касается человека, то, по-видимому, он более устойчив к действию синильной кислоты, чем некоторые высшие животные. Это подтверждает, например, опыт, поставленный с большим риском для себя известным английским физиологом Баркрофтом, который в специальной камере вместе с собакой подвергался воздействию синильной кислоты в концентрации 1:6000. Опыт продолжался до тех пор, пока собака не впала в коматозное состояние и у нее не появились судороги. Экспериментатор в это время у себя не отмечал каких-либо признаков отравления. Лишь спустя 10–15 мин после извлечения из камеры погибающей собаки у него отмечалось нарушение внимания и тошнота.
Имеется немало данных, свидетельствующих об образовании цианидов в организме человека в физиологических условиях. Цианиды эндогенного происхождения обнаружены в биологических жидкостях, в выдыхаемом воздухе, в моче. Считается, что нормальный их уровень в плазме крови может достигать 140 мкг/л. В связи с этим должен быть упомянут и витамин В12 (цианокобаламин), который, как известно, является фактором роста, — необходимым организму для нормального кроветворения и функционирования нервной системы, печени и других органов. По химической структуре витамин В12 — сложное полициклическое соединение с атомом кобальта в центре молекулы к которому присоединена CN-группа.
Механизм биологического действия цианидов
Цианиды могут проникать во внутренние среды организма с отравленной пищей и водой, а также через поврежденную кожу. Очень опасно ингаляционное воздействие летучих цианидов, прежде всего синильной кислоты и хлорциана. Еще в 60-х годах XIX столетия обратили внимание на то, что венозная кровь, оттекающая от тканей и органов отравленных цианидами животных, приобретает алый, артериальный цвет. В дальнейшем было показано, что в ней содержится примерно столько же кислорода, сколько и в артериальной крови. Следовательно, под воздействием цианидов организм теряет способность усваивать кислород. Почему же это происходит?
Рис. 15. Схема процесса клеточного окисления. НАД (никотинамидадениндинуклеотид) и НАДФ (никотинамидадениндинуклео-тидфосфат) — коферменты дегидрогеназ; ФМН (флавинмононуклеотид) и ФАД (флавинадениндинуклеотид) — коферменты флавиновых ферментов; цВ, цС, цС1 цА — цитохромы; цА3 — цитохромоксидаза
Ответ на этот вопрос был получен в Германии в конце 20-х годов в работах Отто Варбурга, который установил,[165] что, проникая в кровеносное русло, цианиды очень скоро оказываются в клеточных структурах, прежде всего в митохондриях, где протекают ферментативные процессы тканевого окисления (потребления клетками кислорода). Как видно из рис. 15, первое звено этих процессов включает отщепление водорода от окисляющегося субстрата, При этом каждый атом водорода разделяется на протон и электрон. Данная часть окислительных реакций в клетках катализируется ферментами из группы дегидраз, а также так называемым флавиновым (желтым) ферментом Варбурга. Второе звено клеточного окисления состоит в переносе электронов на кислород, что делает возможным его взаимодействие с атомами активированного водорода (протонами) и приводит к образованию одного из важнейших конечных продуктов окисления — молекулы воды. Это звено окислительных реакций функционирует благодаря особой группе ферментов — цитохромам и цитохромоксидазе, содержащих атомы железа переменной валентности. Именно такое их химическое свойство является источником электронов, присоединяющихся к кислороду. Как следует из приведенной схемы, электроны последовательно переходят от одного цитохрома к другому, от них к цитохромоксидазе, а затем на кислород. По образному выражению, «цепочка цитохромов подобна цепочке баскетболистов, передающих мяч (электрон) от одного игрока к другому, неумолимо приближая его к корзине (кислороду)».[166] Этот конечный этап клеточного окисления схематично можно представить в виде следующих двух реакций: 1) 2белок — R -Fe2+ + 1/2O2 2белок — R — Fe3+ + 1/2O22-,
восстановленная окисленная
цитохромоксидаза цитохромоксидаза
2) 1/2O22- + 2H+ → H2O.
Оказалось, что синильная кислота, точнее CN-ион, вследствие особого химического сродства к трехвалентному железу избирательно (хотя и обратимо) взаимодействует с окисленными молекулами цитохромоксидазы. Тем самым тормозится течение нормального процесса тканевого дыхания.[167] Таким образом, блокируя один из железосодержащих дыхательных ферментов, цианиды вызывают парадоксальное явление: в клетках и тканях имеется избыток кислорода, а усвоить его они не могут, так как он химически неактивен. Вследствие этого в организме быстро формируется патологическое состояние, известное под названием тканевой, или гистотоксической, гипоксии, что проявляется удушьем, тяжелыми нарушениями работы сердца, судорогами, параличами. При попадании в организм несмертельных доз яда дело ограничивается металлическим вкусом во рту, покраснением кожи и слизистых оболочек, расширением зрачков, рвотой, одышкой и головной болью. С другой стороны, если животный организм адаптирован к низкому уровню кислородного обмена, то его чувствительность к цианидам резко снижается. Выдающимся русским фармакологом Н. П. Кравковым в. начале этого века был установлен любопытный факт: во время зимней спячки ежи переносят такие дозы цианида калия, которые во много раз превосходят смертельные. Стойкость ежей к цианиду Н. П. Кравков объяснял тем, что в условиях зимней спячки при низкой температуре тела потребление кислорода значительно снижено и животные лучше переносят торможение его усвоения клетками.[168] Однако не весь яд, попавший в организм, взаимодействует с дыхательными ферментами. Некоторое его количество выделяется в неизмененном виде с выдыхаемым воздухом и подвергается детоксикации с образованием в крови безвредных продуктов за счет реакций с сахарами, соединениями, содержащими серу, и кислородом. Вероятно, именно данное обстоятельство определяет отсутствие у синильной кислоты и других цианидов выраженных кумулятивных свойств. Иными словами, когда эти яды действуют в субтоксических дозах, организм справляется с ними самостоятельно, без вмешательства извне. Так, если концентрация синильной кислоты во вдыхаемом воздухе не превышает 0,01–0,02 мг/л, то она оказывается практически безопасной в течение нескольких часов. Увеличение концентрации яда только до 0,08–0,1 мг/л уже опасно для жизни из-за истощения защитных механизмов обезвреживания цианидов.
Способность CN-ионов обратимо тормозить тканевое дыхание и тем понижать уровень обменных процессов неожиданно оказалась весьма ценной для профилактики и лечения радиационных поражений. Это связано с тем, что в механизме повреждающего действия ионизирующих излучений на клеточные структуры ведущую роль играют продукты радиолиза воды (Н2О2, НО2, О, ОН и др.), которые окисляют многие макромолекулы, в том числа ферменты тканевого дыхания. Цианиды, обратимо блокируя эти ферменты, защищают их от действия этих биологически активных веществ, образующихся под влиянием радиации. Иными словами, комплекс «цианид-фермент» — становится относительно устойчивым к облучению. После лучевого воздействия он диссоциирует вследствие понижения концентрации CN-ионов в биофазе из-за обезвреживания их в крови и выделения из организма. В качестве цианидного радиозащитного средства наибольшее распространение получил амигдалин.[169] Любопытно, что еще более 40 лет назад в опытах на нескольких видах животных было установлено противолучевое (как лечебное, так и профилактическое) действие окиси углерода. Экспериментальные данные свидетельствуют, что радиозащитное значение имеет блокада окисью углерода гемоглобина, а не ингибирование ею ферментов тканевого дыхания. По-видимому, при этом сказывается общее снижение уровня кислородного обмена, что в свою очередь уменьшает образование названных кислородсодержащих радикалов. Однако на практике это свойство окиси углерода не используется, так как проявляется оно при высокой концентрации карбоксигемоглобина.
2белок — R — Fe3+ + 1/2O22-,
восстановленная окисленная
цитохромоксидаза цитохромоксидаза
2) 1/2O22- + 2H+ → H2O.
Оказалось, что синильная кислота, точнее CN-ион, вследствие особого химического сродства к трехвалентному железу избирательно (хотя и обратимо) взаимодействует с окисленными молекулами цитохромоксидазы. Тем самым тормозится течение нормального процесса тканевого дыхания.[167] Таким образом, блокируя один из железосодержащих дыхательных ферментов, цианиды вызывают парадоксальное явление: в клетках и тканях имеется избыток кислорода, а усвоить его они не могут, так как он химически неактивен. Вследствие этого в организме быстро формируется патологическое состояние, известное под названием тканевой, или гистотоксической, гипоксии, что проявляется удушьем, тяжелыми нарушениями работы сердца, судорогами, параличами. При попадании в организм несмертельных доз яда дело ограничивается металлическим вкусом во рту, покраснением кожи и слизистых оболочек, расширением зрачков, рвотой, одышкой и головной болью. С другой стороны, если животный организм адаптирован к низкому уровню кислородного обмена, то его чувствительность к цианидам резко снижается. Выдающимся русским фармакологом Н. П. Кравковым в. начале этого века был установлен любопытный факт: во время зимней спячки ежи переносят такие дозы цианида калия, которые во много раз превосходят смертельные. Стойкость ежей к цианиду Н. П. Кравков объяснял тем, что в условиях зимней спячки при низкой температуре тела потребление кислорода значительно снижено и животные лучше переносят торможение его усвоения клетками.[168] Однако не весь яд, попавший в организм, взаимодействует с дыхательными ферментами. Некоторое его количество выделяется в неизмененном виде с выдыхаемым воздухом и подвергается детоксикации с образованием в крови безвредных продуктов за счет реакций с сахарами, соединениями, содержащими серу, и кислородом. Вероятно, именно данное обстоятельство определяет отсутствие у синильной кислоты и других цианидов выраженных кумулятивных свойств. Иными словами, когда эти яды действуют в субтоксических дозах, организм справляется с ними самостоятельно, без вмешательства извне. Так, если концентрация синильной кислоты во вдыхаемом воздухе не превышает 0,01–0,02 мг/л, то она оказывается практически безопасной в течение нескольких часов. Увеличение концентрации яда только до 0,08–0,1 мг/л уже опасно для жизни из-за истощения защитных механизмов обезвреживания цианидов.
Способность CN-ионов обратимо тормозить тканевое дыхание и тем понижать уровень обменных процессов неожиданно оказалась весьма ценной для профилактики и лечения радиационных поражений. Это связано с тем, что в механизме повреждающего действия ионизирующих излучений на клеточные структуры ведущую роль играют продукты радиолиза воды (Н2О2, НО2, О, ОН и др.), которые окисляют многие макромолекулы, в том числа ферменты тканевого дыхания. Цианиды, обратимо блокируя эти ферменты, защищают их от действия этих биологически активных веществ, образующихся под влиянием радиации. Иными словами, комплекс «цианид-фермент» — становится относительно устойчивым к облучению. После лучевого воздействия он диссоциирует вследствие понижения концентрации CN-ионов в биофазе из-за обезвреживания их в крови и выделения из организма. В качестве цианидного радиозащитного средства наибольшее распространение получил амигдалин.[169] Любопытно, что еще более 40 лет назад в опытах на нескольких видах животных было установлено противолучевое (как лечебное, так и профилактическое) действие окиси углерода. Экспериментальные данные свидетельствуют, что радиозащитное значение имеет блокада окисью углерода гемоглобина, а не ингибирование ею ферментов тканевого дыхания. По-видимому, при этом сказывается общее снижение уровня кислородного обмена, что в свою очередь уменьшает образование названных кислородсодержащих радикалов. Однако на практике это свойство окиси углерода не используется, так как проявляется оно при высокой концентрации карбоксигемоглобина.
Антицианиды
Сахар и сера обезвреживают цианиды
В конце прошлого века было подмечено, что сахар способен обезвреживать цианиды. Однако это явление не подвергалось химической оценке до 1915 г., когда немецкие химики Рупп и Гольце показали, что глюкоза, соединяясь с синильной кислотой и другими цианидами, образует нетоксичное соединение — циангидрин: Некоторые продукты окисления глюкозы, например ди-оксиацетон
Некоторые продукты окисления глюкозы, например ди-оксиацетон  , также способны образовывать циангидрины. Особенно активно эта реакция протекает при профилактическом использовании сахаров. Не случайно поэтому при опасности контакта с цианидами с давних пор рекомендуется держать за щекой кусочек сахара. В этой связи нельзя не вспомнить совершенное в Петрограде в декабре 1916 г. убийство Распутина, которого, как известно, вначале пытались отравить цианидом калия, примешанным к кремовым пирожным и портвейну. Однако яд не подействовал, что в последующем с достаточным основанием связали с защитными свойствами сахара, содержавшегося в пирожных и вине. Небезынтересно, что особое внимание на этот эпизод обратили французские военные химики, у которых были свои причины следить за всем, что относилось к действию цианидов: именно тогда во Франции усиленноразрабатывались способы применения синильной кислоты на войне.
В настоящее время в качестве циангидринообразующих антидотов реальное значение имеют водные растворы глюкозы (5%, 40%-ные), вводимые в экстренных случаях внутривенно. Но глюкоза и другие сахара реагируют только с ядом, циркулирующим в крови. Поскольку в крови постоянно растворено определенное количество сахара (800–1200 мг/л, или 4,4–6,5 ммоль/л), возможно обезвреживание медленно поступающих небольших доз цианидов и без дополнительного введения сахара в организм. В то же время яд, связавшийся с клеточными структурами, уже недосягаем для сахаров. К тому же реакция образования циангидринов протекает медленно. Все это требует применения более эффективных противоядий.
Как уже отмечалось, при попадании в организм небольших количеств цианидов в крови образуются безвредные их соединения с серой, получившие название роданидов. Этот естественный способ детоксикации, открытый в 90-х годах прошлого столетия, реализуется за счет наличия в организме веществ, способных отщеплять серу, например таких аминокислот, как цистии, цистеин, глутатион. В конце прошлого века для искусственного образования роданидов при цианидных интоксикациях С. Ланг впервые предложил тиосульфат натрия, легко отдающий серу.[170] В последующем был установлен важный факт: реакция роданообразования нуждается в обязательном участии специального катализатора — фермента роданазы, находящегося в клетках печени. Эта реакция протекает в присутствии кислорода по схеме:
Na2S2О3 + HCN + О
, также способны образовывать циангидрины. Особенно активно эта реакция протекает при профилактическом использовании сахаров. Не случайно поэтому при опасности контакта с цианидами с давних пор рекомендуется держать за щекой кусочек сахара. В этой связи нельзя не вспомнить совершенное в Петрограде в декабре 1916 г. убийство Распутина, которого, как известно, вначале пытались отравить цианидом калия, примешанным к кремовым пирожным и портвейну. Однако яд не подействовал, что в последующем с достаточным основанием связали с защитными свойствами сахара, содержавшегося в пирожных и вине. Небезынтересно, что особое внимание на этот эпизод обратили французские военные химики, у которых были свои причины следить за всем, что относилось к действию цианидов: именно тогда во Франции усиленноразрабатывались способы применения синильной кислоты на войне.
В настоящее время в качестве циангидринообразующих антидотов реальное значение имеют водные растворы глюкозы (5%, 40%-ные), вводимые в экстренных случаях внутривенно. Но глюкоза и другие сахара реагируют только с ядом, циркулирующим в крови. Поскольку в крови постоянно растворено определенное количество сахара (800–1200 мг/л, или 4,4–6,5 ммоль/л), возможно обезвреживание медленно поступающих небольших доз цианидов и без дополнительного введения сахара в организм. В то же время яд, связавшийся с клеточными структурами, уже недосягаем для сахаров. К тому же реакция образования циангидринов протекает медленно. Все это требует применения более эффективных противоядий.
Как уже отмечалось, при попадании в организм небольших количеств цианидов в крови образуются безвредные их соединения с серой, получившие название роданидов. Этот естественный способ детоксикации, открытый в 90-х годах прошлого столетия, реализуется за счет наличия в организме веществ, способных отщеплять серу, например таких аминокислот, как цистии, цистеин, глутатион. В конце прошлого века для искусственного образования роданидов при цианидных интоксикациях С. Ланг впервые предложил тиосульфат натрия, легко отдающий серу.[170] В последующем был установлен важный факт: реакция роданообразования нуждается в обязательном участии специального катализатора — фермента роданазы, находящегося в клетках печени. Эта реакция протекает в присутствии кислорода по схеме:
Na2S2О3 + HCN + О  HCNS + Na2SО4.
Практическое применение находит 30%-ный раствор тиосульфата натрия, который вводят внутривенно или внутримышечно. Однако роданообразующие противоядия реагируют лишь со свободно циркулирующим в крови ядом и действуют сравнительно медленно, хотя по антидотной активности и превосходят глюкозу и другие сахара. Их рекомендуется применять, как и глюкозу, в комбинации с другими антицианидами.
HCNS + Na2SО4.
Практическое применение находит 30%-ный раствор тиосульфата натрия, который вводят внутривенно или внутримышечно. Однако роданообразующие противоядия реагируют лишь со свободно циркулирующим в крови ядом и действуют сравнительно медленно, хотя по антидотной активности и превосходят глюкозу и другие сахара. Их рекомендуется применять, как и глюкозу, в комбинации с другими антицианидами.
Метгемоглобин как антицианид
Молекулы гемоглобина, входящего в состав эритроцитов, содержат, как известно, атомы двухвалентного железа. Поэтому цианиды, попавшие в кровь, довольно быстро, почти не задерживаясь, устремляются к тем рецепторным структурам, которые включают трехвалентное железо, т. е. к железосодержащим дыхательным ферментам. Еще в конце прошлого столетия внимание токсикологов привлекло свойство метгемоглобина быстро присоединять к себе цианид-ион. Следовательно, — создавалась возможность предохранения дыхательных ферментов от отравляющего действия цианида посредством связывания его в кровяном русле метгемоглобином.[171] Но только в 1929 г. румынские исследователи Младовеану и Георгиу[172] придали этому факту антидотное значение, сохранив жизнь собаки, отравленной смертельной дозой цианида, посредством внутривенного вливания ей раствора сильного метгемоглобинообразователя — нитрита натрия. Из многих веществ этого типа действия в качестве эффективных противоядий в дальнейшем стали использоваться и другие нитросоединения, в том числе органические. Одним из таких препаратов является амилнитрит — изоамиловый эфир азотистой кислоты ((СН3)2-СН-(СН2)2-О-N=0), который применяют подобно нашатырному спирту — дают понюхать с ватки. Реакция взаимодействия метгемоглобина с цианид-ионом, приводящая к образованию нетоксичного комплекса — цианметгемоглобина, протекает по схеме: Hb(Fe3+) MtHb(Fe3+) + CN-
MtHb(Fe3+) + CN- CNMtHb(Fe3+).
гемоглобин метгемоглобин цианметгемоглобин
Но метгемоглобин не только связывает циркулирующий в крови цианид, а и освобождает от него заблокированный дыхательный фермент:
MtHb(Fe3+) + белок — R — Fe3+ — CN → CNMtHb(Fe3+) + белок — R — Fe3+.
ингибированная активная
цитохромоксидаза цитохромоксидаза
Что касается молекулярного механизма этого процесса реактивирования цитохромоксидазы, то он остается нераскрытым. Ясно, что гемоглобин, содержащийся в эритроцитах, непосредственно не взаимодействует с дыхательными ферментами. По-видимому, в силу обратимости реакции ингибирования цитохромоксидазы в биофазе постоянно находятся токсичные CN-ионы, определенное количество которых диффундирует в эритроциты и связывается метгемоглобином. Можно предположить, что тем самым сдвигается равновесие в сторону образования свободных молекул дыхательного фермента. Такой механизм антидотного эффекта основывается, следовательно, на конкуренции метгемоглобина и фермента за связь с токсичным радикалом.
Метгемоглобинообразующими свойствами, как уже отмечалось, обладает и метиленовый синий, однако окисляет он гемоглобин медленнее, чем нитриты. Весьма ценным является комбинированный антидот хромосмон — 1%-ный раствор метиленового синего на 25%-ном растворе глюкозы. Надо иметь в виду, что метгемоглобино-образующие препараты, в особенности нитриты, являются ядовитыми веществами, так как лишают гемоглобин его главного свойства — способности переносить кислород. В известном смысле это тот случай, когда яд выступает в роли противоядия (с целью борьбы с тканевой гипоксией в организме вызывается кислородная недостаточность кровяного типа). Поэтому при отравлении цианидами образование метгемоглобина должно идти до определенного предела. Токсикологи считают, что количество его в крови, превышающее 25–30% от общей массы гемоглобина, может усилить гипоксическое состояние. К тому же одним из опасных побочных свойств нитритных метгемоглобинообразователей является их способность резко снижать артериальное давление вследствие расширения кровеносных сосудов. Попутно напомним, что на этом основано действие нитроглицерина — лекарства, широко применяющегося для снижения кровяного давления и при стенокардии. Передозировка нитритных антидотов может привести к обморочному состоянию, что требует строго дозировать вводимый в организм препарат.[173] Другой отрицательной стороной действия разбираемых антидотов является обратимость реакции образования цианметгемоглобина, вследствие чего он постепенно распадается с выделением токсичного CN-иона. Вот почему для предотвращения повторной интоксикации целесообразно вслед за нитритами или одновременно с ними применять другие антицианиды — тиосульфат натрия а глюкозу, которые будут «подхватывать» отщепляющийся СN-ион. При этом антидотная значимость глюкозы увеличивается ее деметгемоглобинизирующими свойствами: на фоне нитритной метгемоглобинемии она будет ускорять восстановление кровяного пигмента после того, как он выполнит свою роль.
CNMtHb(Fe3+).
гемоглобин метгемоглобин цианметгемоглобин
Но метгемоглобин не только связывает циркулирующий в крови цианид, а и освобождает от него заблокированный дыхательный фермент:
MtHb(Fe3+) + белок — R — Fe3+ — CN → CNMtHb(Fe3+) + белок — R — Fe3+.
ингибированная активная
цитохромоксидаза цитохромоксидаза
Что касается молекулярного механизма этого процесса реактивирования цитохромоксидазы, то он остается нераскрытым. Ясно, что гемоглобин, содержащийся в эритроцитах, непосредственно не взаимодействует с дыхательными ферментами. По-видимому, в силу обратимости реакции ингибирования цитохромоксидазы в биофазе постоянно находятся токсичные CN-ионы, определенное количество которых диффундирует в эритроциты и связывается метгемоглобином. Можно предположить, что тем самым сдвигается равновесие в сторону образования свободных молекул дыхательного фермента. Такой механизм антидотного эффекта основывается, следовательно, на конкуренции метгемоглобина и фермента за связь с токсичным радикалом.
Метгемоглобинообразующими свойствами, как уже отмечалось, обладает и метиленовый синий, однако окисляет он гемоглобин медленнее, чем нитриты. Весьма ценным является комбинированный антидот хромосмон — 1%-ный раствор метиленового синего на 25%-ном растворе глюкозы. Надо иметь в виду, что метгемоглобино-образующие препараты, в особенности нитриты, являются ядовитыми веществами, так как лишают гемоглобин его главного свойства — способности переносить кислород. В известном смысле это тот случай, когда яд выступает в роли противоядия (с целью борьбы с тканевой гипоксией в организме вызывается кислородная недостаточность кровяного типа). Поэтому при отравлении цианидами образование метгемоглобина должно идти до определенного предела. Токсикологи считают, что количество его в крови, превышающее 25–30% от общей массы гемоглобина, может усилить гипоксическое состояние. К тому же одним из опасных побочных свойств нитритных метгемоглобинообразователей является их способность резко снижать артериальное давление вследствие расширения кровеносных сосудов. Попутно напомним, что на этом основано действие нитроглицерина — лекарства, широко применяющегося для снижения кровяного давления и при стенокардии. Передозировка нитритных антидотов может привести к обморочному состоянию, что требует строго дозировать вводимый в организм препарат.[173] Другой отрицательной стороной действия разбираемых антидотов является обратимость реакции образования цианметгемоглобина, вследствие чего он постепенно распадается с выделением токсичного CN-иона. Вот почему для предотвращения повторной интоксикации целесообразно вслед за нитритами или одновременно с ними применять другие антицианиды — тиосульфат натрия а глюкозу, которые будут «подхватывать» отщепляющийся СN-ион. При этом антидотная значимость глюкозы увеличивается ее деметгемоглобинизирующими свойствами: на фоне нитритной метгемоглобинемии она будет ускорять восстановление кровяного пигмента после того, как он выполнит свою роль.
Другие антицианиды
В последнее время все чаще подчеркивается значение кобальтовых соединений при отравлениях синильной кислотой и ее производными. Хотя химическое сродство кобальта к цианидам известно еще с конца прошлого века, практическое его использование в качестве антидота стало возможным с появлением малотоксичных кобальтовых комплексонов. Это прежде всего Со2ЭДТА, молекулы которой связывают отрицательно заряженный CN-ион за счет свободных координационных валентностей. Определенный интерес представляют такие производные кобальта, которые включают остатки меркаптосоединений. Последние сами по себе обладают заметным защитным эффектом при цианидной интоксикации. Так, в экспериментах на животных, отравленных смертельными дозами цианида натрия, было показано антидотное (как профилактическое, так и лечебное) действие СоДПЭС[174] — вещества, в котором кобальт включен в пятичленный цикл: Антицианидом оказался также постоянно необходимый организму витамин B12 (гидроксокобаламин), в молекуле которого к атому кобальта присоединена гидроксильная группа. Его детоксикационное действие сводится к замещению гидроксила на CN-группу. Образующийся в результате данной реакции комплекс есть не что иное, как упомянутый витамин В12.
В нашей лаборатории было установлено, что антикоагулянтный препарат гепарин обладает выраженным противоцианидным действием: он защищает белых мышей от смертельных доз цианида натрия.[175]
Антицианидом оказался также постоянно необходимый организму витамин B12 (гидроксокобаламин), в молекуле которого к атому кобальта присоединена гидроксильная группа. Его детоксикационное действие сводится к замещению гидроксила на CN-группу. Образующийся в результате данной реакции комплекс есть не что иное, как упомянутый витамин В12.
В нашей лаборатории было установлено, что антикоагулянтный препарат гепарин обладает выраженным противоцианидным действием: он защищает белых мышей от смертельных доз цианида натрия.[175]
 Из структуры гепарина следует, что его молекула, включающая глюкуроновую и сернистую кислоты, а также глюкозамин, отщепляя любой из названных компонентов, будет способствовать детоксикации цианидов, а возможно, и реактивированию цитохромоксидазы.
Обезвреживания цианидов в организме можно достичь и с помощью β-оксиэтилметиленамина:
CN
/
HO-CH2-CH2-N=CH2+HCN → HO-CH2-CH2-N
\
CH3
Это показали опыты В. Н. Розенберга,[176] в которых удавалось спасать от гибели кроликов и кошек, отравленных 1,5–2 смертельными дозами цианида.
Новыми противоядиями при цианидных интоксикациях могут стать некоторые акцепторы электронов и протонов. В настоящее время они рассматриваются как средства предупреждения и лечения гистотоксических гипоксий. Одним из таких веществ оказался гидрохинон, который в водной среде одновременно находится в 3 формах — нейтральной (а), окисленной (б) и восстановленной (в):
Из структуры гепарина следует, что его молекула, включающая глюкуроновую и сернистую кислоты, а также глюкозамин, отщепляя любой из названных компонентов, будет способствовать детоксикации цианидов, а возможно, и реактивированию цитохромоксидазы.
Обезвреживания цианидов в организме можно достичь и с помощью β-оксиэтилметиленамина:
CN
/
HO-CH2-CH2-N=CH2+HCN → HO-CH2-CH2-N
\
CH3
Это показали опыты В. Н. Розенберга,[176] в которых удавалось спасать от гибели кроликов и кошек, отравленных 1,5–2 смертельными дозами цианида.
Новыми противоядиями при цианидных интоксикациях могут стать некоторые акцепторы электронов и протонов. В настоящее время они рассматриваются как средства предупреждения и лечения гистотоксических гипоксий. Одним из таких веществ оказался гидрохинон, который в водной среде одновременно находится в 3 формах — нейтральной (а), окисленной (б) и восстановленной (в):
 Способность гидрохинона акцептировать электроны была с успехом использована при цианидной интоксикации в опытах на животных.[177] По-видимому, в условиях тканевой гипоксии гидрохинон разгружает дыхательные ферменты от избытка электронов и, кроме того активирует дегидразное звено клеточного окисления, являющееся резистентным по отношению к цианидам.
Вмешательство в процессы клеточного окисления свойственно и метиленовому синему как препарату, обладающему способностью акцептировать водород. Поскольку в механизме токсического действия цианидов накопление протонов (ядер водорода) играет роль фактора, тормозящего течение реакций биологического окисления, то связывание избытка протонов будет стимулировать эти реакции. Следовательно, в известном смысле метиленовый синий должен рассматриваться также и как препарат, эквивалентный одному из дыхательных ферментов. Однако четко отделить это его действие от метгемоглобинообразующего при цианидной интоксикации практически невозможно.
Способность гидрохинона акцептировать электроны была с успехом использована при цианидной интоксикации в опытах на животных.[177] По-видимому, в условиях тканевой гипоксии гидрохинон разгружает дыхательные ферменты от избытка электронов и, кроме того активирует дегидразное звено клеточного окисления, являющееся резистентным по отношению к цианидам.
Вмешательство в процессы клеточного окисления свойственно и метиленовому синему как препарату, обладающему способностью акцептировать водород. Поскольку в механизме токсического действия цианидов накопление протонов (ядер водорода) играет роль фактора, тормозящего течение реакций биологического окисления, то связывание избытка протонов будет стимулировать эти реакции. Следовательно, в известном смысле метиленовый синий должен рассматриваться также и как препарат, эквивалентный одному из дыхательных ферментов. Однако четко отделить это его действие от метгемоглобинообразующего при цианидной интоксикации практически невозможно.

Рис. 16. Сравнительная антидотная эффективность наиболее значимых антицианидов
Сравнительная антидотная эффективность наиболее значимых антицианидов, изученная в опытах на собаках, представлена на рис. 16, где цифры в кружочках обозначают количество смертельных доз, от которых предохраняет данный антидот или комбинация. Многолетняя практика экспериментального лечения тяжелых цианидных отравлений в нашей лаборатории подтверждает эти данные. В частности, особо эффективной оказывалась комбинация нитрита натрия и тиосульфата натрия. Экстренное внутривенное последовательное введение этих антидотов спасало животных от гибели даже в судорожно-паралитической стадии интоксикации. Опыт показывает, что наряду с комплексным применением противоядий для успешной борьбы с цианидной интоксикацией необходимо использовать и такие реанимационные мероприятия, как искусственное дыхание стимуляция сердечной деятельности, ингаляция кислорода и др. В этой связи сохраняет актуальность инструкция о первой помощи в случае отравления синильной кислотой и ее солями, разработанная около 30 лет назад во Франкфурте-на-Майне одной из фирм по извлечению золота и серебра из руд. Вот ее основные положения:«Сохранять спокойствие! Быстро действовать! Вынести пострадавшего из зараженной зоны; тотчас удалить стесняющие тело части одежды, не допускать охлаждения пациента (накрывание, грелки) и вызвать врача. а) Если пострадавший находится еще в сознании, то … разбивать ампулы с амилнитритом и давать вдыхать больному в течение 10–15 секунд, но в общем не более 8 раз. В случае если цианиды попали внутрь при глотании, готовят смесь 2 г сульфата железа и 10 г окиси магния в 100 см3 воды и дают выпить эту смесь пострадавшему, чтобы вызвать рвоту (ни в коем случае не давать при потере сознания). б) Если пострадавший без сознания, то немедленно провести энергичное искусственное дыхание …, дать амилнитрит (как это описано в пункте „а“). Не прекращать искусственное дыхание, особенно при доставке в больницу, и производить его до возвращения сознания у пациента. Как только прибудет врач, рекомендуется, чтобы он ввел … раствор нитрита натрия и в заключение той же иглой для инъекций — … раствор тиосульфата натрия. в) Если цианид попал в рану или ссадину на коже и брызги синильной кислоты попали на кожу, то эти места следует тщательно промыть водой и затем 5%-ным раствором бикарбоната натрия… При попадании брызг в глаза провести особенно тщательное и длительное промывание и доставить пострадавшего к глазному врачу».[178]
ГЛАВА 7 Лекарственные интоксикации и антидоты
Одно из наиболее распространенных осложнений фармакотерапии — токсическое действие лекарств. По данным отечественных и зарубежных авторов, в настоящее время от 11 до 13% всех отравлений вызываются лекарствами. Основные их причины — передозировка медикаментозных средств или же нарушения функционирования органов выделения и ферментных систем, обеспечивающих биотрансформацию лекарств. Повышенная чувствительность отдельных лиц к лекарственным препаратам может возникнуть из-за недостаточной функции печени или почек. В этих случаях лекарственное вещество накапливается в организме и наступает его токсическое действие от обычных доз, в особенности при длительном применении. Отравления могут быть также следствием нерациональной комбинации и несовместимости медикаментов, что в свою очередь приводит к изменению скорости метаболизма лекарств, их выделения из организма, связывания с белками, а также к нарушению всасывания в желудочно-кишечном тракте. Это особенно важно отметить в связи с растущей тенденцией к одновременному приему нескольких лекарственных препаратов с целью усиления терапевтического эффекта. Не исключается возникновение токсических осложнений и при чрезмерно быстром введении лекарств в принятых дозах или же при нарушении способов их введения. Надо также отметить существенную роль составных частей пищи в усвоении организмом лекарственных препаратов и их фармако-динамике, что косвенно может определить возникновение и развитие медикаментозных интоксикаций. Так, ряд клиницистов и фармакологов как в нашей стране, так и за рубежом обратили внимание, что при приеме лекарств — ингибиторов моноаминоксидазы (ипразид, ниаламид) — совместно с пищей и напитками, содержащими большое количество тирамина — биогенного амина с высокой степенью биологической активности (сыры, фасоль, пиво, сухое вино и др.), повышается кровяное давление вплоть до развития гипертензивных кризов с тяжелыми последствиями. Такие осложнения связываются с лекарственным ослаблением ферментной защиты организма против вещества гипертензивного действия, каким является тирамин. При этом обычная реакция его детоксикации (окислительное дезаминирование) резко затормаживается. Все больше накапливается данных об отрицательном влиянии алкогольных напитков на процессы превращения лекарств в организме. В частности, алкоголь потенцирует действие гистамина, барбитуратов, производных хлорпромазина и других веществ. Например, токсичность барбитуратов алкоголь повышает на 50% .[179] Немецкие исследователи Байнхауэр и Шмакке пишут: «Очевидно, что в предстоящие 30 лет фармацевтическая промышленность будет расти более высокими темпами, чем в прошедшие полвека. Уже сейчас производство лекарственных препаратов имеет большое значение для химической промышленности (даже с экономической точки зрения). На их долю приходится 12% мирового производства химической промышленности».[180] Неудивительно поэтому, что в литературе последних лет приводятся многочисленные данные, свидетельствующие о все возрастающей опасности лекарственных интоксикаций. В Советском Союзе создана стройная система контроля за безопасностью применения лекарственных средств. В настоящее время она включает четыре ступени: 1) экспериментальное фармакологическое и токсикологическое исследование препарата; 2) предварительное клиническое изучение лекарства; 3) лимитированное клиническое испытание препарата; 4) контроль за действием лекарств в широкой врачебной практике с информацией о выявленных при этом отклонениях в соответствующий регистрирующий центр.[181] Получаемые таким образом данные служат материалом для выработки более обоснованных рекомендаций по применению лекарств, разработке рациональных схем лечения и мерах профилактики медикаментозных осложнений. Однако, несмотря на строго обоснованные правила применения и достаточно высокий качественный уровень современных лекарственных средств, пока еще нет гарантии полной безопасности их использования.[182] Так, французские исследователи в течение 5 лет наблюдали в специализированной токсикологической клинике 1814 случаев неблагоприятного, главным образом токсического действия лекарств. При этом они отметили, что наибольшее число осложнений давали болеутоляющие, противосвертывающие и нейротропные средства (соответственно 24, 14 и 9%).[183] Что касается причин медикаментозных отравлений, то анализ показывает, что примерно 60% из них возникают из-за передозировки лекарств, а около 40% связаны с различными изменениями внутренней среды организма и наблюдаются при приеме лекарств в допустимых лечебных дозах. При лекарственных отравлениях значительно чаще наблюдается не общая интоксикация, а нежелательное воздействие на те органы или системы, которые являются наиболее чувствительными к тому или иному лекарству.[184] Так, препараты наперстянки в первую очередь действуют токсически на сердце, стрептомицин — на орган слуха, а цитостатические препараты — на кроветворную систему и печень. Все сказанное указывает на большое практическое значение лечебных средств, специфически влияющих на течение медикаментозных отравлений.[185] Мы рассмотрим те из них, которые, будучи химическими соединениями антидотного типа действия, могут непосредственно реагировать с лекарственными веществами или же вмешиваться в функцию тех или иных биоструктур. В связи с необходимостью в ряде случаев применять лекарства в заведомо больших, а нередко и токсических дозах такие средства иногда могут использоваться и профилактически одновременно или незадолго до приема соответствующего лечебного препарата. Логично предположить, что прежде всего это должны быть химические соединения, действующие на организм противоположно ядовитому агенту. И действительно, такие фармакологические антагонисты довольно широко используются на практике, так как способны тормозить или прерывать течение лекарственных отравлений. Их антидотный эффект может рассматриваться как следствие разнонаправленного реагирования с одними и теми или же с разными рецепторными структурами, т. е. основываться на различных видах функционального антагонизма. Так, препараты ацетилхолина (карбахолин и др.), действуя на соответствующие холинорецепторы, замедляют сердечный ритм, расширяют кровеносные сосуды, суживают зрачки, бронхи, усиливают секрецию слюнных и потовых желез, перистальтику кишечника, в то время как катехоламины (например, адреналин) вследствие возбуждения адренорецепторов вызывают в организме противоположные сдвиги. И хотя названные вещества имеют в организме разные «точки приложения», при адреналиновой интоксикации в качестве антидотов показаны соединения типа карбахолина, а при ацетилхолиновой — типа адреналина.[186] И конечно, прямыми функциональными антагонистами адреналиновых лекарственных средств являются α- и β-адреноблокаторы. В частности, при передозировках препаратов адреналина, изадрина, эфедрина противоядием служит α-адреноблокатор фентоламин. Есть еще немало примеров, когда противоположно действующие на организм лекарственные препараты выступают в роли антидотов. Наибольший интерес среди них, безусловно, представляют вещества, обладающие сходным химическим строением и вследствие этого конкурентно влияющие на однотипные рецепторы. Одним из таких соединений является налорфин, весьма близкий по строению к морфину, как это видно из приводимых далее формул. Налорфин (синоним — апторфин) оказался очень эффективным антидотом при острых отравлениях морфином и другими наркотическими препаратами из группы опия (кодеином, промедолом). Широко известно, что применение аналептиков — средств, сильно возбуждающих центральную нервную систему, благотворно сказывается на течении отравлений лекарственными препаратами, вызывающими ее глубокое торможение. Недаром эти средства называют еще оживляющими. К примеру, аналептик бемегрид быстро улучшает состояние отравленных люминалом, барбиталом и другими снотворными, стимулирует дыхание и кровообращение. Можно полагать, что для такого эффекта определенное значение имеет структурное сходство названных фармакологических антагонистов:
Широко известно, что применение аналептиков — средств, сильно возбуждающих центральную нервную систему, благотворно сказывается на течении отравлений лекарственными препаратами, вызывающими ее глубокое торможение. Недаром эти средства называют еще оживляющими. К примеру, аналептик бемегрид быстро улучшает состояние отравленных люминалом, барбиталом и другими снотворными, стимулирует дыхание и кровообращение. Можно полагать, что для такого эффекта определенное значение имеет структурное сходство названных фармакологических антагонистов:
 При тяжелых отравлениях снотворными бемегрид вводят многократно массивными дозами (через каждые 10 мин) до появления рефлексов и нормализации дыхания. Введение бемегрида удобно комбинировать с другим аналептиком — стрихнином, что подчас позволяет добиться излечения в самых безнадежных случаях. Так, например, одной отравленной, принявшей 5 г этаминал-натрия, эти антидоты непрерывно вводились в течение 2 суток. Возвращение сознания было достигнуто после введения больной 1900 мг бемегрида и 162 мг (!) стрихнина. Для сравнения отметим, что обычная лечебная суточная доза стрихнина — 1–3 мг. В этой связи представляет интерес беллоид — лекарственный препарат, содержащий барбитуровую кислоту и алкалоиды красавки. Отравление беллоидом характеризуется явлениями переатропинизации с выраженным снотворным действием барбитуровой кислоты. Вот почему здесь наиболее эффективно как показали И. М. Девагин и соавторы,[187] комплексное применение пилокарпина и прозерина (антагонистов алкалоидов красавки) и бемегрида и стрихнина (антагонистов барбитуратов). Авторы приводят случай успешного антидотного лечения перечисленными препаратами ребенка 1 года 10 мес, которому по ошибке вместо витаминов дали внутрь одномоментно 10 таблеток беллоида (около 30 разовых доз). Естественно предположить, что снотворные и наркотические препараты могут проявить себя как противоядия при интоксикации лекарственными веществами, возбуждающими центральную нервную систему. Так, в частности, действуют гексенал и люминал при отравлении стрихнином и коразолом, когда возникают приступы судорог. Но особенно сильными противосудорожными средствами оказались дифенин и гексамидин. По-видимому, названные фармакологические антагонисты влияют на различные элементы нервных клеток, так как не имеют структурного сходства. Это видно, например, при сопоставлении химических формул стрихнина и дифенина:
При тяжелых отравлениях снотворными бемегрид вводят многократно массивными дозами (через каждые 10 мин) до появления рефлексов и нормализации дыхания. Введение бемегрида удобно комбинировать с другим аналептиком — стрихнином, что подчас позволяет добиться излечения в самых безнадежных случаях. Так, например, одной отравленной, принявшей 5 г этаминал-натрия, эти антидоты непрерывно вводились в течение 2 суток. Возвращение сознания было достигнуто после введения больной 1900 мг бемегрида и 162 мг (!) стрихнина. Для сравнения отметим, что обычная лечебная суточная доза стрихнина — 1–3 мг. В этой связи представляет интерес беллоид — лекарственный препарат, содержащий барбитуровую кислоту и алкалоиды красавки. Отравление беллоидом характеризуется явлениями переатропинизации с выраженным снотворным действием барбитуровой кислоты. Вот почему здесь наиболее эффективно как показали И. М. Девагин и соавторы,[187] комплексное применение пилокарпина и прозерина (антагонистов алкалоидов красавки) и бемегрида и стрихнина (антагонистов барбитуратов). Авторы приводят случай успешного антидотного лечения перечисленными препаратами ребенка 1 года 10 мес, которому по ошибке вместо витаминов дали внутрь одномоментно 10 таблеток беллоида (около 30 разовых доз). Естественно предположить, что снотворные и наркотические препараты могут проявить себя как противоядия при интоксикации лекарственными веществами, возбуждающими центральную нервную систему. Так, в частности, действуют гексенал и люминал при отравлении стрихнином и коразолом, когда возникают приступы судорог. Но особенно сильными противосудорожными средствами оказались дифенин и гексамидин. По-видимому, названные фармакологические антагонисты влияют на различные элементы нервных клеток, так как не имеют структурного сходства. Это видно, например, при сопоставлении химических формул стрихнина и дифенина:
 Но вернемся, однако, к разнонаправленному действию сходных по химическому строению лекарственных веществ и проиллюстрируем его еще несколькими интересными примерами. Первый из них связан с использованием антагонистов фолиевой кислоты. Согласно современным представлениям, фолиевая кислота является необходимым витаминным компонентом процесса клеточного деления, выполняющим важную роль при синтезе нуклеиновых кислот и белков. Выключение или торможение функции фолиевой кислоты с неизбежностью приводит к замедлению или даже к подавлению деления клеток, причем в большей степени это будет сказываться тогда, когда митотическая активность резко возрастает, например при развитии злокачественных опухолей. Вот почему антагонисты фолиевой кислоты оказались эффективными противоопухолевыми (цитотостатическими) препаратами. Таким веществом является ее структурный аналог — метотрексат:
Но вернемся, однако, к разнонаправленному действию сходных по химическому строению лекарственных веществ и проиллюстрируем его еще несколькими интересными примерами. Первый из них связан с использованием антагонистов фолиевой кислоты. Согласно современным представлениям, фолиевая кислота является необходимым витаминным компонентом процесса клеточного деления, выполняющим важную роль при синтезе нуклеиновых кислот и белков. Выключение или торможение функции фолиевой кислоты с неизбежностью приводит к замедлению или даже к подавлению деления клеток, причем в большей степени это будет сказываться тогда, когда митотическая активность резко возрастает, например при развитии злокачественных опухолей. Вот почему антагонисты фолиевой кислоты оказались эффективными противоопухолевыми (цитотостатическими) препаратами. Таким веществом является ее структурный аналог — метотрексат:
 Метотрексат способен вмешиваться в некоторые из тех биохимических реакций, в которых участвует фолиевая кислота, нарушать обмен нуклеиновых кислот и тем самым тормозить безудержное размножение опухолевых клеток. При длительном лечении лейкозов — злокачественных заболеваний крови — нередки передозировки метотрексата. В этих случаях фолиевая кислота, как его конкурентный антагонист, естественно, становится противоядием. Надо также иметь в виду, что такое использование фолиевой кислоты оправдывается и признаками недостаточности ее в организме на фоне длительного применения метотроксата, когда становятся сильно уязвимыми и нормальные клетки. Как и некоторые другие стимуляторы размножения клеток (цианокобаламин, метилурацил), фолиевая кислота рекомендуется также при отравлениях амидопирином, анальгином, бутадионом. Оказалось, что эти широко используемые обезболивающий препараты в больших дозах тормозят выработку лейкоцитов в кроветворной ткани костного мозга.
Другая подобная иллюстрация — разнонаправленное действие камфоры и ее структурного аналога борнеола:
Метотрексат способен вмешиваться в некоторые из тех биохимических реакций, в которых участвует фолиевая кислота, нарушать обмен нуклеиновых кислот и тем самым тормозить безудержное размножение опухолевых клеток. При длительном лечении лейкозов — злокачественных заболеваний крови — нередки передозировки метотрексата. В этих случаях фолиевая кислота, как его конкурентный антагонист, естественно, становится противоядием. Надо также иметь в виду, что такое использование фолиевой кислоты оправдывается и признаками недостаточности ее в организме на фоне длительного применения метотроксата, когда становятся сильно уязвимыми и нормальные клетки. Как и некоторые другие стимуляторы размножения клеток (цианокобаламин, метилурацил), фолиевая кислота рекомендуется также при отравлениях амидопирином, анальгином, бутадионом. Оказалось, что эти широко используемые обезболивающий препараты в больших дозах тормозят выработку лейкоцитов в кроветворной ткани костного мозга.
Другая подобная иллюстрация — разнонаправленное действие камфоры и ее структурного аналога борнеола:
 Камфора синтезируется посредством дегидрирования борнеола, выделенного из пихтового масла. В токсических дозах она вызывает у теплокровных животных судороги, в то время как борнеол является наркотиком. Было установлено, что в препаратах камфоры (как синтетической, так и натуральной) всегда содержится борнеол. Чем его больше, тем в меньшей степени проявляется возбуждающее действие камфоры на центральную нервную систему, так как борнеол является ее конкурентным антагонистом.[188]
Еще один пример такого рода касается синтетических антикоагулянтов типа дикумарина, широко применяющихся с целью торможения процесса свертывания крови. Эти лекарственные препараты резко снижают активность фермента (так называемого голофермента), который катализирует синтез протромбина — важнейшего белкового компонента свертывающей системы крови. Выраженные антидотные свойства при передозировке дикумариновых антикоагулянтов проявляет витамин К (викасол). В настоящее время с достаточным основанием предполагается, что он представляет собою составной элемент активной части голофермента.[189] Полагают, что действие антикоагулянтов сводится к вытеснению витамина К из голофермента, синтезирующего протромбин. Как видно из приводимых ниже формул, строение частей, из которых складывается симметричная структура дикумарина, весьма сходно со строением витамина К, что определяет конкуренцию между ними за место в молекуле голофермента.
Камфора синтезируется посредством дегидрирования борнеола, выделенного из пихтового масла. В токсических дозах она вызывает у теплокровных животных судороги, в то время как борнеол является наркотиком. Было установлено, что в препаратах камфоры (как синтетической, так и натуральной) всегда содержится борнеол. Чем его больше, тем в меньшей степени проявляется возбуждающее действие камфоры на центральную нервную систему, так как борнеол является ее конкурентным антагонистом.[188]
Еще один пример такого рода касается синтетических антикоагулянтов типа дикумарина, широко применяющихся с целью торможения процесса свертывания крови. Эти лекарственные препараты резко снижают активность фермента (так называемого голофермента), который катализирует синтез протромбина — важнейшего белкового компонента свертывающей системы крови. Выраженные антидотные свойства при передозировке дикумариновых антикоагулянтов проявляет витамин К (викасол). В настоящее время с достаточным основанием предполагается, что он представляет собою составной элемент активной части голофермента.[189] Полагают, что действие антикоагулянтов сводится к вытеснению витамина К из голофермента, синтезирующего протромбин. Как видно из приводимых ниже формул, строение частей, из которых складывается симметричная структура дикумарина, весьма сходно со строением витамина К, что определяет конкуренцию между ними за место в молекуле голофермента.
 Помимо синтетических большое клиническое значение имеют естественные, или физиологические, антикоагулянты. Из них прежде всего следует назвать гепарин — мукополисахарид, постоянно циркулирующий в крови человека и высших животных и препятствующий свертыванию крови в кровеносных сосудах (см. с. 147).
Гепарин получают из печени и легких животных в виде различных солей: натриевой, бариевой и др. В связи с широким его применением для профилактики и терапии тромбоэмболических процессов (тромбофлебиты, тромбозы артерий, инфаркты), в том числе и при хирургических операциях с искусственным кровообращением, возможны передозировки гепарина, что приводит к кровотечениям. В настоящее время известен ряд веществ, обладающих способностью снимать противосвертывающее действие гепарина. Наибольшее значение среди них имеют протамины — растворимые соли простых белков (протеинов) с молекулярной массой 2000–12000, из которых практическое применение нашел протаминсульфат. Предполагается, что механизм их антидотного действия состоит в образовании с гепарином малодиссоциирующего комплекса. При этом возможно взаимодействие сульфогрупп гепарина и свободных аминогрупп протаминов.[190] Помимо белковых существует ряд синтетических антагонистов гепарина. Наибольшее практическое значение из них имеет полибрен[191] — полимер на основе четвертичных аммониевых оснований с эмпирической формулой (C13H30BrN2)n. Антидотный эффект этого вещества состоит, по-видимому, в образовании с гепарином полиэлектролитного комплекса с последующим торможением его антикоагулянтной активности.
В связи с необходимостью лечебного применения в больших дозах препаратов наперстянки, строфанта и других сердечных гликозидов возникла настоятельная необходимость лекарственной профилактики их токсических эффектов. Исследованием, проведенным профессором Ф. 3. Меерсоном с соавторами,[192] было выяснено, что стимулирующее влияние сердечных гликозидов на мышцу сердца в значительной степени определяется их взаимодействием с сульфгидрильными группами фермента аденозинтрифосфатазы. Этот фермент, который тормозится большими дозами строфантина и наперстянки, обеспечивает энергией перенос ионов через клеточные мембраны. Своими опытами Т. А. Федорова[193] показала, что унитиол как донатор сульфгидрильных групп значительно снижает у животных отравляющее действие сердечных гликозидов. Так, при применении сверхвысоких доз этих препаратов унитиол предупреждал остановку сердца. Благотворное действие унитиола было отмечено и у больных с явлениями передозировки сердечных гликозидов.[194] Затем это стало основанием к одновременному назначению унитиола и больших доз данных лекарств с целью предупреждения их нежелательного действия или даже к продолжению лечения при наличии явлений интоксикации.[195] Второй механизм антидотного влияния на токсическое действие сердечных гликозидов связан с кальциевым обменом. Оказалось, что повышенна концентрации ионов Са2+ в сердечной мышце усиливает тонизирующее влияние на нее гликозидов, в то время как ионы К+ ослабляют это влияние. Вот почему, связывая кальций и тем самым снижая его концентрацию в миокарде, можно уменьшить неблагоприятное действие больших доз сердечных гликозидов, чему также будет способствовать одновременное усиление действия калия. С этой целью уже более 25 лет используются комплексоны, в частности Nа2ЭТДА.[196] В настоящее время наряду с унитиолом Nа2ЭДТА служит специальным средством экстренного воздействия на интоксикации сердечными гликозидами. Как противоядие Na2ЭДТА используется и при передозировке солей лития (LiCl, Li2CО3), которые применяются в психиатрии для лечения маниакально-депрессивного психоза. Особенно действенно применение Na2ЭДТА при острых и подострых отравлениях хлоридом лития.[197] Антидотный эффект здесь, по-видимому, состоит в вытеснении литием натрия из молекулы Nа2ЭДТА с последующим образованием литиевого комплексона и выведением его из организма.
Фармакотерапия пока еще не может обойтись без значительного числа лекарственных средств, в состав которых входят токсичные металлы: ртуть, мышьяк, висмут, сурьма и др. Это и мочегонные (новурит, промеран), и тонизирующие, и противоанемические (арсенит натрия, мышьяковистый ангидрид), и противопротозойные (солю-сурьмин, аминарсон), и применяемые еще противосифилитические препараты (миарсенол, бийохинол), и некоторые средства лечения желудочно-кишечных заболеваний (нитрат висмута, викалин). Они могут оказывать неблагоприятное побочное действие вследствие ингибирования сульфгидрильных и аминогрупп ферментных и иных биоструктур. Поэтому их целесообразно комбинировать с унитиолом или другими дитиоловыми антидотами, что позволяет предотвратить осложнения при длительном применении перечисленных лекарств в больших дозах, У некоторых из этих лекарственных веществ сродство к SH- и NH2-гpyппaм проявляется после биотрансформации. Так, миарсенол приобретает в организме химио-терапевтическую активность в результате окисления в арсеноксид — вещество типа R-As=О. В дальнейшем арсеноксид реагирует с дитиоловыми ферментами микроорганизмов по схеме:
HS S
\ / \
R-As=O+ R-белок→R-As R-белок+H2O
/ \ /
HS S
Можно полагать, что реакция такого типа лежит в основе прямого противоспирохетозного действия миарсенола. Взаимодействуя с арсеноксидом по этой схеме, унитиол и другие дитиолы, кроме того, способны освобождать от мышьяка заблокированный фермент (см. также с. 100). Здесь следует упомянуть и дефероксамин (синоним — десферал) — сложное производное пропионгидроксамовей кислоты. Оказалось, что этот препарат избирательно реагирует с железом и образует с ним комплексное соединение. Тем самым создается возможность удаления из организма железа при передозировке железосо держащих лекарственных веществ.[198] Ценным свойством деферокс-амина является то, что он не удаляет железо и гемоглобина и ферментов тканевого дыхания и существенно но влияет на выделение других металлов и микроэлементов из организма.
В настоящее время для лечения злокачественных новообразований как цитостатические средства используются производные β-хлорэтиламина: новэмбихин, эмбитол, допан, — сарколизин и др. Все они высокотоксичны, — что существенно осложняет их лечебное применение. Поэтому так важен поиск средств специфической профилактики нежелательного действия лекарственных препаратов типа новэмбихина, В одном экспериментальном исследовании данного направления[199] была установлена высокая степень защитного действия унитиола и меркаптоянтарной кислоты при их одновременном применении с новэмбихином, который вводился животным в летальной дозе, близкой к DL50 (рис. 17). Что касается молекулярного механизма такого эффекта, то надо иметь в виду возможность прямого взаимодействия SH-групп антидотов с высокоактивным иммониевым ионом, образуемым в организме производными β-хлорэтиламина. Помимо этого, предполагается, что унитиол и меркаптоянтарная кислота образуют с тиоловыми биоструктурами дисульфиды и тем защищают их от повреждающего действия токсичных лекарств.
Помимо синтетических большое клиническое значение имеют естественные, или физиологические, антикоагулянты. Из них прежде всего следует назвать гепарин — мукополисахарид, постоянно циркулирующий в крови человека и высших животных и препятствующий свертыванию крови в кровеносных сосудах (см. с. 147).
Гепарин получают из печени и легких животных в виде различных солей: натриевой, бариевой и др. В связи с широким его применением для профилактики и терапии тромбоэмболических процессов (тромбофлебиты, тромбозы артерий, инфаркты), в том числе и при хирургических операциях с искусственным кровообращением, возможны передозировки гепарина, что приводит к кровотечениям. В настоящее время известен ряд веществ, обладающих способностью снимать противосвертывающее действие гепарина. Наибольшее значение среди них имеют протамины — растворимые соли простых белков (протеинов) с молекулярной массой 2000–12000, из которых практическое применение нашел протаминсульфат. Предполагается, что механизм их антидотного действия состоит в образовании с гепарином малодиссоциирующего комплекса. При этом возможно взаимодействие сульфогрупп гепарина и свободных аминогрупп протаминов.[190] Помимо белковых существует ряд синтетических антагонистов гепарина. Наибольшее практическое значение из них имеет полибрен[191] — полимер на основе четвертичных аммониевых оснований с эмпирической формулой (C13H30BrN2)n. Антидотный эффект этого вещества состоит, по-видимому, в образовании с гепарином полиэлектролитного комплекса с последующим торможением его антикоагулянтной активности.
В связи с необходимостью лечебного применения в больших дозах препаратов наперстянки, строфанта и других сердечных гликозидов возникла настоятельная необходимость лекарственной профилактики их токсических эффектов. Исследованием, проведенным профессором Ф. 3. Меерсоном с соавторами,[192] было выяснено, что стимулирующее влияние сердечных гликозидов на мышцу сердца в значительной степени определяется их взаимодействием с сульфгидрильными группами фермента аденозинтрифосфатазы. Этот фермент, который тормозится большими дозами строфантина и наперстянки, обеспечивает энергией перенос ионов через клеточные мембраны. Своими опытами Т. А. Федорова[193] показала, что унитиол как донатор сульфгидрильных групп значительно снижает у животных отравляющее действие сердечных гликозидов. Так, при применении сверхвысоких доз этих препаратов унитиол предупреждал остановку сердца. Благотворное действие унитиола было отмечено и у больных с явлениями передозировки сердечных гликозидов.[194] Затем это стало основанием к одновременному назначению унитиола и больших доз данных лекарств с целью предупреждения их нежелательного действия или даже к продолжению лечения при наличии явлений интоксикации.[195] Второй механизм антидотного влияния на токсическое действие сердечных гликозидов связан с кальциевым обменом. Оказалось, что повышенна концентрации ионов Са2+ в сердечной мышце усиливает тонизирующее влияние на нее гликозидов, в то время как ионы К+ ослабляют это влияние. Вот почему, связывая кальций и тем самым снижая его концентрацию в миокарде, можно уменьшить неблагоприятное действие больших доз сердечных гликозидов, чему также будет способствовать одновременное усиление действия калия. С этой целью уже более 25 лет используются комплексоны, в частности Nа2ЭТДА.[196] В настоящее время наряду с унитиолом Nа2ЭДТА служит специальным средством экстренного воздействия на интоксикации сердечными гликозидами. Как противоядие Na2ЭДТА используется и при передозировке солей лития (LiCl, Li2CО3), которые применяются в психиатрии для лечения маниакально-депрессивного психоза. Особенно действенно применение Na2ЭДТА при острых и подострых отравлениях хлоридом лития.[197] Антидотный эффект здесь, по-видимому, состоит в вытеснении литием натрия из молекулы Nа2ЭДТА с последующим образованием литиевого комплексона и выведением его из организма.
Фармакотерапия пока еще не может обойтись без значительного числа лекарственных средств, в состав которых входят токсичные металлы: ртуть, мышьяк, висмут, сурьма и др. Это и мочегонные (новурит, промеран), и тонизирующие, и противоанемические (арсенит натрия, мышьяковистый ангидрид), и противопротозойные (солю-сурьмин, аминарсон), и применяемые еще противосифилитические препараты (миарсенол, бийохинол), и некоторые средства лечения желудочно-кишечных заболеваний (нитрат висмута, викалин). Они могут оказывать неблагоприятное побочное действие вследствие ингибирования сульфгидрильных и аминогрупп ферментных и иных биоструктур. Поэтому их целесообразно комбинировать с унитиолом или другими дитиоловыми антидотами, что позволяет предотвратить осложнения при длительном применении перечисленных лекарств в больших дозах, У некоторых из этих лекарственных веществ сродство к SH- и NH2-гpyппaм проявляется после биотрансформации. Так, миарсенол приобретает в организме химио-терапевтическую активность в результате окисления в арсеноксид — вещество типа R-As=О. В дальнейшем арсеноксид реагирует с дитиоловыми ферментами микроорганизмов по схеме:
HS S
\ / \
R-As=O+ R-белок→R-As R-белок+H2O
/ \ /
HS S
Можно полагать, что реакция такого типа лежит в основе прямого противоспирохетозного действия миарсенола. Взаимодействуя с арсеноксидом по этой схеме, унитиол и другие дитиолы, кроме того, способны освобождать от мышьяка заблокированный фермент (см. также с. 100). Здесь следует упомянуть и дефероксамин (синоним — десферал) — сложное производное пропионгидроксамовей кислоты. Оказалось, что этот препарат избирательно реагирует с железом и образует с ним комплексное соединение. Тем самым создается возможность удаления из организма железа при передозировке железосо держащих лекарственных веществ.[198] Ценным свойством деферокс-амина является то, что он не удаляет железо и гемоглобина и ферментов тканевого дыхания и существенно но влияет на выделение других металлов и микроэлементов из организма.
В настоящее время для лечения злокачественных новообразований как цитостатические средства используются производные β-хлорэтиламина: новэмбихин, эмбитол, допан, — сарколизин и др. Все они высокотоксичны, — что существенно осложняет их лечебное применение. Поэтому так важен поиск средств специфической профилактики нежелательного действия лекарственных препаратов типа новэмбихина, В одном экспериментальном исследовании данного направления[199] была установлена высокая степень защитного действия унитиола и меркаптоянтарной кислоты при их одновременном применении с новэмбихином, который вводился животным в летальной дозе, близкой к DL50 (рис. 17). Что касается молекулярного механизма такого эффекта, то надо иметь в виду возможность прямого взаимодействия SH-групп антидотов с высокоактивным иммониевым ионом, образуемым в организме производными β-хлорэтиламина. Помимо этого, предполагается, что унитиол и меркаптоянтарная кислота образуют с тиоловыми биоструктурами дисульфиды и тем защищают их от повреждающего действия токсичных лекарств.

Рис. 17. Влияние унитиола и меркаптоянтарной кислоты на летальность мышей, отравленных новэмбихином (Бсльгова, 1968). По оси ординат — % летальных исходов, по оси абсцисс: а — новэмбихин; б — унитиол+новэмбихин; в — меркаптоянтарная кислота+новэмбихин. 1 — доза новэмбихина 2 мг/кг; 2 — доза новэмбихина 3 мг/кг
Вследствие увеличения нервно-психического напряжения в повседневной жизни и его влияния на возникновение и развитие многих заболеваний все большее распространение получают различные психотропные средства: нейролептики, транквилизаторы, антидепрессанты я др. Постоянно расширяющееся бесконтрольное применение этих веществ нередко становится источником как острых, так и хронических интоксикаций. Достаточно из звать такие известные психофармакологические препараты, как мепробамат, триоксазин, аминазин, пипольфен, тизерцин, фенамин, чтобы представить, насколько реальна эта опасность. Экспериментальные и клинические наблюдения свидетельствуют о вмешательстве многих психотропных лекарственных средств в функции адренергических систем. Например, среди антидепрессантов имеется ряд веществ, ингибирующих моноаминоксидазу и тем способствующих накоплению катехоламинов в головном мозге. Такой механизм действия характерен для ипразида, ниамида и других производных гидразина.[200] Из лекарств, угнетающих активность моноаминоксидазы, заслуживают упоминания и противотуберкулезные препараты: тубазид (изониазид), фтивазид, салюзид. В этой связи важно иметь в виду, что, как показали Н. В. Лазарев и соавторы,[201] если лекарства — ингибиторы моно-аминоксидазы — применяются на фоне длительного воздействия промышленных ядов, угнетающих данный фермент (например, сероуглерода), то это может привести к усугублению тяжести соответствующих профессиональ-ных интоксикаций. При объяснении сущности фармакологических эффектов лекарств — производных гидразина — ряд исследователей придают значение непосредственному биохимическому предшественнику серотонина — 5-окситриптофану, содержание которого в мозге увеличивается при лекарственной инактивации меноаминоксидазы. То же самое молено вызвать и такими препаратами, структура которых подобна структуре медиатора. В этом случае осуществляется «обман» фермента, который направляет свою каталитическую активность не на естественный субстрат (медиатор), а на чужеродное вещество. Понятно, что накапливающиеся в синапсах молекулы медиатора будут усиливать поток возбудительных импульсов. Вероятно, таков механизм действия широко известного стимулятора центральной нервной системы — фенамина (рис. 13). Вполне естественно полагать, что для лечения и предупреждения интоксикации лекарствами, угнетающими моноаминоксидазу и другие пиридоксалевые ферменты (например, глутаматдекарбоксилазу), показаны прежде всего пиридоксин и глутаминовая кислота.
Рис. 18. Предполагаемый механизм действия фенамина. Слева — схема инактивации молекулы норадреналина моноаминоксидазой в адренергическом синапсе; справа — сходная по строению с норадреналином молекула фенамина инактивируется тем же ферментом; вследствие этого тормозится окислительное дезаминирование медиатора, который накапливается в синапсе и вызывает избыточную функцию адренорецепторов
Когда лекарственные отравления сопровождаются избыточной функцией адренорецепторов, могут стать полезными препараты из группы β-адреноблокаторов (пропранолол, бензодиксин), которые тормозят потребление и снижают накопление норадреналина в синаптических структурах.[202] Однако пока еще нет достаточного числа наблюдений по практическому применению этих веществ при медикаментозных отравлениях.ГЛАВА 8 Обмен веществ, яды и противоядия
Из предыдущих глав можно было видеть, что большинство ядов прямо или опосредованно нарушают функции ферментно-медиаторных систем организма. В свою очередь и противоядия только тогда могут считаться действенными, когда они нормализуют эти нарушения. Иными словами, в той мере, в какой обменные процессы изменяются под влиянием ядов, они могут стать и объектом воздействия противоядий. В этой связи достаточно, например, вспомнить активное вмешательство в обмен веществ таких ядов и антидотов, — как мышьяк и унитиол, — свинец и комплексоны. Ряд ядов и противоядий заслуживает отдельного рассмотрения из-за особенностей их превращений в организме. Если биохимический механизм изменения структуры яда и какого-то другого вещества сходны, то такое вещество при определенных условиях может затормозить или снизить отравляющее действие яда. Это видно на примере метилового спирта — сильного общетоксического яда, который достаточно широко применяется в органическом синтезе и как растворитель. Сходство его органолептических свойств с этиловым спиртом нередко приводит к использованию метилового спирта с целью алкогольного опьянения. Уже в дозе 100–150 мл метиловый спирт вызывает ряд тяжелых расстройств, среди которых особое место занимает слепота. В организме он трансформируется в основном за счет реакций окисления с участием фермента алкогольдегидрогеназы, но некоторую роль играет и конъюгация с глюкуроновой кислотой. Особое значение для понимания механизма действия этого яда играют его метаболиты (продукты биотрансформации): формальдегид и муравьиная кислота. Именно эти вещества, прежде всего муравьиная кислота, а не сам метиловый спирт определяют развитие наиболее грозных симптомов отравления. Оказалось, что биотрансформация этилового (винного) спирта катализируется в основном тем же ферментом, который окисляет и метиловый спирт, т. е. алкогольдегидрогеназой (рис. 19). Таким образом, окисление обоих спиртов в организме идет по конкурентному типу, а этиловый спирт, введенный отравленному метиловым спиртом, увеличивает долю выведения последнего из организма в неизмененном, т. е. практически безопасном, виде и тем самым тормозит токсический процесс. При этом четкий антидотный эффект достигается внутривенными вливаниями 5%-ного раствора этилового спирта и назначением его внутрь в виде 20 %-ного раствора.[203] Любопытно, что лечебное действие известного противоалкогольного препарата антабуса (тетурама) заключается в ингибировании алкогольдегидрогеназы. Этиловый алкоголь, как видно из рис. 19, в процессе превра щений проходит через фазу ацетальдегида, который обычно быстро окисляется в уксусную кислоту. Антабус, блокируя фермент, задерживает эту реакцию, приводя после приема алкоголя к значительному увеличению концентрации ацетальдегида в крови и к появлению комплекса отрицательных вегетативных реакций. В одной из своих работ профессор Ж. И. Абрамова обратила внимание на то, что чем меньше различия в химической структуре обоих комбинирующихся в организме веществ, «тем больше вероятность их общего пути биотранcформации, а следовательно, и возможность конкурентных взаимоотношений по отношению к окислительным и другим энзимам».title="">[204] Основываясь на собственных данных, полученных в опытах па нескольких видах животных, автор указывает на защитный эффект этилового спирта нем отравлении этиленгликолем (двухатомным спортом) и фторэтанолом. Тем самым тормозится окисление этих спиртов в высокотоксичные метаболиты — щавелевую и фторуксусную кислоты.
Рис. 19. Биотрансформация метилового и этилового спиртов. НАД — никотинамидадениндинуклеотид, кофермент дегидрогеназы, обеспечивающий перенос водорода при окислительно-восстановительных реакциях
Вмешательство в биохимические процессы обмена ядовитых веществ возможно и с помощью ферментных препаратов заместительного действия. Здесь в первую очередь надо вспомнить те ферменты, ингибирование которых при отравлениях определяет существо механизма действия ядов. Мы уже имели возможность убедиться, что введение в организм отравленного препаратов, включающих каталитически активные компоненты ферментов (моноаминоксидазы, пируватоксидазы), является весьма действенным лечебным приемом. В связи с этим несомненный антидотный интерес представляют препараты, включающие целые молекулы ингибируемых ферментов. Одна из первых попыток в данном направлении связана с холинэстеразой, очищенный препарат которой был предложен еще в 1952 г. шведским ученым Аугустинссоном для борьбы с отравлением ФОС. В 1961 г. в США специалисты одной исследовательской лаборатории пришли к выводу о возможности использования электрических угрей как источника холинэстеразы. Оказалось, что в организме этих рыб содержится весьма большое количество фермента. В 1970 г. сотрудниками Института эволюционной физиологии и биохимии им. И. М. Сеченова (г. Ленинград) был разработан метод получения холинэстеразы из эритроцитов крови быка. Тогда же была налажена технология ее промышленного получения с учетом возможного использования в клинике. Надо, однако, иметь в виду, что, кок и любой другой ферментный белок, холинэстераза слабо проникает в ткани нервной системы, с это, естественно, снижает ее лечебное действие. Если фермент ускоряет обезвреживание яде, то дополнительное его впадение в организм должно затормозить течение интоксикации. Таким действием, к примеру, обладает роданаза. Было доказано,[205] что на фоне цианидного отравления этот фермент значительно усиливает дезинтоксикационное роданообразование тиосульфатом натрия и другими донаторами серы. Иное использование ферментов при интоксикациях связано с их способностью вступать в конкурентные отношения с той или иной биоструктурой за связь с ядом или же непосредственно взаимодействовать с его молекулами. Тем самым ферментный препарат как бы принимает удар на себя. Данный механизм защитного действия можно видеть на примере использования протеолитических, т. е. расщепляющих белки, ферментов — химотрипсина и трипсина — при отравлениях ФОС. Установлено, что эти ферменты очень чувствительны к фосфорорганическим ингибиторам и вступают с ними, подобно холинэстеразе, в реакцию фосфорилирования.[206] Несомненный интерес в связи с этим представляют результаты экспериментального исследования, показавшего, что панкреатин (препарат, содержащий трипсин и амилазу, — пищеварительные ферменты поджелудочной железы) обладает выраженными антидотными свойствами по отношению к ряду высокотоксичных ФОС (октаметилу, хлорофосу и др.).[207] На основании этих данных таблетки панкреатина по 0,2–0,5 г и аэрозоли трипсина предлагается использовать в качестве специфического средства профилактики профессиональных отравлений ФОС. Наряду с другими антидотами некоторые авторы рекомендуют применять их также и при появлении признаков интоксикации. Как уже указывалось, окись углерода имеет особое сродство к ферропротеидам, содержащим двухвалентное железо, в тем числе и к дыхательным ферментам — цитохромам. Отсюда практическая ценность полученного в лаборатории профессора Л. А. Тиунова доказательства антидотных свойств цитохрома С при отравлении окисью углерода.[208] В чистом виде цитохром С впервые был выделен в 1935 г. из сердечной мышцы быка. Из 100 кг сердечной мышцы удалось получить 1 г цитохрома. Интересно отметить, что содержание железа в этом препарате (0,34%) было таким же, как и в гемоглобине.[209] Предполагалось, что антидотное действие цитохрома С является следствием насыщения организма железом, содержащимся в этом препарате. Однако исследования итальянских ученых, проведенные в 1957–1959 гг., показали, что железо выполняет защитную роль при отравлении СО в дозировках, превышающих в пересчете на содержание Fe2+ в 30 раз лечебные дозы цитохрома С. К тому же было установлено, что поступающий извне цитохром выводится из организма в неизмененном виде. Тем самым, по-видимому, подтверждается мысль о заместительном лечебном действии этого фермента тканевого дыхания.[210] При прослеживании судьбы многих ядов в организме возникло предположение о возможности направленного воздействия на процессы их метаболизма с целью снижения токсичности. Как было показано многочисленными экспериментами на животных, прежде всего это достигается усилением или ослаблением активности ферментов, ответственных за ход реакций биотрансформации ядовитых веществ. Тем самым применение химических соединений, вмешивающихся в процессы превращения ядов в организме, становится новым и многообещающим направлением антидотного воздействия на течение отравлений. Естественно, что если фермент ускоряет обезвреживание яда, то усиление его активности должно способствовать торможению токсического процесса. И наоборот, в тех случаях, когда токсичность яда увеличивается при его биотрансформации, эта же цель может быть достигнута ослаблением функции соответствующего фермента. В настоящее время известно немало как природных, так и синтетических соединений — активаторов и ингибиторов ферментов, метаболизирующих токсические вещества. К примеру, алдрин и некоторые другие хлорированные углеводороды активируют эетеразы — ферменты, гидролизующие ФОС, что усиливает процесс детоксикации последних. Поэтому введение животным алдрина способствует их выживанию при отравлении фосфорорганическими ядами. Опытным путем было также установлено, что активатором оксидазы, катализирующей окисление барбитуратов в организме, является гексахлорциклогексан, благодаря чему он защищает животных от отравляющего действия больших доз снотворных. В других экспериментах была показана практическая значимость воздействия на метаболизм некоторых промышленных ядов биологических антиоксидантов. Так, токсическое действие бензола, которое связывается с продуктами его окисления — фенолами и полифенолами,[211] может быть резко ослаблено с помощью таких антиоксидантов, как метионин, цистин, цистеамин. Эти серосодержащие соединения угнетают оксидазы, окисляющие бензол в названные опасные для организма метаболиты. И наоборот: на фоне введения животным тиреодина — производного гормона щитовидной железы, повышающего окислительные процессы, отравляющее действие бензола усиливалось. С другой стороны, некоторые анти-оксиданты могут усиливать действие ферментов, катализирующих превращения ядов в организме. Так, цистеин и унитиол оказались эффективными активаторами роданазы. И. П. Лапин в лаборатории профессора В. М. Карасика показал, что эти вещества значительно ускоряют образование роданидов в клетках печени и тем способствуют выживанию экспериментальных животных при тяжелом отравлении цианидом натрия.[212] Активирующее действие цистеина и унитиола, вероятно, зависит от наличия в их молекулах SH-групп. Более 10 лет назад известным канадским ученым Селье[213] при ряде отравлений были установлены защитные свойства сивронолактона (синонимы — альдактон, верошпирон): Данный лекарственный препарат, обладающий диуретическим (мочегонным) действием, является антагонистом альдостерона — гормона коры надпочечников. Оказалось, что антидотный эффект спиронолактона отчетливо выражен при интоксикациях такими лекарственными веществами, как дигитоксин, метацил, новокаин. Кроме того, спиронолактон надежно предотвращал у животных развитие отравления сулемой. Эти результаты наблюдались главным образом при предварительном (незадолго до отравления) введении спиронолактона в организм. Основываясь на своих исследованиях, автор приходит к выводу, что это действие спиронолактона есть следствие его стимулирующего влияния на некоторые микросомальные ферменты клеток печени. Одновременно такой детоксикационный эффект связывается с наличием в молекуле спиронолактона тиоацетатной группы, а также с его способностью активировать синтез сульфгидрильных групп биомолекул и проявлять свойства антиоксиданта в процессах биотрансформации чужеродных веществ.
Но, пожалуй, самым интересным, — самым ценным веществом, способным активно вмешиваться в процессы биотрансформации, является диметиламиноэтиловый эфир дифенилиропилуксусной кислоты, более известный под плаванием SKF-525A:[214]
Данный лекарственный препарат, обладающий диуретическим (мочегонным) действием, является антагонистом альдостерона — гормона коры надпочечников. Оказалось, что антидотный эффект спиронолактона отчетливо выражен при интоксикациях такими лекарственными веществами, как дигитоксин, метацил, новокаин. Кроме того, спиронолактон надежно предотвращал у животных развитие отравления сулемой. Эти результаты наблюдались главным образом при предварительном (незадолго до отравления) введении спиронолактона в организм. Основываясь на своих исследованиях, автор приходит к выводу, что это действие спиронолактона есть следствие его стимулирующего влияния на некоторые микросомальные ферменты клеток печени. Одновременно такой детоксикационный эффект связывается с наличием в молекуле спиронолактона тиоацетатной группы, а также с его способностью активировать синтез сульфгидрильных групп биомолекул и проявлять свойства антиоксиданта в процессах биотрансформации чужеродных веществ.
Но, пожалуй, самым интересным, — самым ценным веществом, способным активно вмешиваться в процессы биотрансформации, является диметиламиноэтиловый эфир дифенилиропилуксусной кислоты, более известный под плаванием SKF-525A:[214]
 Этому веществу посвящены десятки исследований, которые с убедительностью показывают, что оно обладает свойствами универсального ингибитора ферментативных реакций превращений в организме многих чужеродных веществ, в том числе ядов. Так, было обнаружено, что, вводя животным препарат SKF-525A, можно защитить их от отравляющего действия одного из высокотоксичных ФОС — октаметила.[215] Оказалось, что антидотный эффект препарата SKF-525A связан с его способностью подавлять окислительные ферменты, которые в печени активируют превращение октаметила в значительно более токсичное вещество — оксиметил:
Этому веществу посвящены десятки исследований, которые с убедительностью показывают, что оно обладает свойствами универсального ингибитора ферментативных реакций превращений в организме многих чужеродных веществ, в том числе ядов. Так, было обнаружено, что, вводя животным препарат SKF-525A, можно защитить их от отравляющего действия одного из высокотоксичных ФОС — октаметила.[215] Оказалось, что антидотный эффект препарата SKF-525A связан с его способностью подавлять окислительные ферменты, которые в печени активируют превращение октаметила в значительно более токсичное вещество — оксиметил:
 И наоборот, в тех случаях, когда окислительные или иные реакции превращения чужеродных веществ приводят к их детоксикации, препарат SKF-525A, угнетая эта реакции, усиливает биологическую активность чужеродных веществ. Это можно видеть на примере наркотиков (морфина, кодеина и др.) и снотворных из группы барбитуратов, действие которых резко усиливается и удлиняется при предварительном введении животным (крысам, кошкам, — собакам) препарата SKF-525A. Дальнейшие исследования показали способность препарата SKF-525A как политронного блокатора процессов биотрансформации тормозить такие реакции, как дезаминирование, восстановление, синтез с глюкуроновой кислотой.
Пока нет еще точных данных, позволяющих представить интимный механизм действия активаторов и ингибиторов процессов превращения ядов в организме. Можно лишь с достаточной достоверностью считать, что основным местом, где развертывается действие этих веществ, является микросомальная фракция печеночных клеток, в которой вырабатывается большинство ферментов-биотрансформаторов. При этом активаторы увеличивают число молекул микросомальных ферментов, ускоряя их синтез или снижая скорость распада. Ингибиторы оказывают противоположный эффект.
Согласно одним данным, активаторы вмешиваются в функции генетических систем синтеза ферментных (белковых) структур посредством ускорения образования молекул информационной РНК.
С другой стороны, полагают, что на молекулярном уровне эффект ингибиторов может заключаться в конкурентном их взаимодействии с ферментами — катализаторами превращений ядов в организме. Например, установлено,[216] что препарат SKF-525A реагирует с активными центрами фермента N-деметилазы, инактивирующей в организме морфин. Тем самым ингибитор пролонгирует действие наркотика.
Таким образом, химические соединения — стимуляторы и блокаторы процессов биотрансформации ядовитых веществ с достаточным основанием могут быть причислены к противоядиям и как справедливо отметил профессор В. И. Розенгарт,[217] дальнейшее изучение этих соединений при все возрастающем интересе к ним как биохимиков, так и токсикологов будет способствовать разработке новых действенных специфических средств борьбы с отравлениями.
В последние годы появилось немало доказательств усиления реакций превращения многих чужеродных соединений посредством предварительного введения этих веществ в организм в малых дозах. Давно было отмечено, что ряд ядовитых веществ при повторном поступления в организм постепенно теряет первоначальную токсичность и что при этом развивается привыкание к ним на более или менее длительный период. В связи с этим можно вспомнить антидот царя Митридата. Как уже отмечалось, постепенно увеличивая принимаемую внутрь дозу яда, Митридат достиг того, что мог совершенно безопасно принимать такое его количество, которое для всякого другого оказалось бы смертельным. Такого рода устойчивость к высокотоксичным веществам, формирующаяся в организме путем постепенного длительного их приема, была впоследствии названа митридатизмом. Это явление наиболее часто отмечалось при употреблении снотворных и наркотических веществ. Уже в нашу эпоху фантастическую устойчивость организма к громадным дозам наркотика (опиума) продемонстрировал английский писатель Томас Квинсей (1785–1859 гг.), который в течение почти 20 лет практиковал свою собственную форму митридатизма, основанную на своеобразной иммунизации организма ядом. «В кульминационной фазе моей карьеры опиомана, — писал Квинсей, — … моя ежедневная норма составляла восемь тысяч капель опия, что означает обычную больничную дозу на 320 больных».[218] В настоящее время такая резистентность организма связывается с активированием ферментативных процессов обезвреживания ядов, что в свою очередь сопровождается образованием и выделением все возрастающего количества биологически инертных метаболитов. По-видимому, в ответ на повторное введение чужеродного вещества организм интенсивно формирует для борьбы с ним все большее количество ферментов-инактиваторов. Это явление, получившее название самостимуляции ферментов, или ослабления эффекта дозы, есть, следовательно, не что иное, как ускоренный синтез белков-катализаторов, способствующий адаптации организма к токсическому воздействию. Кроме того, надо иметь в виду, что помимо самостимуляции ферментов в реакциях организма на повторяющееся воздействие того или иного химического агента проявляется снижение чувствительности к нему соответствующих рецепторных структур.
Нечто подобное можно видеть при повторяющемся приеме одной и той же дозы некоторых лекарств. Это, например, наблюдается при применении больными бутадиена (фенилбутазона) — болеутоляющего и жаропонижающего препарата, когда обычная его суточная доза дает прогрессивно уменьшающийся эффект. Сходное явление было продемонстрировано в опытах на мышах и крысах, у которых при регулярном введении фиксированных доз барбитуратов сон становился все менее продолжительным. Индукция синтеза ферментов, вызывающих биотрансформацию этих и ряда других лекарственных веществ при их повторном введении, доказана экспериментально. При этом возвращение содержания микросомальных ферментов к исходному уровню наблюдалось не ранее чем через 10 недель после лекарственного воздействия. Здесь уместно отметить, что названные лечебные препараты могут стимулировать функцию ферментов, инактивирующих другие лекарственные вещества, в частности дикума-риновые антикоагулянты. Вот почему последние могут не оказать лечебного действия, если больные одновременно получают барбитураты или бутадион.[219] С другой стороны, в последнее время была показана возможность развития так называемой энзиматической адаптации, когда продолжительное влияние на организм некоторых ядов ведет к усилению их токсичности из-за активирования ферментов, разрушающих глюкуроновую кислоту и другие вещества, необходимые для образования безвредных конъюгатов. Подобное явление может наблюдаться также тогда, когда многократное токсическое воздействие стабилизирует ферменты, трансформирующие яды в опасные для организма продукты. Например, при повторяющемся введении животным малых доз метилового спирта резко усиливается его действие вследствие, по-видимому, активирования алкогольдегидрогеназы и ускорения превращения яда в высокотоксичные метаболиты. Таким образом, сами ядовитые вещества в определенных условиях могут оказаться специфическими средствами направленного воздействия на токсический процесс.
И наоборот, в тех случаях, когда окислительные или иные реакции превращения чужеродных веществ приводят к их детоксикации, препарат SKF-525A, угнетая эта реакции, усиливает биологическую активность чужеродных веществ. Это можно видеть на примере наркотиков (морфина, кодеина и др.) и снотворных из группы барбитуратов, действие которых резко усиливается и удлиняется при предварительном введении животным (крысам, кошкам, — собакам) препарата SKF-525A. Дальнейшие исследования показали способность препарата SKF-525A как политронного блокатора процессов биотрансформации тормозить такие реакции, как дезаминирование, восстановление, синтез с глюкуроновой кислотой.
Пока нет еще точных данных, позволяющих представить интимный механизм действия активаторов и ингибиторов процессов превращения ядов в организме. Можно лишь с достаточной достоверностью считать, что основным местом, где развертывается действие этих веществ, является микросомальная фракция печеночных клеток, в которой вырабатывается большинство ферментов-биотрансформаторов. При этом активаторы увеличивают число молекул микросомальных ферментов, ускоряя их синтез или снижая скорость распада. Ингибиторы оказывают противоположный эффект.
Согласно одним данным, активаторы вмешиваются в функции генетических систем синтеза ферментных (белковых) структур посредством ускорения образования молекул информационной РНК.
С другой стороны, полагают, что на молекулярном уровне эффект ингибиторов может заключаться в конкурентном их взаимодействии с ферментами — катализаторами превращений ядов в организме. Например, установлено,[216] что препарат SKF-525A реагирует с активными центрами фермента N-деметилазы, инактивирующей в организме морфин. Тем самым ингибитор пролонгирует действие наркотика.
Таким образом, химические соединения — стимуляторы и блокаторы процессов биотрансформации ядовитых веществ с достаточным основанием могут быть причислены к противоядиям и как справедливо отметил профессор В. И. Розенгарт,[217] дальнейшее изучение этих соединений при все возрастающем интересе к ним как биохимиков, так и токсикологов будет способствовать разработке новых действенных специфических средств борьбы с отравлениями.
В последние годы появилось немало доказательств усиления реакций превращения многих чужеродных соединений посредством предварительного введения этих веществ в организм в малых дозах. Давно было отмечено, что ряд ядовитых веществ при повторном поступления в организм постепенно теряет первоначальную токсичность и что при этом развивается привыкание к ним на более или менее длительный период. В связи с этим можно вспомнить антидот царя Митридата. Как уже отмечалось, постепенно увеличивая принимаемую внутрь дозу яда, Митридат достиг того, что мог совершенно безопасно принимать такое его количество, которое для всякого другого оказалось бы смертельным. Такого рода устойчивость к высокотоксичным веществам, формирующаяся в организме путем постепенного длительного их приема, была впоследствии названа митридатизмом. Это явление наиболее часто отмечалось при употреблении снотворных и наркотических веществ. Уже в нашу эпоху фантастическую устойчивость организма к громадным дозам наркотика (опиума) продемонстрировал английский писатель Томас Квинсей (1785–1859 гг.), который в течение почти 20 лет практиковал свою собственную форму митридатизма, основанную на своеобразной иммунизации организма ядом. «В кульминационной фазе моей карьеры опиомана, — писал Квинсей, — … моя ежедневная норма составляла восемь тысяч капель опия, что означает обычную больничную дозу на 320 больных».[218] В настоящее время такая резистентность организма связывается с активированием ферментативных процессов обезвреживания ядов, что в свою очередь сопровождается образованием и выделением все возрастающего количества биологически инертных метаболитов. По-видимому, в ответ на повторное введение чужеродного вещества организм интенсивно формирует для борьбы с ним все большее количество ферментов-инактиваторов. Это явление, получившее название самостимуляции ферментов, или ослабления эффекта дозы, есть, следовательно, не что иное, как ускоренный синтез белков-катализаторов, способствующий адаптации организма к токсическому воздействию. Кроме того, надо иметь в виду, что помимо самостимуляции ферментов в реакциях организма на повторяющееся воздействие того или иного химического агента проявляется снижение чувствительности к нему соответствующих рецепторных структур.
Нечто подобное можно видеть при повторяющемся приеме одной и той же дозы некоторых лекарств. Это, например, наблюдается при применении больными бутадиена (фенилбутазона) — болеутоляющего и жаропонижающего препарата, когда обычная его суточная доза дает прогрессивно уменьшающийся эффект. Сходное явление было продемонстрировано в опытах на мышах и крысах, у которых при регулярном введении фиксированных доз барбитуратов сон становился все менее продолжительным. Индукция синтеза ферментов, вызывающих биотрансформацию этих и ряда других лекарственных веществ при их повторном введении, доказана экспериментально. При этом возвращение содержания микросомальных ферментов к исходному уровню наблюдалось не ранее чем через 10 недель после лекарственного воздействия. Здесь уместно отметить, что названные лечебные препараты могут стимулировать функцию ферментов, инактивирующих другие лекарственные вещества, в частности дикума-риновые антикоагулянты. Вот почему последние могут не оказать лечебного действия, если больные одновременно получают барбитураты или бутадион.[219] С другой стороны, в последнее время была показана возможность развития так называемой энзиматической адаптации, когда продолжительное влияние на организм некоторых ядов ведет к усилению их токсичности из-за активирования ферментов, разрушающих глюкуроновую кислоту и другие вещества, необходимые для образования безвредных конъюгатов. Подобное явление может наблюдаться также тогда, когда многократное токсическое воздействие стабилизирует ферменты, трансформирующие яды в опасные для организма продукты. Например, при повторяющемся введении животным малых доз метилового спирта резко усиливается его действие вследствие, по-видимому, активирования алкогольдегидрогеназы и ускорения превращения яда в высокотоксичные метаболиты. Таким образом, сами ядовитые вещества в определенных условиях могут оказаться специфическими средствами направленного воздействия на токсический процесс.
Заключение
Все изложенное в данной книге говорит об определенных успехах науки в раскрытии молекулярных механизмов действия многих ядовитых веществ и выяснении сущности процессов их превращения в организме. Это в свою очередь обусловило реальные возможности создания эффективных противоядий, которые или уже стали практически используемыми препаратами, или еще находятся в стадии экспериментальной разработки. При описании действия противоядий мы не разграничивали их по такому признаку и не акцентировали внимание на лечебной стороне вопроса, поскольку стремились ознакомить читателя прежде всего с важнейшими механизмами антидотного эффекта в том виде, в каком они представляются в настоящее время. И здесь необходимо особо подчеркнуть, что успешное специфическое воздействие на токсический процесс с помощью антидотов является хотя и весьма надежным, но лишь одним из нескольких реально значимых принципов борьбы с отравлениями. Это тем более важно иметь в виду, что в настоящее время еще не существует противоядий при интоксикациях многими распространенными ядами: дихлорэтаном, бензолом и рядом его производных, высокотоксичными веществами растительного и животного происхождения и др. Современную практическую токсикологию невозможно представить без многих других неотложных мероприятий (назовем их неспецифическими) по предупреждению и лечению интоксикаций. Не касаясь конкретных показаний к проведению этих мероприятий, перечислим важнейшие из них. 1. Экстренное прекращение дальнейшего поступления (всасывания) яда во внутренние среды организма (промывание желудка, вызывание рвоты, удаление яда из кишечника, а также его нейтрализация при попадании в глаза, на кожу и слизистые оболочки). 2. Ускоренное выведение из организма уже всосавшегося яда и его токсичных метаболитов для максимального уменьшения их количества в крови и тканях. С этой целью при тяжело протекающих острых отравлениях применяются: а) форсированный диурез, т. е. резкое усиление выделительной функции почек как естественного способа очищения организма от токсичных веществ, что достигается введением отравленному больших количеств жидкости и растворов осмотически активных веществ, а также диуретических средств; при ряде тяжелых отравлений форсированный диурез проводится совместно с алкалинизацией (ощелачиванием) плазмы и мочи, что препятствует задержке ядов в тканях, повышает растворимость и тормозит их обратное всасывание в почках; б) увеличение продукции желчи клетками печени и усиление работы органов дыхания с помощью соответствующих лекарственных средств; в) гемодиализ (избирательный обмен различных веществ между плазмой крови и специальным раствором электролитов через поры полупроницаемой мембраны), перитонеальный диализ (введение в брюшную полость гипертонического раствора электролитов, в который ядовитые вещества переходят из крови через брюшину, выполняющую функцию диализирующей мембраны); г) гемосорбция и ее разновидности — плазмо и лимфосорбция (очищение крови от чужеродных и балластных эндогенных веществ посредством подключения кровеносного русла к специальному аппарату с сорбирующими веществами, что одновременно обеспечивает поддержание детоксикационной функции печени); по быстроте и эффективности гемосорбция теперь ставится на первое место из всех способов выведения токсичных веществ из организма. 3. Восстановление и обеспечение нормального функционирования жизненно важных систем и органов: кровообращения, дыхания, центральной нервной системы, печени, почек, а также гуморальной среды организма (электролитный баланс, кислотно-щелочное равновесие, водный обмен). 4. Введение кислорода в организм отравленного как метод патогенетического лечения гипоксических состояний, практически возникающих при всех острых интоксикациях. Необходимым условием успешного кислородного лечения является устранение (или по крайней мере уменьшение) токсических нарушений транспорта кислорода в организме. Опыт показывает, что экспериментальные и клинические данные о разнообразных типах специфического воздействия на токсический процесс могут считаться достоверными лишь тогда, когда позволяют на молекулярном уровне оценить характер взаимодействия ядов, — реактивных структур организма и антидотов. Иными словами, особую токсикологическую значимость приобретает анализ сущности химических (биохимических) и физико-химических процессов, протекающих при таком взаимодействии. Сейчас есть достаточно оснований полагать (и в этом мог убедиться читатель), что наибольшую практическую ценность и перспективность имеют те антидоты, которые в «точках приложения» ядов действуют выборочно на определенные биологические структуры и позволяют тем самым вмешиваться в интимные механизмы жизнедеятельности, в частности в функцию передатчиков нервного возбуждения и рецепторных образований организма. Несомненно также большое значение противоядий, активно влияющих на течение различных обменных процессов. В числе всех этих так называемых функциональных противоядий мы рассмотрели вещества, препятствующие действию яда на рецепторные структуры или блокирующие это действие (атропиноподобные соединения, адреноблокаторы, обратимые ингибиторы ферментов); реактивирующие биоструктуры с последующей окончательной или временной детоксикацией яда (оксимы, унитиол, цистамин); конкурирующие с ядом за связь с рецепторами (кислород, структурные аналоги токсичных лекарств); замещающие биоструктуры, поврежденные или утраченные под воздействием яда (пиридоксин, цитохром С, хлорид кальция); активаторы и ингибиторы ферментов, метаболизирующих яды (препарат SKF-525A, антиоксиданты), и ряд других. Некоторые из них являются анти-дотами многостороннего действия и, значит, могут использоваться при различных отравлениях или яда воздействовать на один и тот же токсический процесс разными путями. Например, глюкоза и метиленовый синий — антицианиды и в то же время восстановители метгемоглобина. Кроме того, глюкоза может быть заместительным антидотом при инсулиновой интоксикации, а метиленовый сивый влиять на процессы тканевого окисления, нарушенные ядами. Здесь уместно отметить, что в последнее время все большее значение в качестве противоядий многостороннего действия приобретают антиоксиданты. В частности, такие вещества, как токоферол, селенит натрия, цистамин и другие содержащие серу аминокислоты, снижают токсичность отдельных ФОС, воздействуя, по-видимому, на соответствующие ферменты, подобно препарату SKF-525A. Кроме того, они тормозят окислительные превращения некоторых токсичных химических соединений в вещества, избирательно влияющие на биоструктуры. Например, антиоксиданты препятствуют окислению анилина в метгемоглобинообразующий метаболит. Однако наличие разнообразных антидотов непрямого типа действия не снижает практической роли препаратов, обезвреживающих яды в организме химическим (физико-химическим) путем. Именно эти противоядия по традиции принято использовать в первую очередь прежде всего из-за доступности способов применения и достаточно уверенного прогнозирования их действия. Подводя итог рассмотрению антидотных средств, приходится констатировать некоторое отставание практики лечения отравлений от достижений экспериментальной токсикологии. На это, например, обратил внимание академик АМН СССР С. Н. Голиков,[220] который, в частности, указал на неиспользуемые реальные возможности применения многих новых холинолитиков и их комбинаций, значительно превосходящих по своей активности атропин и в то же время лучше переносимых человеком. К сожалению, даже в некоторых токсикологических практических руководствах и учебных пособиях подчас не описываются отдельные известные и хорошо зарекомендовавшие себя на практике антидоты (например, актарсин как антидот мышьяковистого водорода, а также цистамин и метиленовый синий как активные средства восстановления метгемоглобина). Не вызывает сомнения, что точная диагностика и наличие быстро и надежно действующего антидота являются необходимыми условиями эффективной борьбы с отравлениями. Но специфическое вмешательство в течение отравления дает желаемый результат тогда, когда антидот вводится в нужном количестве и в наиболее подходящие сроки. В этой связи интересно рассмотреть в динамике воздействие яда и антидота на организм. Можно представить острый токсический процесс графически в виде кривой, которая отображает направление сдвига физиологической функции (например, кровообращения, дыхания, нервно-мышечного аппарата) от нормального ее уровня до максимального проявления с последующим спадом (рис. 20). Если антидот введен в начальном периоде развития отравления, то, будучи антагонистом яда, он способствует замедлению или остановке токсического процесса. Здесь имеет значение доза антидота: когда она недостаточна, то действие яда продолжается, а когда слишком велика то может снизить уровень физиологических функций ниже нормального. На высоте развития интоксикации лечебный эффект может быть достигнут с помощью большей дозы антидота, который действует медленнее. При этом вероятность возврата к исходному уровню уже уменьшается. Если же противоядие начинают применять на последней стадии отравления, когда уже сказывается истощение энергетических ресурсов эффекторных органов и их избыточная функция проявляется в меньшей степени, то взаимоотношения яда и антидота принципиально меняются: из антагонистов они превращаются в синергистов. Здесь еще большее значение приобретает выбор дозы антидота, так как при его передозировке может быть ускорено наступление рокового исхода. Конечно, на этой стадии эффективность антидотного лечения резко снижается. Такое представление о динамической взаимосвязи яда и антидота оказывается справедливым в отношении многих остро протекающих интоксикаций. Из него следует что одной из труднейших задач которую призвана решить токсикология, — является разработка в каждом конкретном случае временных и количественных рекомендаций по использованию антидотов.

Последние комментарии
21 часов 36 минут назад
23 часов 53 минут назад
1 день 14 часов назад
1 день 14 часов назад
1 день 19 часов назад
1 день 23 часов назад